20 أمثلة على الأملاح الحمضية
منوعات / / July 04, 2021
في ال الكيمياء غير العضوية تسمى الأملاح المركبات التي يتم الحصول عليها عند أ حامض يتم استبدال ذرات الهيدروجين بالكاتيونات المعدنية (على الرغم من أنها في بعض الأحيان الكاتيونات غير المعدنية ، على سبيل المثال ، كاتيون الأمونيوم ، NH4+). في حالة محددة من الأملاح الحمضية، يتم استبدال هيدروجين الحمض جزئيًا ، أي بقايا هيدروجين واحدة على الأقل غير مستبدلة كجزء من الملح. في أنها تتميز عن أملاح محايدة، حيث يتم استبدال هيدروجين الحمض تمامًا.
ال انت اخرج تتشكل عادة من خلال التفاعل بين أ حامض و أ هيدروكسيد (يتمركز). في هذه التفاعلات ، تفقد القاعدة عادةً مجموعات الهيدروكسيل (-OH) ويفقدها الحمض. ذرات الهيدروجين (H) ، مكونًا ملحًا متعادلًا ؛ ولكن إذا كان الحمض المعني يحافظ على واحدة على الأقل من ذرات الهيدروجين الخاصة به ، مما يؤدي إلى تغيير الشحنة الكهربائية للتفاعل ، فسنحصل على ملح حامضي أو ملح مهدرج.
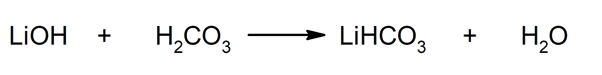
وهكذا ، على سبيل المثال ، يتم الحصول على بيكربونات الليثيوم والماء من التفاعل بين هيدروكسيد الليثيوم وحمض الكربونيك:
تسمية الأملاح الحمضية
يمكن تسمية الأملاح الحمضية وفقًا لـ ثلاثة أنواع التسميات الأكثر شيوعًا:
أمثلة على الأملاح الحمضية
- بيكربونات الصوديوم (ناكو3). تسمى أيضًا كربونات هيدروجين الصوديوم (IV) ، وهي مادة صلبة بلورية بيضاء ، قابلة للذوبان في الماء ، ويمكن العثور عليها في الطبيعة في الحالة المعدنية أو يمكن إنتاجه في المختبر. إنه أحد أفضل الأملاح الحمضية المعروفة ويستخدم على نطاق واسع في صناعة الحلويات أو الصيدلة أو صناعة الزبادي.
- بيكربونات الليثيوم (LiHCO3). تم استخدام هذا الملح الحمضي كعامل احتجاز لثاني أكسيد الكربون2 في الحالات التي يكون فيها هذا الغاز غير مرغوب فيه ، كما هو الحال في مهمات الفضاء "أبولو" في أمريكا الشمالية.
- البوتاسيوم هيدروجين فوسفات (KH2ص4). إنها مادة صلبة بلورية ، عديمة الرائحة ، قابلة للذوبان في الماء ، تستخدم على نطاق واسع في صناعات مختلفة مثل خميرة غذاء، عامل مخلب ، مقوي غذائي ومساعد في عمليات التخمير.
- سلفات الصوديوم (ناهسو4). إنه ملح حامض يتكون من معادلة حامض الكبريتيك. يستخدم على نطاق واسع صناعيًا في تكرير المعادن ومنتجات التنظيف. على الرغم من أنها شديدة السمية لبعض شوكيات الجلد ، إلا أنها تستخدم كمادة مضافة في أغذية الحيوانات الأليفة وفي صناعة المجوهرات.
- كبريتيد هيدروجين الصوديوم (ناهس). إنه مركب خطير يجب التعامل معه ، لأنه شديد التآكل وسام. يمكن أن يسبب حروقًا جلدية شديدة وتلفًا للعين لأنه قابل للاحتراق أيضًا.
- فوسفات هيدروجين الكالسيوم (CaHPO4). يتم استخدامه كمكمل غذائي في الحبوب للماشية. إنه مادة صلبة غير قابلة للذوبان في الماء ولكنها قادرة على التبلور عند ترطيبها باستهلاك اثنين الجزيئات من الماء.
- كربونات هيدروجين الأمونيوم ([NH4] HCO3). يُعرف أيضًا باسم "بيكربونات الأمونيوم" ، ويستخدم في صناعة المواد الغذائية مثل الخميرة مادة كيميائية ، على الرغم من أن لها عيوب في حبس الأمونيا وإعطاء الطعام طعمًا سيئًا إذا تم استخدامه فيه إفراط. كما أنها تستخدم في طفايات الحريق ، وصنع الأصباغ ، ولتوسيع المطاط.
- بيكربونات الباريأو (Ba [HCO3]2). إنه ملح حمضي يمكن أن يعكس تفاعل إنتاجه عند تسخينه ويكون غير مستقر للغاية ، إلا في المحلول. يستخدم على نطاق واسع في صناعة السيراميك.
- بيسلفيت الصوديوم (ناهسو3). هذا الملح غير مستقر للغاية وفي وجود الأكسجين فإنه يشتق إلى كبريتات الصوديوم (Na2جنوب غرب4) ، وهذا هو سبب استخدامه في صناعة المواد الغذائية كمادة حافظة ومجففة للأغذية. إنه عامل اختزال شديد وشائع الاستخدام من قبل الإنسان ، ويستخدم أيضًا في تثبيت الألوان.
- سترات الكالسيوم (AC3[ج6ح5أو7]2). يُعرف باسم الملح المر ، ويستخدم كمواد حافظة للأغذية وكمكمل غذائي عندما يرتبط بالحمض الأميني ليسين. إنه مسحوق بلوري أبيض عديم الرائحة.
- فوسفات الكالسيوم (كاليفورنيا [H2ص4]2). وهي مادة صلبة عديمة اللون يتم الحصول عليها من تفاعل هيدروكسيد الكالسيوم وحمض الفوسفوريك ، وتستخدم على نطاق واسع كعامل تخمير أو كسماد في الأعمال الزراعية.
- ثاني فوسفات الكالسيوم (CaHPO4). يُعرف أيضًا باسم فوسفات أحادي الهيدروجين الكالسيوم ، وله ثلاثة أشكال بلورية مختلفة تُستخدم كمادة مضافة في الطعام وهي موجودة في معاجين الأسنان. بالإضافة إلى ذلك ، يتشكل بشكل طبيعي في حصوات الكلى وما يسمى بـ "حصوات الكلى".
- فوسفات المغنيسيوم (مغ4ص2أو8). إنه ملح أبيض بلوري وعديم الرائحة ، قابل للذوبان جزئيًا في الماء. يتم استخدامه في حفظ الطعام ، كمحمض ، كمصحح للحموضة أو كعامل في معالجة دقيق.
- ثنائي أسيتات الصوديوم (ناه [ج2ح3أو2]2). يستخدم هذا الملح كعامل منكه وحافظ في وجبات الطعام مما يمنع أو يؤخر ظهوره الفطر والمتفطرات ، سواء في المنتجات المعبأة بتفريغ الهواء مثل منتجات اللحوم وفي صناعة الدقيق.
- بيكربونات الكالسيوم (Ca [HCO3]2). هو ملح مهدرج ينشأ من كربونات الكالسيوم ، موجود في المعادن مثل الحجر الجيري والرخام وغيرها. يتضمن هذا التفاعل وجود الماء وثاني أكسيد الكربون2لذلك يمكن أن يحدث بشكل عفوي في الكهوف والكهوف الغنية بالكالسيوم.
- فلوريد حمض الروبيديوم (RbHF). يتم الحصول على هذا الملح من تفاعل حمض الهيدروفلوريك (الهيدروجين والفلور) والروبيديوم ، وهو معدن قلوي. والنتيجة هي مركب سام ومسبب للتآكل يجب التعامل معه بحذر.
- فوسفات أحادي الأمونيوم ([NH4] ح2ص4). إنه ملح قابل للذوبان في الماء ينتج عن تفاعل الأمونيا وحمض الفوسفوريك. يستخدم عادة كسماد لأنه يعطي التربة العناصر الغذائية من النيتروجين والفوسفور الضروريين لنمو النبات. وهو أيضًا جزء من مسحوق ABC في طفايات الحريق.
- orthoborate الهيدروجين الزنك (Zn [HBO3]). وهو ملح يستخدم كمطهر وكمادة مضافة في صناعة السيراميك.
- فوسفات أحادي الصوديوم (ناه2ص4). يتم استخدامه في الغالب في المختبرات ، كمحلول "عازل" أو "عازل" ، والذي يمنع التغيرات المفاجئة في درجة الحموضة في المحلول.
- البوتاسيوم الفثالات الهيدروجين (KHP). يُطلق عليه أيضًا "فثالات حمض البوتاسيوم" ، وهو ملح صلب ومستقر في الهواء العادي ، ولهذا السبب غالبًا ما يستخدم كمعيار أساسي في قياسات الرقم الهيدروجيني. كما أنه مفيد كعامل تخزين مؤقت في ملفات تفاعلات كيميائية.
اتبع مع:
