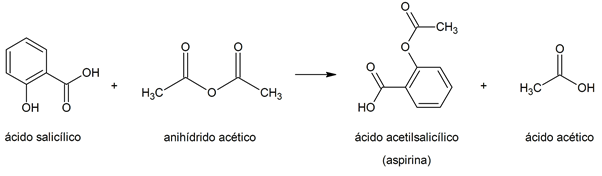20 أمثلة على التفاعلات الكيميائية
منوعات / / July 04, 2021
تسمى تفاعل كيميائي إلى العملية التي بواسطتها واحد أو أكثر مواد كيميائية (تسمى "المواد المتفاعلة") يتم تحويلها وتؤدي إلى ظهور منتجات أخرى (تسمى "المنتجات"). وهكذا ، بالنسبة للمواد المتفاعلة لتوليد المنتجات من خلال تفاعل كيميائي ، يتم إعادة تنظيم ذرات ص الجزيئات الذي يحدث فيه تبادل الطاقة. على سبيل المثال: الاحتراق والأكسدة والتفاعلات الحمضية القاعدية.
ال مركبات كيميائية لديك الطاقة الكيميائية في الروابط بين الذرات التي تتكون منها. عادة ما يتم التعبير عن التفاعلات الكيميائية من خلال المعادلات ، حيث يشار إلى المواد المتفاعلة على اليسار والنواتج على اليمين ، ربط كلا الجزأين بسهم لليمين إذا كان رد الفعل قابلاً للانعكاس أو سهم للخلف وللأمام إذا كان رد فعل تفريغ.
عندما يشار إلى الكميات أو النسب التي تتفاعل بها المواد المتفاعلة ويتم الحصول على المنتجات ، فإننا نتحدث عن تفاعلات متكافئة.
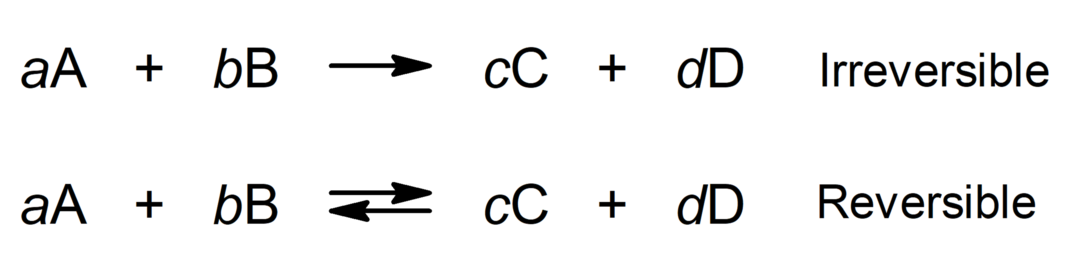
أين:
- A و B هما المتفاعلات.
- C و D هما المنتجان.
- أ ، ب ، ج ، د هي المعاملات المتكافئة (عدد الجزيئات أو الذرات من نوع معين التي تشارك في معادلة كيميائية).
تفاعلات كيميائية يمكن تصنيفها حسب نوع الطاقة التي تطلقها أو تمتصها. بهذا المعنى ، يمكن أن تكون طاردة للحرارة أو ماصة للحرارة (إذا تم إطلاقها أو امتصاصها
الحار) ، خارجي أو داخلي (إذا أطلق أو تمتص الضوء) ، كهربي خارجي أو داخلي (إذا كان ينتج أو يحتاج كهرباء).قوانين التفاعلات الكيميائية
في التفاعلات الكيميائية يتم استيفاء القوانين. الأهم هو قانون حفظ الكتلة أو قانون لافوازييه، التي صاغها هذا الكيميائي عام 1774 ، والتي تفترض أنه في كل تفاعل كيميائي تكون كتلة المواد المتفاعلة مساوية لكتلة المنتجات.
كانت دالتون الذي أكمل شرح هذا القانون بعد بضع سنوات ، من خلال الإشارة إلى أنه في تفاعل كيميائي عدد لا تختلف الذرات عند مقارنة المواد المتفاعلة مع المنتجات ، إلا أن تنظيمها يتغير ، وبالتالي فإن كتلة نفسه يحفظ.
معلمة أخرى مهمة في التفاعلات الكيميائية هي سرعة رد الفعل حيث لا تستغرق جميعها نفس الوقت للإنتاج. يتم تعريف معدل التفاعل على أنه مقدار المنتج الذي يظهر لكل وحدة زمنية أو كمية الكاشف التي تختفي لكل وحدة زمنية.
على الرغم من أن كل تفاعل له سرعة مختلفة ، إلا أن بعض العوامل يمكن أن تؤدي إلى زيادة أو زيادة انخفاض: سطح التلامس بين جزيئات التفاعل ودرجة الحرارة هي بعض من أنهم.
ال المحفزات إنها مواد تزيد من سرعة التفاعل دون تعديل بنيتها. في كثير من الأحيان يتم تنفيذ هذا الدور من قبل البعض المعادن.
أمثلة على التفاعلات الكيميائية
تحدث التفاعلات الكيميائية باستمرار في الطبيعة ، في جسم الإنسان ، في المصانع ، في محطات معالجة النفايات السائلة ، إلخ. بعض الأمثلة هي:
-
الإحتراق
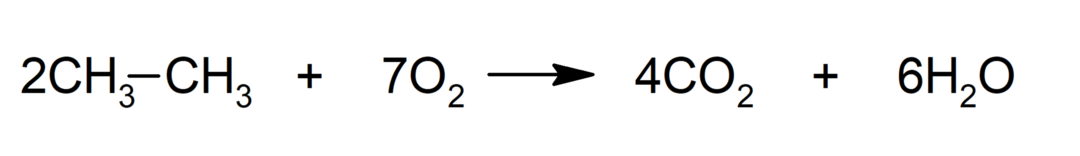
-
الاستبدال
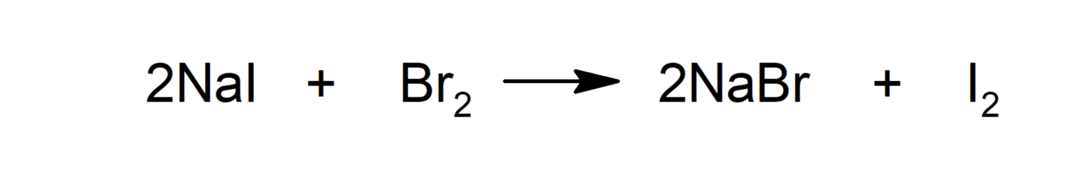
-
إضافة
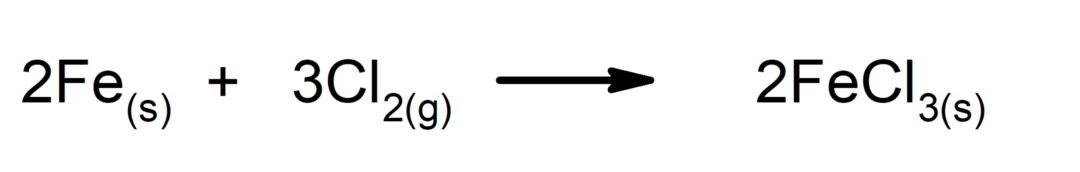
-
إزالة
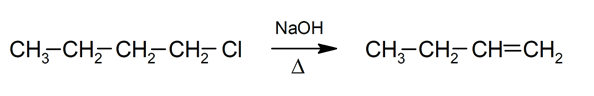
-
أكسدة
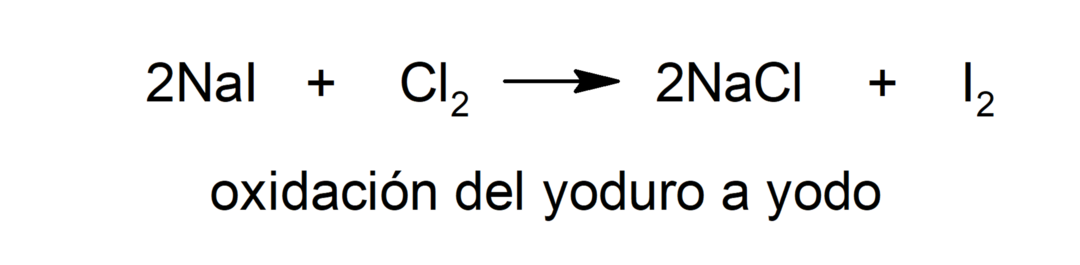
-
تخفيض
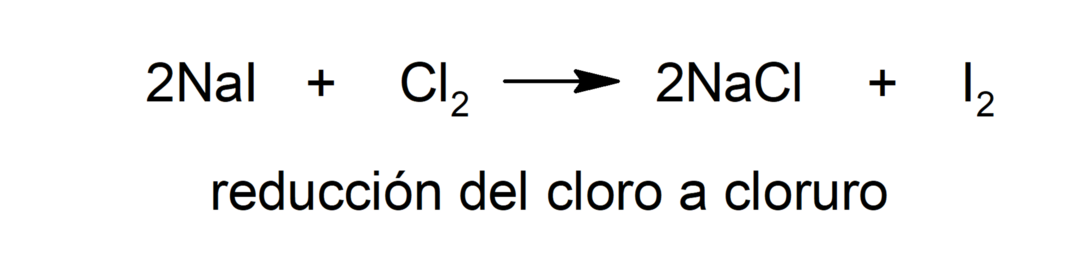
-
التفاعلات الحمضية القاعدية
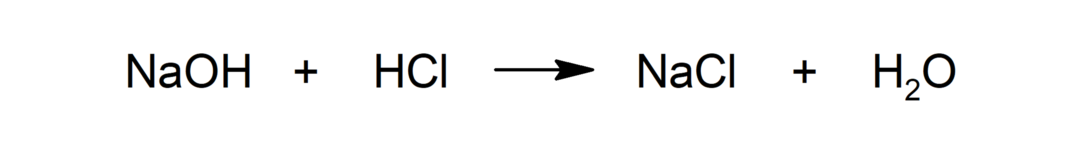
-
أكسجين
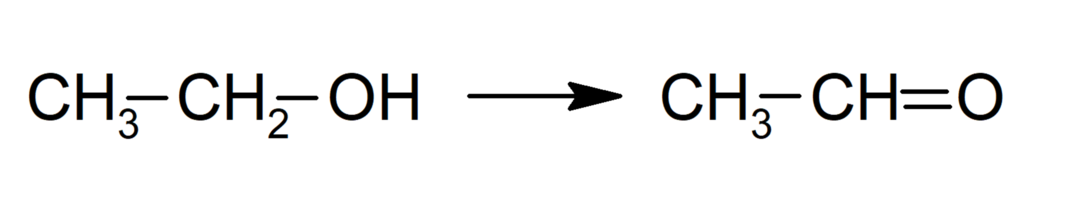
-
النقل

-
الكلورة
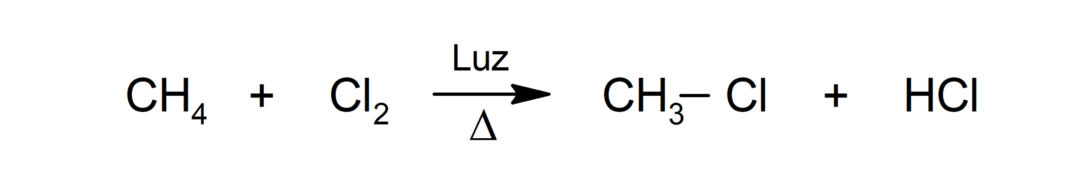
-
الكاربونيل

-
النتروجين. إنه تفاعل حيث ترتبط مجموعة نيتروزيل ببروتين ، بعد أن يتم تصنيعها بواسطة الريبوسومات.

-
بيروكسيد
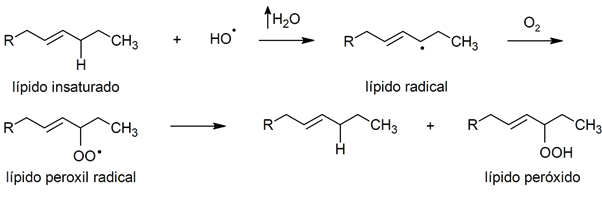
-
التحلل الضوئي للماء
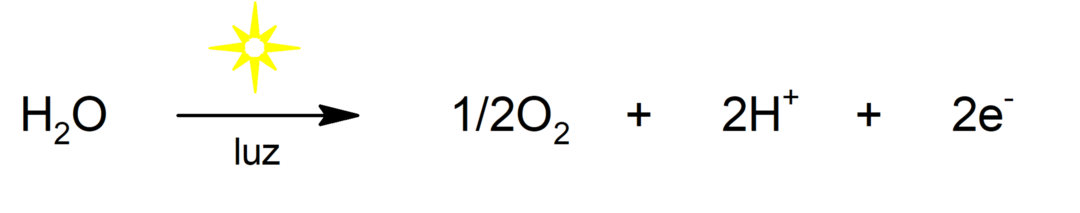
-
الكبريت
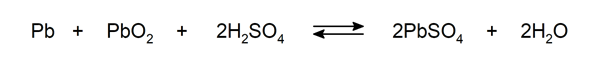
-
الكربنة
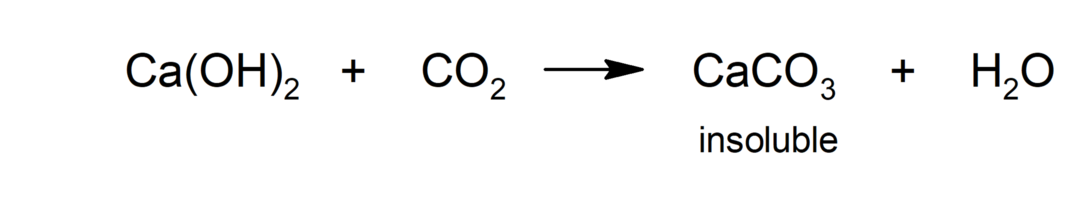
- الأوزون. إنه تفاعل بديل للمعالجة بالكلور لتطهير المياه.
-
الأسترة
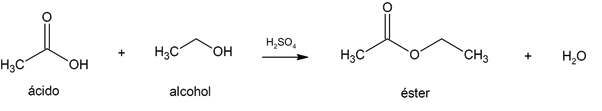
-
هدرجة الألكينات
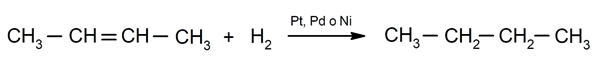
-
أستلة