20 أمثلة على الروابط التساهمية
منوعات / / July 04, 2021
الكثير من مركبات كيميائية تتكون من الجزيئات والتي بدورها تتكون من ذرات. لتكوين الجزيئات ، تتحد الذرات معًا عن طريق التكوين روابط كيميائية.
الروابط الكيميائية ليست كلها متشابهة: فهي تعتمد أساسًا على الخصائص الإلكترونية للذرات المعنية ، وقيمها الكهربية ، من بين عوامل أخرى. أكثر أنواع الروابط شيوعًا هي: الرابطة الأيونية و ال روابط تساهمية.
تتشكل الروابط التساهمية بين الذرات غير المعدنية من نفس الذرات عنصر كيميائي، بين الذرات غير المعدنية لعناصر مختلفة مع فرق كهرسلبية أقل من أو يساوي 1.7 وبين أ اللافلزية والهيدروجين. على سبيل المثال: ثنائي الكلور والأكسجين الجزيئي والماء.
تتشكل الرابطة التساهمية عندما تشترك اثنتان من هذه الذرات في إلكترونات آخر مستوى للطاقة لديهما لتحقيق القاعدة الثماني، والذي يثبت أن أيونات العناصر الكيميائية المختلفة الموجودة في الجدول الدوري تميل إلى إكمال مستويات طاقتها الأخيرة بـ 8 إلكترونات ، بحيث يمكن للجزيئات أن تكتسب استقرارًا مشابهًا لاستقرار غازات نبيلة.
لذلك ، فإن الطريقة التي تحقق بها هذه المواد أو المركبات الكيميائية الاستقرار هي من خلال مشاركة زوج من الإلكترونات (واحد من كل ذرة). بهذه الطريقة ، يكون زوج الإلكترونات المشترك شائعًا بين الذرتين وفي نفس الوقت يربطهما معًا.
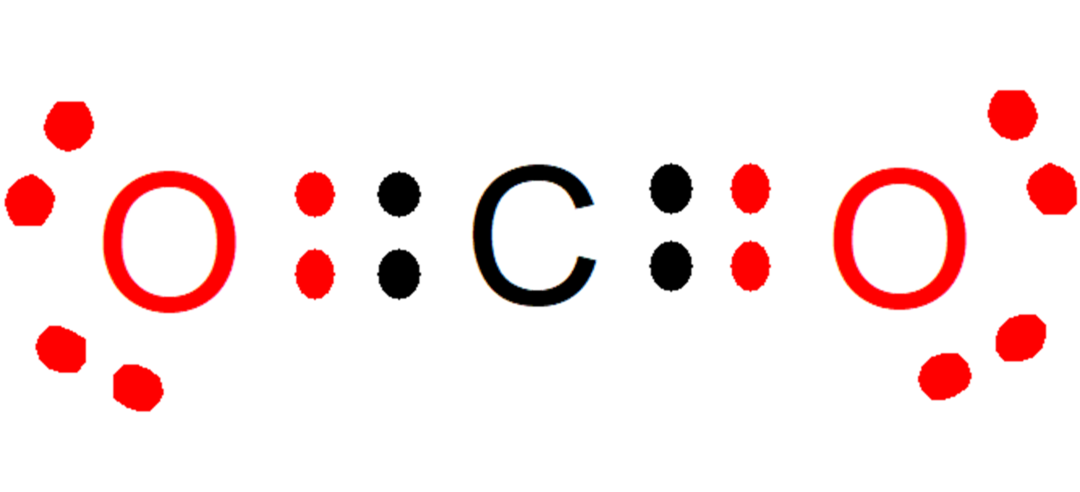
على سبيل المثال ، في ثاني أكسيد الكربون (CO2)يساهم كل أكسجين بإلكترونين (لون أحمر) في الرابطة مع الكربون ، بينما يساهم الكربون بإلكترونين (لون أسود) لكل رابطة مع كل أكسجين. في المركب المتكون ، تبقى 8 إلكترونات على كل ذرة ، وبالتالي تتحقق قاعدة الثمانية.
أنواع الروابط
هناك في الأساس ثلاثة أنواع من الروابط التساهمية، على الرغم من أنه من المهم توضيح أنه لا توجد رابطة تساهمية مطلقًا أو أيونية تمامًا. تحتوي جميع الروابط على نسبة معينة من الرابطة التساهمية والأيونية ، في الواقع ، يُنظر أحيانًا إلى الترابط الأيوني على أنه "مبالغة" في الرابطة التساهمية. بهذا المعنى ، قد تحدث الأنواع التالية من الرابطة التساهمية:
مواد تتكون من جزيئات تساهمية
ال مواد التي تحتوي على الجزيئات التساهمية يمكن أن يحدث في أي حالة من المواد (صلبة أو سائلة أو غازية) وبشكل عام ، هم من الموصلات الضعيفة الحار و كهرباء.
هناك مواد تساهمية جزيئية ومواد تساهمية شبكية. ال التساهمات الجزيئية لديهم نقاط غليان وانصهار منخفضة ، قابلة للذوبان في المذيبات غير القطبية (مثل البنزين أو رابع كلوريد الكربون) ، وتكون لينة في الحالة الصلبة. ال تساهمية شعرية إنها تشكل شبكات بلورية ، وبالتالي فهي تتمتع بنقاط انصهار وغليان أعلى وهي مواد صلبة صلبة غير قابلة للذوبان.
أمثلة على الروابط التساهمية
يمكن إعطاء أمثلة عديدة للمركبات أو المواد التي تحتوي على روابط تساهمية:
- ديفلورين
- ديبرومو
- ديكلور
- ديودو
- الأكسجين الجزيئي
- ماء
- الأمونيا
- نشبع
- الميثان
- البروبان
- الجلوكوز
- النيتروجين الجزيئي
- كوارتز
- البارافين
- ديزل

اتبع مع:
