20 أمثلة للألكانات
منوعات / / July 04, 2021
ال الألكانات هم نوع من الهيدروكربونات حيث يتم ربط عدد متغير من ذرات الكربون ببعضها البعض بواسطة روابط مفردة ، مثل الهيكل العظمي ، و يتم ربط كل ذرة كربون بدورها بذرات الهيدروجين ، والتي قد يتم استبدالها في النهاية بأخرى ذرات أو المجموعات الوظيفية. على سبيل المثال: الكلوروفورم والميثان والأوكتان.
ال الصيغة الجزيئية من سلسلة الألكانات الخطية المفتوحة هو CnH2n + 2، حيث يمثل C الكربون ، ويمثل H الهيدروجين ويمثل n عدد ذرات الكربون. الألكانات عبارة عن هيدروكربونات مشبعة ، مما يعني أنها لا تحتوي على روابط مزدوجة أو ثلاثية. لتسميتهم ، يمكنك استخدام لاحقة "-Ano" بعد تسمية سلسلة الكربون باستخدام اختصار يتوافق مع عدد ذرات الكربون (et- (2) ، pro- (3) ، ولكن- (4) ، القلم- (5) ، hex- (6) ، hep- (7) ، إلخ).
يمكن أن تخدمك:
تصنيف الألكانات
عادة ما يتم التعرف عليها داخل الألكانات مجموعتين كبيرتين: سلسلة مفتوحة (تسمى أيضًا غير دورية) وسلسلة مغلقة (أو دورية).
عندما مركبات السلسلة المفتوحة لا يقدمون أي استبدال للهيدروجين الذي يصاحب كل ذرة كربون ، ويطلق عليهم اسم الألكانات الخطية: هذه هي أبسط الألكانات. عندما يقدمون استبدال أي من الهيدروجين الخاص بهم بسلسلة كربون واحدة أو أكثر ، يطلق عليهم الألكانات المتفرعة. البدائل الأكثر شيوعًا هي مجموعات الإيثيل (CH
3CH2-) والميثيل (CH3-).من جانبهم ، هناك مركبات ذات دورة واحدة في الجزيء (أحادي الحلقة) وأخرى لها عدة (متعددة الحلقات). ال الألكانات الحلقية يمكن أن تكون حلقية متجانسة (تتشكل بالتدخل الحصري لذرات الكربون) أو حلقية غير متجانسة (تشارك فيها ذرات أخرى ، على سبيل المثال ، الأكسجين أو الكبريت).
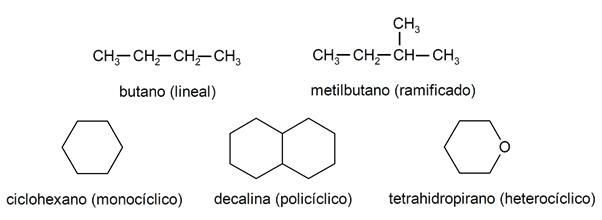
الخصائص الفيزيائية للألكانات
على العموم، الخصائص الفيزيائية يتم تكييف الألكانات بالكتلة الجزيئية (ترتبط بدورها بطول سلسلة الكربون). أولئك الذين لديهم أقل عدد من الكربون هم الغازي ل درجة الحرارة البيئة ، تلك التي تتراوح من 5 إلى 18 ذرة كربون السوائل، وفوق هذا الرقم صلب (على غرار الشمع).
كونها أقل كثافة من الماء ، فإنها تميل إلى الطفو عليها. بشكل عام ، الألكانات غير قابلة للذوبان في الماء وقابلة للذوبان في المذيبات العضوية.
الهدف من الغليان وبناءا على انصهار من الألكانات تعتمد على الكتلة الجزيئية، وهذا يعني ، على طول سلسلة الكربون ، على الرغم من أنها تعتمد أيضًا عدة مرات على الترتيب المكاني للذرات. الألكانات الخطية والدائرية لها نقاط غليان أعلى من تلك المتفرعة.
الخواص الكيميائية للألكانات
تتميز الألكانات بكونها مركبات كيميائية جدا تفاعل ضعيف، ولهذا السبب تُعرف أيضًا باسم "البارافين" (باللاتينية ، parum affinis تعني "تقارب منخفض"). إنها مركبات لها طاقة تنشيط عالية جدًا عندما تشارك فيها تفاعلات كيميائية. أهم تفاعل يمكن أن تتعرض له الألكانات هو الإحتراق توليد ، في وجود الأكسجين والحرارة وثاني أكسيد الكربون والماء.
الألكانات هي الأساس لمجموعة متنوعة مهمة من التفاعلات المرتبطة العمليات الصناعية مهم جدًا ، لكونه أكثر أنواع الوقود التقليدية. تظهر أيضًا كمنتجات نهائية لعمليات بيولوجية مثل التخمير الميثاني المنشأ الذي يقوم به البعض الكائنات الدقيقة.
أمثلة على الألكانات
بعض الأمثلة على الألكانات (بما في ذلك بعض الألكانات الخطية والمتفرعة المعروفة) هي:
- كلوروفورم (اسم يتوهم ثلاثي كلورو ميثان; CHCl3). تستخدم أبخرة هذه المادة في التخدير. تم إيقافه لهذا الغرض لأنه وجد ضررًا الأعضاء مهم ، مثل الكبد أو الكلى. يتم استخدامه اليوم في المقام الأول كمذيب أو مبرد.
- الميثان (CH4). إنه أبسط ألكان على الإطلاق: يتكون من ذرة كربون واحدة فقط وأربع ذرات هيدروجين. إنه غاز يحدث بشكل طبيعي عن طريق تحلل الركائز العضوية المختلفة وهو المكون الرئيسي للغاز الطبيعي. في الآونة الأخيرة ، تم التعرف عليه كواحد من الغازات الأكثر مساهمة في ما يسمى بتأثير الاحتباس الحراري.
- أوكتان (ج8ح18). إنه ألكان ثماني الكربون وله أهمية كبيرة لأنه يحدد الجودة النهائية للنافثا ، وهي عبارة عن مزج من الهيدروكربونات المختلفة. تُقاس هذه الجودة برقم الأوكتان أو الأوكتان للوقود ، والذي يتخذ كمرجع مرجعي منخفض التفجير (المؤشر 100) ورقم شديد الانفجار (المؤشر 0).
- الهكسان (ج6ح14). وهو مذيب مهم ويجب تجنب استنشاقه لأنه شديد السمية.
- البيوتان (ج4ح10). جنبا إلى جنب مع البروبان (سي3ح8) ، تشكل ما يسمى بالغازات البترولية المسالة (LPG) ، والتي تتكون في أكياس الغاز أثناء عملية استخراج النفط. حاليًا ، يتم الترويج لاستبدال البنزين أو الديزل بغاز البترول المسال كوقود منذ ذلك الحين من الهيدروكربون الصديق للبيئة (لا ينبعث منه إلا ثاني أكسيد الكربون والماء أثناء احتراقه).
- إيكوسانو (ج20ح42). إنه الألكان ذو العشرين كربونًا (البادئة "ico" تعني عشرين)
- سيكلوبروبان (ج3ح6). سابقا كان يستخدم كمخدر
- ن هيبتان (ج7ح16). هو الذي يؤخذ كمرجع لنقطة الصفر في مقياس أوكتان البنزين ، والذي سيكون أقل رغبة ، لأنه يحترق بشكل متفجر. يتم الحصول عليها من راتنج معين النباتات.
- 3-إيثيل -2 ، 3-ثنائي ميثيل بنتان (ج9ح20)
- 2-ميثيل بوتان (ج5ح12)
- 3-كلورو-4-ن-بروبيل هبتان (ج10ح21Cl)
- 3،4،6-تريميثيل هبتان (ج10ح22)
- 1-برومو-2- فينيلان (ج8ح9Br)
- 3-إيثيل -4-ميثيلهكسان (ج9ح18)
- 5-إيزوبروبيل -3 ميثيلنونان (ج13ح28)
- الكوبي (ج8ح8)
- 1-بروموبروبان (ج3ح7Br)
- 3-ميثيل-5-ن-بروبيلوكتان (ج12ح26)
- 5-ن-بوتيل-4،7-ديثيلديكان (ج18ح28)
- 3،3-ديميثيلديكان (ج12ح26)