المفهوم في التعريف ABC
منوعات / / April 22, 2022
تعريف المفهوم
Azeotropes عبارة عن خليط من المركبات الكيميائية ، بتركيبة محددة ، تغلي عند درجات حرارة معينة. السمة الأساسية هي أن المخلوط يتصرف كما لو كان مادة نقية واحدة يحافظ على خصائصه ويسهل التعامل معه.

مهندس كيميائي
يمكن إعطاء الخليط من مكونين أو أكثر ومكوناته تعبير إنه نفسه في كل من المرحلة السائلة وفي الطور الغازي ، وهذا يولد أوجه تشابه مع المواد النقية. من هذا ، يُستنتج بسهولة أن هذا المزيج لا يمكن فصله إلى مكوناته من خلال عمليات مثل التقطير التجزيئي لأنه ، كما ذكر أعلاه ، سيحتفظ بنسبه ، ويتصرف كما لو كان منفردًا عنصر.
خاصية أخرى هي أن درجة غليان هذا الخليط يمكن أن تكون أعلى أو أقل أو حتى مساوية لتلك الخاصة بأحد مكوناته. عندما يغلي الأزيوتروب عند أ درجة الحرارة من الحد الأقصى للغليان ، يُعرف باسم الحد الأقصى من الأزيوتروب وعندما يحدث ذلك عند أدنى درجة حرارة ممكنة يُعرف باسم الحد الأدنى من الأزيوتروب. هذا يعني أن الحد الأدنى من الأزيوتروب لديه نقطة غليان أقل من مكوناته النقية والعكس صحيح مع الحد الأقصى من الأزيوتروب. على سبيل المثال ، في خليط الميثانول - البنزين ، يكون الأزيوتروب بحد أدنى (0.61 بنزين - 0.39 ميثانول في الكسور المولي) التي تبلغ درجة غليانها 58 درجة مئوية ، في خزان حيث تبلغ درجة غليان البنزين 80 درجة مئوية ونقطة غليان الميثانول 65 درجة مئوية
الحد الأدنى والأقصى للزيوتروبس
الآن... من أين يأتي الأزيوتروب؟ عندما يكون هناك انحراف عن قانون راولت ، أي أن ضغط بخار الخليط الأزيوتروبي لا يرتبط ارتباطًا مباشرًا بالجزء المولي ، إنه عندما ينشأ مفهوم المزيج الأزيوتروبي. تحدث هذه الانحرافات عندما تجذب المكونات أو تتنافر بشكل كبير ، أي أن القوى بين الجزيئات مختلفة جدًا في المركبات المختلفة.
عندما يكون الانحراف موجبًا ، يكون لدينا الحد الأدنى من الأزيوتروب ، بينما إذا كان الانحراف سالبًا ، يكون لدينا الحد الأقصى من الأزيوتروب. لفهم هذا المفهوم بشكل أفضل ، دعنا نلقي نظرة على بعض الرسومات:
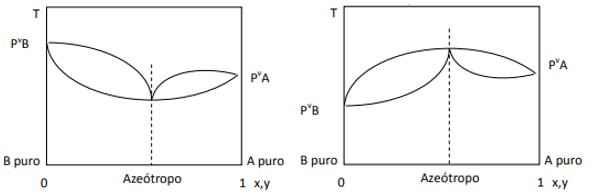
هنا نلاحظ أنه إذا كان الخليط مثاليًا ، وفقًا لقانون راولت ، يجب ربط ضغط بخار المكونات النقية بخط مستقيم ، حيث حسنًا ، هناك انحراف عن هذا القانون يتسبب في تكوين الحد الأدنى والحد الأقصى من الأزيوتروبس ، اعتمادًا على ما إذا كان هناك تقارب أكبر أو أقل بين عناصر. عندما يكون الانحراف عن قانون راولت سالبًا ، كما في الشكل على اليسار ، يكون الحد الأدنى عند رسم بياني من الضغط ، ولكن الحد الأقصى في مخطط درجة الحرارة (وبالتالي ، أزيوتروب من الحد الأقصى). من ناحية أخرى ، إذا كان الانحراف موجبًا لقانون راولت ، فسيكون الحد الأقصى في الضغط مقابل. التكوين ، ولكن الحد الأدنى في الرسم البياني لدرجة الحرارة مقابل. التكوين (هنا لدينا حد أدنى من الأزيوتروب). لا تخلط بين المخططات والضغط. التركيب ودرجة الحرارة مقابل. تعبير.
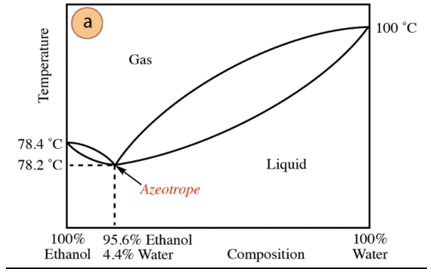
في حالة خليط الإيثانول والماء ، يوجد حد أدنى من الأزيوتروب يتكون من 95.6٪ إيثانول و 4.4٪ ماء. درجة حرارة غليان الخليط الأزيوتروبي أقل بـ 78.2 درجة مئوية من درجة حرارة المكونات النقية. لذلك ، افترض تقطير خليط الماء والإيثانول مع نسبة عالية من الماء (ما يقرب من 100٪). لن يكون من الممكن الحصول على كحول نقي ، حيث سيتم الحصول على أجزاء أكبر في كل مرحلة من مراحل التقطير. من الإيثانول ، ولكنه لا يصل أبدًا إلى 100٪ ، فإنه سيقترب تدريجيًا من تكوين الخليط الأزيوتروبي (أدنى نقطة تحت). لهذا السبب ، مثل الماء ، يميل إلى تكوين الحد الأدنى من الأزيوتروبس مركبات العضوية (بالنظر إلى نوع القوى بين الجزيئات التي تتفاعل) ، يلزم مسبقًا إزالة الماء من الخليط للحصول على المركب النقي. أو بمجرد الحصول على الأزيوتروب ، طرق اِستِخلاص من الماء الإضافي.
بناءً على ما سبق ، ليس من قبيل الصدفة العثور على الكحول (في السوبر ماركت و مقابل) بنسبة 95٪ ، أرخص منتج يمكن الحصول عليه. للحصول على الكحول النقي ، من الضروري "كسر" الأزيوتروب تقنية إضافية ، مثل استخدام عوامل التجفيف أو التقطير الأزيوتروبي. يتكون التقطير الأيزوتروبي من إضافة مكون إضافي إلى الخليط الذي يعمل عن طريق السحب وبواسطة تفاعل مع أي من مكونات الخليط (تقارب أعلى) يمكن إزالتها من الخليط.
موضوعات في Azeotropes


