20 أمثلة على الأمينات
أمثلة / / November 06, 2023
ال الأمينات نكون المركبات الكيميائية العضوية مشتقات الأمونيا (NH3)، حيث تم استبدال واحدة على الأقل من هيدروجين الأمونيا بمجموعة ألكيل أو أريل، مما أدى إلى تكوين مجموعة أمينية (-NH2، -NH-، -N =). على سبيل المثال:ميثيل أمين وإيثيل أمين وبروبيلامين.

مجموعة الألكيل عبارة عن بديل يتشكل عند إزالة الهيدروجين من هيدروكربون مشبع. وبهذه الطريقة، يمكن للكربون الذي تم فصل الهيدروجين منه أن يرتبط بآخر ذرة. على سبيل المثال: الميثيل (CH3 -) والإيثيل (CH3 - الفصل2 -).
مجموعة الأريل هي بديل مشتق من حلقة عطرية، مثل البنزين. على سبيل المثال: فينيل (C6ح5 -)
- أنظر أيضا: أميدات
أنواع الأمينات
يمكن تصنيف الأمينات وفقا لعدد ذرات الهيدروجين المرتبطة بالنيتروجين والتي تم استبدالها بمجموعات وظيفية ألكيل أو أريل.
ووفقا لهذا المعيار هناك:
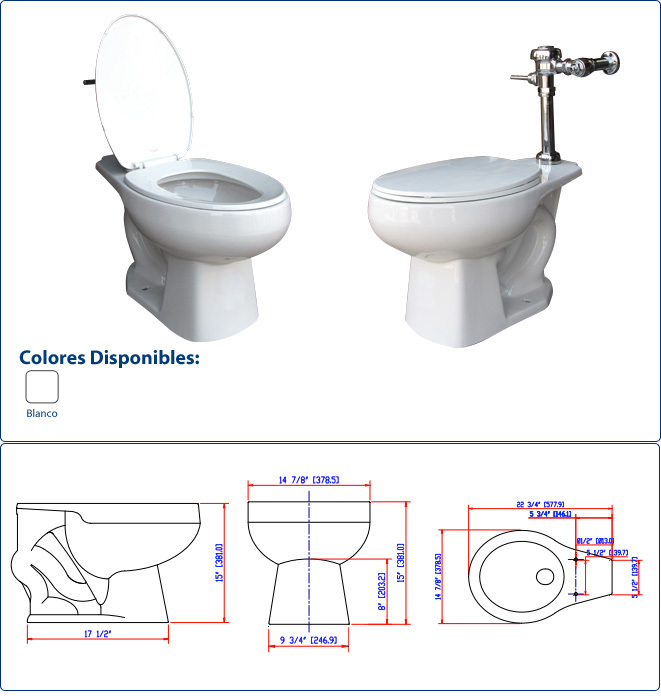
- الأمينات الأولية. تتشكل عندما يتم استبدال ذرة هيدروجين واحدة فقط من الأمونيا بمجموعة ألكيل أو أريل. على سبيل المثال: إيثيل أمين و1-بنتيل أمين.
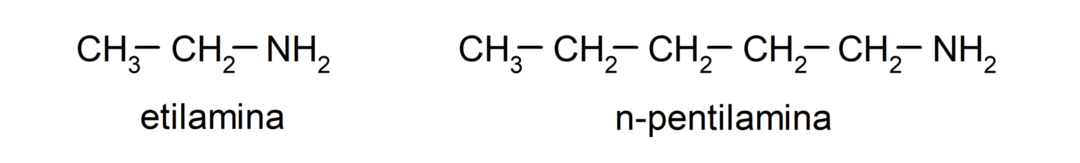
- الأمينات الثانوية. تتشكل عندما يتم استبدال ذرتين من ذرات هيدروجين الأمونيا بمجموعة ألكيل أو أريل. على سبيل المثال: ثنائي إيثيل أمين وإيثيل ميثيل أمين.
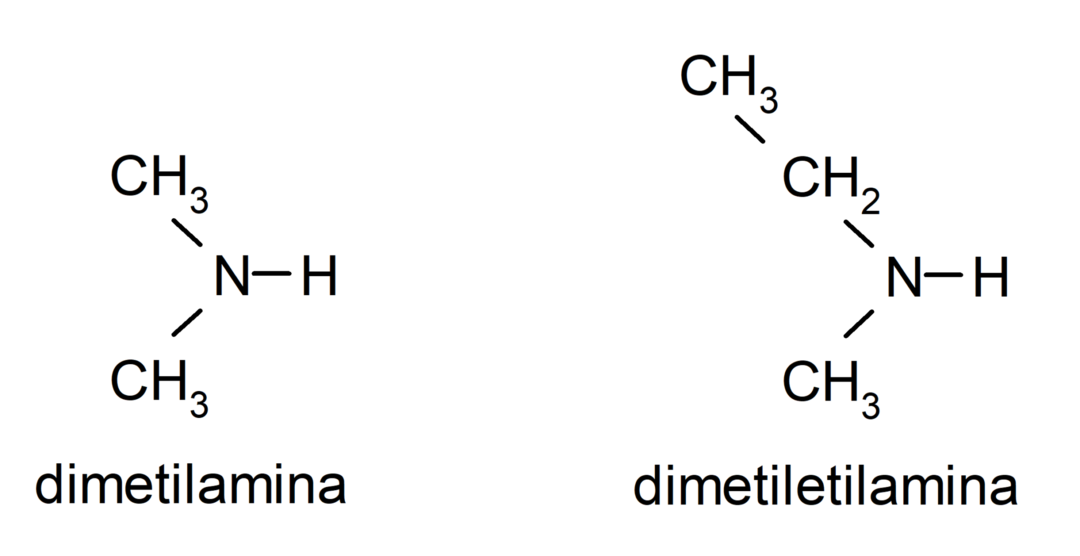
- الأمينات الثلاثية. تتشكل عندما يتم استبدال ذرات الهيدروجين الثلاث للأمونيا بمجموعة ألكيل أو أريل. على سبيل المثال: ثلاثي ميثيل أمين وثنائي ميثيل إيثيل أمين.
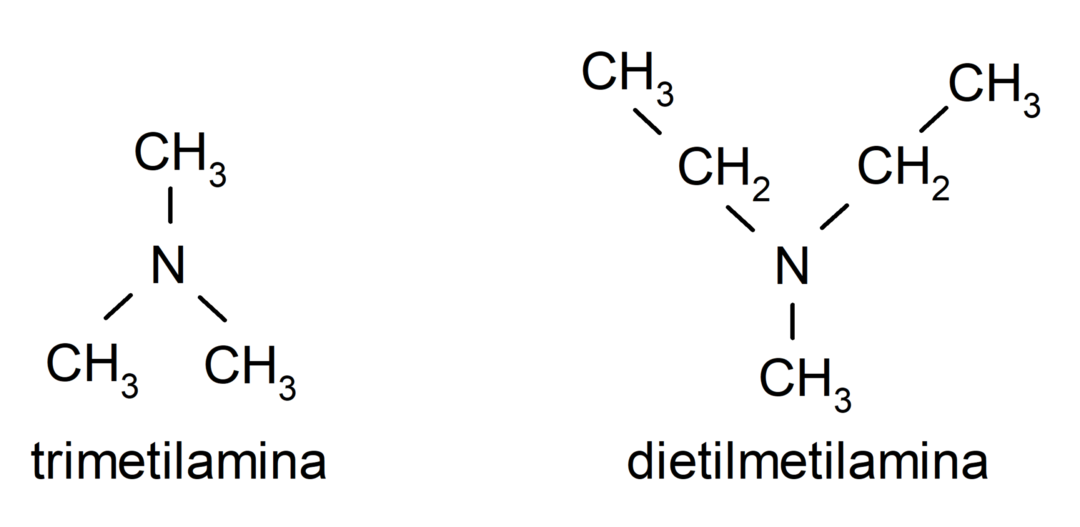
يتم تصنيف الأمينات أيضًا بناءً على نوع المجموعة المرتبطة بالنيتروجين. ووفقا لهذا المعيار هناك:
- الأمينات الأليفاتية. لديهم بدائل الألكيل. على سبيل المثال: بوتيل أمين وثنائي إيثيل أمين.

- الأمينات العطرية. لديهم بدائل أريل. على سبيل المثال: فينيل أمين (أنيلين) وثنائي فينيل أمين.
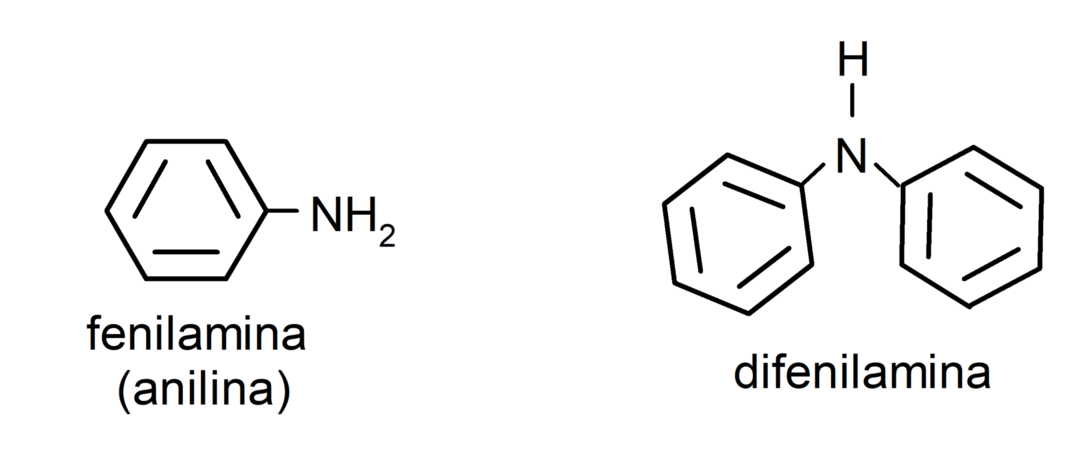
تسميات الأمينات
وفقًا للاتحاد الدولي للكيمياء البحتة والتطبيقية (IUPAC)، تتم تسمية الأمينات وفقًا للقواعد التالية:
بالنسبة لأبسط الأمينات، يتم تسمية كل من بدائل مجموعات الهيدروجين المرتبطة بنيتروجين الأمونيا. ثم توضع كلمة "أمين" في نهاية الاسم.
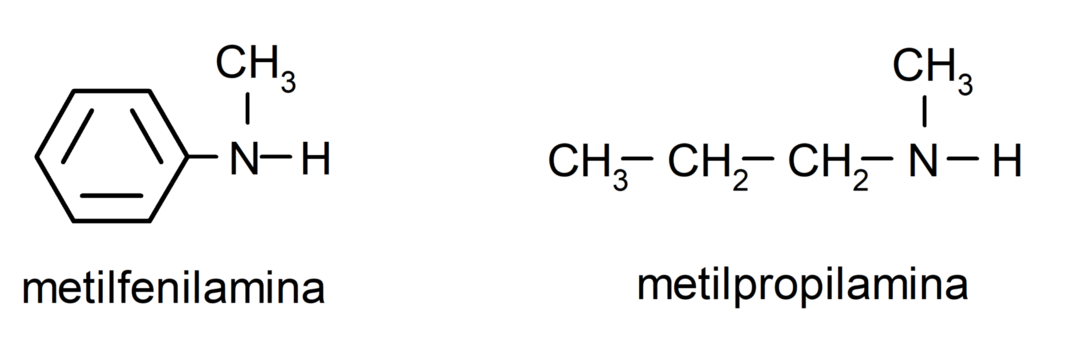
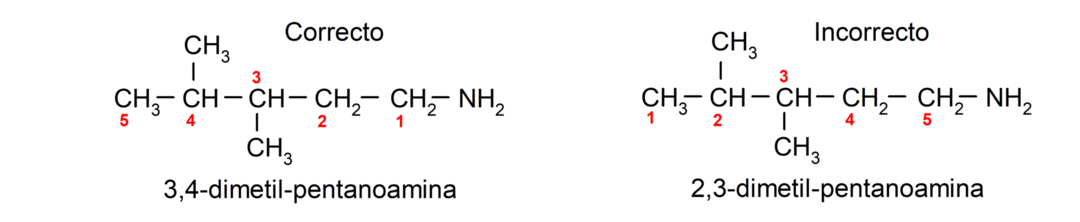
بالنسبة للأمينات التي تحتوي على عدة سلاسل كربون (والتي بدورها لها بدائل أخرى)، يتم اختيار سلسلة الكربون التي تحتوي على المجموعة الأمينية لتكون السلسلة الرئيسية. علاوة على ذلك، يتم اختيار موضع المجموعة الأمينية بحيث تحتل أصغر موضع في السلسلة الكربونية، وفيها وبناءً على هذا الموضع، يتم أيضًا اختيار البدائل بحيث يشغلون أصغر موضع ممكن في سلسلة.
وأخيراً يتم تسميتها باستخدام اسم الألكان أو الألكين أو الألكاين المقابل للسلسلة الرئيسية، ويتم وضع لاحقة الأمين.
إذا كانت سلسلة الكربون تحتوي على عدة مجموعات أمينية، يتم اختيارها في الموضع الذي تشغله في أصغر مجموعة من ترقيم مواقعها. بالإضافة إلى ذلك، يتم وضع اسم الألكان أو الألكين أو الألكاين المقابل، متبوعًا بالمصطلح الذي يشير إلى عدد المجموعات الأمينية، متبوعًا باللاحقة "أمين".

الخصائص الفيزيائية للأمينات
تعتمد الخصائص الفيزيائية للأمينات إلى حد كبير على عدد ذرات الهيدروجين المرتبطة بالنيتروجين التي تم استبدالها، ونوع البدائل التي تم استبدالها.
- الذوبان. بشكل عام، الأمينات أكثر قابلية للذوبان في الماء من الهيدروكربونات المشبعة المقابلة. علاوة على ذلك، فإن الأمينات ذات سلاسل الكربون الطويلة تكون أقل قابلية للذوبان في الماء من الأمينات ذات سلاسل الكربون القصيرة. من ناحية أخرى، الأمينات العطرية غير قابلة للذوبان في الماء.
- نقطة الغليان. درجة غليان الأمينات أعلى من درجة غليان الألكانات التي لها نفس عدد ذرات الكربون.
- يشم. معظم الأمينات لها روائح كريهة. على سبيل المثال، رائحة بوتريسين تشبه رائحة اللحوم المتعفنة ورائحة ثلاثي ميثيل أمين تشبه رائحة الأسماك المتعفنة.
الخواص الكيميائية للأمينات
بعض الخواص الكيميائية للأمينات هي:
- وهي مركبات كيميائية أساسية، أي أنها تخضع لتفاعلات حيث تستقبل البروتونات وفقًا لنظرية برونستد-لوري. على سبيل المثال:
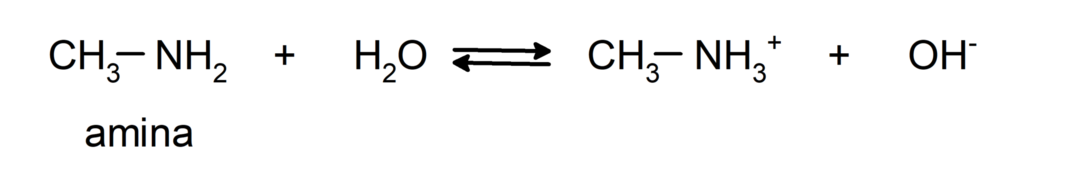
- أنها تقدم ردود فعل تحييد مع الأحماض التي تتكون فيها الأملاح الأمينية. على سبيل المثال:

أمثلة على الأمينات
- ميثيلامين
- إيثيلامين
- بروبيلامين
- ثنائي ميثيل أمين
- إيثيل ميثيل أمين
- فينيل أمين (أنيلين)
- ثنائي فينيلامين
- ميثيل بروبيلامين
- البيوتان -1،4 ديامين
- سبيرمين
- كادافيرين
- 3,5-ديميثيلانيلين
- ميثيلانيلين
- الأمفيتامين
- بيبيرازين


الوظيفة البيولوجية للأمينات
الأمينات موجودة في كثير كائنات حية وأداء وظائف مختلفة. بعض الأمينات، مثل الإبينفرين والنورإبينفرين والسيروتونين والدوبامين، هي ناقلات عصبية.
المجموعة الأمينية هي إحدى المجموعات الوظيفية التي تشكل الأحماض الأمينية، وهي الوحدات الأساسية لها البروتينات. بالإضافة إلى ذلك، تحتوي القواعد النيتروجينية التي تشكل الحمض النووي الريبي (DNA) والحمض النووي الريبي (RNA) على مجموعات أمينية.
استخدامات الأمينات
بعض استخدامات الأمينات هي:
- يتم استخدامها لإنتاج المركبات الكيماوية الزراعية والصيدلانية.
- يتم استخدامها كمحفزات في إنتاج البولي يوريثان.
- نظرا لتأثيرها التخميد، فهي تستخدم لمنع التآكل في البيئات المائية.
- يتم استخدامها لتنقية الغازات في محطات الطاقة ومصافي التكرير.
- يتم استخدامها لصنع منتجات التنظيف.
- يتم استخدامها لإنتاج منتجات العناية الشخصية، لأنها تعمل على تحسين الرغوة في الصابون والشامبو.
سمية الأمينات
استنشاق الأمينات بتركيزات عالية يسبب التسمم، والذي بدوره يؤدي إلى ارتفاع ضغط الدم والنوبات. وعلاوة على ذلك، الاتصال مع الأمينات الأليفاتية في الحالة الغازية يسبب تهيج العين والجهاز التنفسي. تسبب العديد من الأمينات حروقًا جلدية عند ملامستها.
الأمينات العطرية شديدة السمية، ولكن نظرًا لأنها أقل تطايرًا بكثير من الأمينات الأليفاتية، فيمكن التحكم في الاتصال بها بشكل أفضل.
مراجع
- بيريز، ج. ر. سي.، وخيمينيز-كولمينيرو، إف. (2010). الأمينات الحيوية: الأهمية السمية. الإلكترون. ج. بيوميد.، 3، 58-60.
- فرنانديز غارسيا، م.، وألفاريز غونزاليس، م. Á. (2005). الأمينات الحيوية في الأطعمة.
اتبع مع:
- الكحوليات
- الألدهيدات
- الكحول الإيثيلي
- الكيمياء العضوية