أمثلة على التفاعلات الماصة للحرارة
أمثلة / / November 09, 2023
أ تفاعل إمتصاص الحرارة وهو تفاعل يمتص الطاقة من الوسط على شكل حرارة. في هذه التفاعلات، لكي تتحول المواد المتفاعلة إلى منتجات، من الضروري أن تمتص الحرارة، مما يجعل المنتجات تمتلك طاقة أكبر من المواد المتفاعلة التي أدت إلى نشوئها. بعض الأمثلة على التفاعلات الماصة للحرارة هي: التمثيل الضوئي والتحليل الكهربائي للمياه.
- أنظر أيضا: التفاعلات الكيميائية
أمثلة على التفاعلات الماصة للحرارة في الحياة اليومية
بعض التفاعلات الماصة للحرارة الرئيسية هي:
إنتاج الأوزون في الغلاف الجوي. يتم إنتاج الأوزون في الغلاف الجوي عندما يكون الأكسجين الجزيئي (O2) يمتص الأشعة فوق البنفسجية ويتحلل. ومن ثم يمكن لذرة الأكسجين (O) أن تتفاعل مع جزيء أكسجين آخر (O).2) وتشكل الأوزون (O3).

التحليل الكهربائي للمياه. إنها العملية التي يتم من خلالها تطبيقه الطاقة الكهربائية إلى الماء لفصله إلى مكونيه، الهيدروجين (H) والأكسجين (O).
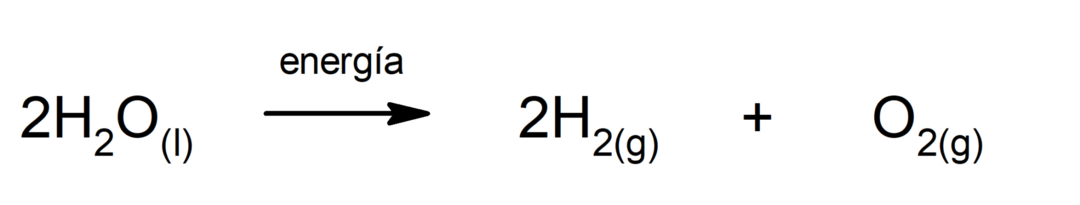
البناء الضوئي. إنه التفاعل الكيميائي الذي يتم من خلاله الامتصاص طاقة شمسية، ثاني أكسيد الكربون (CO2) يتحول إلى جلوكوز. يشكل هذا التفاعل الطريق الرئيسي لتغذية النباتات.
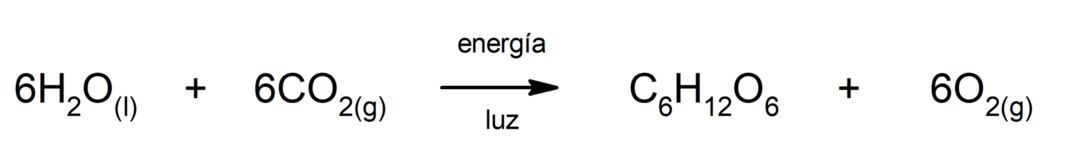
إنتاج كبريتيد الحديد (II).. ولكي يحدث التفاعل بين الكبريت والحديد، من الضروري توفير الطاقة على شكل حرارة.
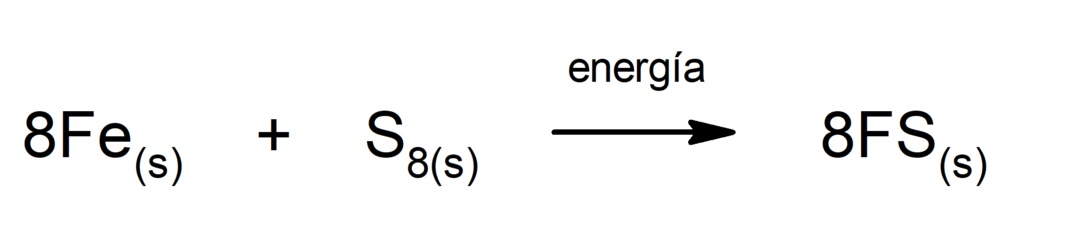
تحلل ثاني أكسيد الكربون (CO2). تحلل CO2 عند درجات الحرارة المرتفعة ينتج أول أكسيد الكربون (CO) والأكسجين (O2).
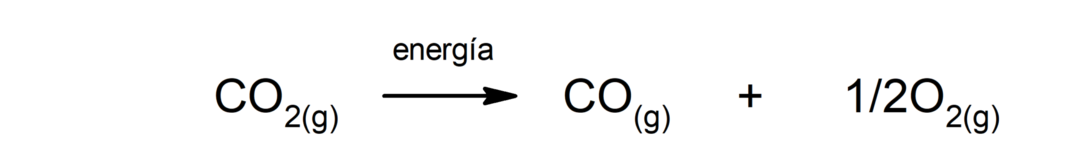
تحلل كربونات الكالسيوم (CaCO3). تتحلل كربونات الكالسيوم بامتصاص الحرارة لتنتج أكسيد الكالسيوم (CaO) وثاني أكسيد الكربون (CO2).
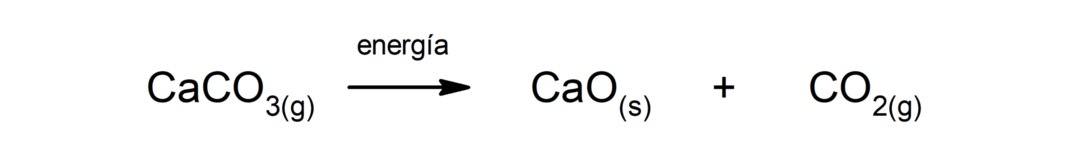
الفرق بين التفاعل الماص للحرارة والطاردة للحرارة
الفرق الرئيسي بين التفاعلات الماصة للحرارة والطاردة للحرارة هو أن التفاعلات الماصة للحرارة تمتص الحرارة، بينما تطلق التفاعلات الطاردة للحرارة الحرارة.
علاوة على ذلك، تتميز التفاعلات الماصة للحرارة بزيادة في المحتوى الحراري، في حين ترتبط التفاعلات الطاردة للحرارة بانخفاض في المحتوى الحراري.
المحتوى الحراري هو كمية ديناميكية حرارية تحدد تدفق الطاقة الحرارية عند ضغط ثابت أثناء التفاعل الكيميائي. ويرمز له بالحرف H، ويعد تنوعه أحد المؤشرات الرئيسية لتحديد ما إذا كان التفاعل الكيميائي ماصًا للحرارة أم طاردًا للحرارة.
- إذا كان التفاعل الكيميائي يحتوي على تغير في المحتوى الحراري أكبر من الصفر (Δح> 0) ماص للحرارة.
- إذا كان التفاعل الكيميائي يحتوي على تغير في المحتوى الحراري أقل من الصفر (ΔH <0) طاردة للحرارة.
اتبع مع:
- الظواهر الفيزيائية والكيميائية
- الكيمياء في الحياة اليومية
- الكيمياء في الحياة اليومية
- الكيمياء العضوية وغير العضوية
مراجع
- سوتو قرطبة، س. (2016). ردود الفعل الماصة للحرارة. مستودع التكنولوجيا المعهد التكنولوجي في كوستاريكا.
- كوروميناس، ج. (2017). التفاعلات الكيميائية للحياة اليومية. الإمبيق، (90)، 8-26.
- سانشيز، M. ت. م.، وسانشيز، م. م. (2002). دراسة تجريبية للتفاعلات الماصة للحرارة لطلاب ESO. حوليات الكيمياء في RSEQ, (4), 36-39.



