مثال على تسمية المركبات العضوية
كيمياء / / July 04, 2021
المركبات العضوية هي جزيئات من خصائصها أنها تتكون من قاعدة من جزيئات الكربون و الهيدروجين ، المعروف أيضًا باسم الهيكل العظمي ، ومُدمج مع عناصر أخرى ، خاصة الأكسجين والنيتروجين والكبريت.
ال IUPAC (الاتحاد الدولي للكيمياء البحتة والتطبيقية ، الاتحاد الدولي للكيمياء البحتة والتطبيقية) وضع قواعد عامة لتصنيف وتسمية الجزيئات العضوية ، والتي نوضح أهمها.
الهيدروكربونات
الهيدروكربونات هي أبسط الجزيئات العضوية ، وتتكون من هيكل عظمي من الكربون وذرات الهيدروجين. هناك ثلاثة أنواع من الهيدروكربونات:
الألكانات
إنها أبسطها ، وتتكون من ذرات كربون مرتبطة بروابط تساهمية بسيطة مع ذرات الهيدروجين ، بالصيغة العامة H = 2n + 2 ، أي أن ذرات الهيدروجين هي ضعف عدد ذرات الهيدروجين. كربون زائد 2. تتكون تسمياتها من البادئات العددية met- لـ 1 ذرة كربون ، et- لـ 2 ، prop- لـ 3 ، و- لـ 4 ؛ من 5 ذرات كربون ، يتم استخدام البادئات الشائعة pent- ، hex- ، hept- ، oct- ، إلخ. يضاف إلى جميع الألكانات النهاية -ano.
مثال: CH4: الميثان ؛ ج2ح6: الإيثان ؛ ج4ح10: البيوتان؛ ج6ح14: الهكسان
الألكينات
يتم تشكيلها بواسطة هيكل عظمي من الكربون حيث يوجد رابطة مزدوجة بين ذرات الكربون. صيغته العامة هي H = 2n ، أي أن ذرات الهيدروجين هي ضعف عدد ذرات الكربون. مثل الألكانات ، يستخدمون البادئات التي تشير إلى عدد ذرات الكربون ، وفي هذه الحالة تتم إضافة النهاية -eno. بالإضافة إلى ذلك ، في الجزيئات التي تحتوي على أكثر من ثلاث ذرات كربون ، يكون الكربون حيث توجد الرابطة المزدوجة ، يبدأ في العد من الكربون الأقرب إليه هو.
أمثلة: ج2ح4: ethene؛ ج3ح6: البروبين؛ ج4ح8: بيوتين ، 2-بيوتين ؛ ج6ح12: Hexene ، 2-hexene (رابطة مزدوجة عند الذرة 2) ، 3-hexene (رابطة مزدوجة في الذرة 3).
ألكينز
تحتوي الألكينات على رابطة ثلاثية عند ذرات الكربون الخاصة بها. صيغته العامة هي H = 2n-2 ، مما يشير إلى أن الجزيء سيحتوي على ذرتين من الهيدروجين أقل من ضعف عدد ذرات الكربون. إلى البادئة التي تشير إلى عدد الكربون ، تتم إضافة النهاية -ino. كما في حالة الألكينات ، يذكر الكربون المحتوي على الرابطة الثلاثية ، محسوبًا من أقصى الأقرب إليه.
أمثلة: ج2ح2: ethyne؛ ج3ح4: تلميح؛ ج4ح6: بوتين ، 2-بوتين ؛ ج6ح12: Hexino ، 2-hexene (رابطة ثلاثية عند الذرة 2) ، 3-hexyne (رابطة ثلاثية عند الذرة 3).
المجموعات الوظيفية
المجموعات الوظيفية عبارة عن مجموعات من الذرات التي تعمل كأيون وتحل محل ذرة الهيدروجين في صيغة الألكان.
الراديكاليون
يسمى الألكان بدون ذرة الهيدروجين بالراديكالي ، وللتعرف عليه تتم إضافة النهاية -ilo:
أمثلة CH4: الميثان - CH3+ الميثيل؛ ج2ح6: إيثان - سي2ح5+ الإيثيل. ج4ح10: البيوتان - سي4ح9+ بوتيل. ج6ح14: الهكسان - سي6ح13+ هيكسيل.
مزيج من الهيدروكربونات
إحدى الحالات التي يمكن أن تحدث هي أنه يتم دمج اثنين أو أكثر من الهيدروكربونات في جزيء. تسمى الهيدروكربونات التي يتم دمجها معها بركب شجر. في هذه الحالات ، سيكون الهيدروكربون الأساسي هو الذي يحتوي على أطول سلسلة ، ورقم الكربون حيث تم العثور على الشجر ، متبوعًا باسم الجذر مع النهاية -il ، ثم اسم الهيدروكربون يتمركز. سيتم ذكر الرقم عدة مرات مثل الأشجار المرتبطة به. في حالة وجود نفس الجذر في ذرات كربون مختلفة ، سيتم ذكر الأرقام مفصولة بفواصل ، متبوعة بشرطة ، اسم الراديكالي ، ثم عدد الذرات التي يتصل بها الجذر الآخر ، إن وجد ، وشرطة ، واسم الجذر واسم الهيدروكربون يتمركز. في حالة وجود جذرين مرتبطين بذرة الكربون نفسها ، فسيتم ذكر الرقم مرتين. إذا كانوا متطرفين مختلفين ، فسيتم ذكره مرة واحدة قبل اسم كل راديكالي ؛ إذا تساوى الجذور ، فسيتم ذكر الرقم مرتين. سنبدأ بذكر أبسط أشكال التشجير أولاً (تلك التي تحتوي على أقل كمية من الكربون) ثم تلك التي تحتوي على أكبر كمية.
مثال: جزيء بنتان ، به جذران إيثان ، متصلان بالكربون 2 و 3:
2،3-إيثيل البنتان. جزيء الأوكتان ، وجذر البروبان عند الكربون 6 ، وجذور الميثان عند الكربون 4 و 5 ، وجذور الإيثان ، المرتبطة بالكربون 2 و 3 و 4: 4،5-ميثيل -2،3،4-إيثيل 6- بروبيل -أوكتان.
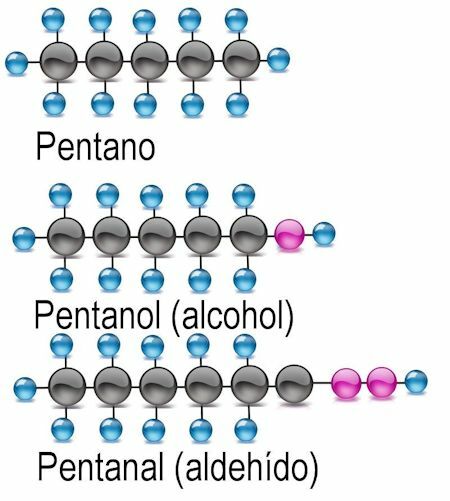
مجموعة الكحول الوظيفية
أبسط المجموعات الوظيفية هو الكحول ، حيث يتم استبدال ذرة الهيدروجين بمجموعة الهيدروكسيل (OH). في هذه المركبات ، تتم إضافة النهاية -anol إلى اسم الراديكالية. عند الاقتضاء ، يجب ذكر ذرة الكربون حيث توجد المجموعة الوظيفية:
أمثلة CH3OH: الميثانول: C2ح5OH الإيثانول ج4ح9OH بيوتانول أو 2-بيوتانول ؛ ج6ح13OH hexanol ، 2-hexanol (مجموعة وظيفية في atom 2) ، 3-hexanol (مجموعة وظيفية في ذرة 3).
مجموعة الألدهيد الوظيفية
في الألدهيدات ، يتم تبادل ذرة الهيدروجين للمجموعة الوظيفية -CHO. للتعرف عليها ، تتم إضافة النهاية-الشرج ، كما تم ذكر ذرة الكربون حيث توجد المجموعة الوظيفية:
أمثلة CH3COH: الميثان: C2ح5إيثانال كوه. ج4ح9COH butanal أو 2-butanal ؛ ج6ح13COH hexanal ، 2-hexanal (المجموعة الوظيفية في الذرة 2) ، 3-hexanal (المجموعة الوظيفية في الذرة 3).
المجموعة الوظيفية الحمضية
في الأحماض العضوية ، يتم تبادل ذرة الهيدروجين للمجموعة الوظيفية -COOH. للتعرف عليها ، تم ذكر كلمة حمض وإضافة النهاية -anoic ، كما تم ذكر ذرة الكربون حيث توجد المجموعة الوظيفية:
أمثلة CH3COOH: حمض الميثانويك: C2ح5حمض COOH ethanoic ؛ ج4ح9حمض COOH البوتانويك أو حمض 2-بوتانويك ؛ ج6ح13حمض هيكسانويك COH ، حمض 2-هيكسانويك (المجموعة الوظيفية في الذرة 2) ، 3-حمض هيكسانويك (المجموعة الوظيفية في الذرة 3).


