مثال الكيمياء العضوية
كيمياء / / July 04, 2021
ال الكيمياء العضوية هو جزء من الكيمياء العامة المسؤول عن الدراسة والتصنيف الوظيفي للمركبات الكيميائية التي يكون عنصرها الهيكلي هو كربون، الموجودة بوفرة في المادة الحية; وهكذا يتم إنشاء كون مختلف جيدًا عن الكيمياء غير العضوية ، مخصص للمركبات الكيميائية المصنفة على أنها معادن.
تحتوي ذرة الكربون على أربعة إلكترونات في الغلاف الأخير من تكوينها الإلكتروني. هذه الخاصية ، إلى جانب تلك الخاصة بنصف قطرها الذري ، تسمح لها بالارتباط بروابط تساهمية بالآخرين ذرات من نفس العنصر ، في سلاسل عديدة ، تشكل تنوعًا كبيرًا من المركبات الكيميائية مستقر.
يمكنك التحقق روابط تساهمية.
تحتوي هذه المركبات الكيميائية ، بالإضافة إلى ذرات الكربون التي تمنحها هيكلها البدائي ، على ذرات الهيدروجين كمكمل رئيسي لتكافؤ الكربون. بالإضافة إلى ذلك ، في هذا التنوع من المركبات ، هناك تلك التي تدخل ذرات الأكسجين ، النيتروجين والهالوجينات والكبريت وحتى الفوسفور والعناصر القلوية والقلوية الأرضية والمعادن من انتقال. اعتمادًا على من يشارك في الجزيء ، ستكون الخواص الفيزيائية والكيميائية للمادة النهائية.
ال مركبات العضوية موجودة في جميع أنحاء
المادة الحية; تعزيز واستدامة الجميع وظائف بيولوجيةعلى عكس المواد غير العضوية أو المعدنية التي استخدمها الإنسان لأغراض تجارية أو للتجارب أو لأداء مهام منزلية معينة.تاريخ الكيمياء العضوية
قبل عام 1828 ، كان هناك تمييز بالفعل بين الكيمياء العضوية والكيمياء غير العضوية. ارتبطت المادة العضوية بالخليقة من خلال أ "قوة قاتلة"، وغير العضوي مع غير الحي ، بالمعدن. بالنظر إلى هذه المفاهيم ، لا يمكن للمرء أن يتوقع الحصول على مركبات عضوية من مواد غير عضوية في المختبر.
ومع ذلك، في عام 1828 فريدريك فولر (1800-1882) نجح في تحضير مادة عضوية ، اليوريا CO (NH2)2، منتج مهم في التمثيل الغذائي الحيواني ، من المركبات غير العضوية. علاج الرصاص سيانات الرصاص (CNO)2 مع الأمونيا NH3 لتأخذ، لتمتلك سيانات الأمونيوم NH4CNO; تم تكوين هذا المركب بالفعل ، ولكن عندما تم غليان المحلول لتبلور سيانات الأمونيوم ، تم تحويله إلى اليوريا.
هذا التغيير الكيميائي هو مثال على إعادة التجميع الداخلي، حيث لا يتغير عدد أو صنف الذرات في الجزيء ، ولكن فقط ترتيبها داخل الجزيء. هذه الأنواع من التحولات شائعة جدًا في الكيمياء العضوية.
بدأ اكتشاف Wöhler التخلي عن نظرية قوة الحياة لاحقًا تم التخلص منها تمامًا من خلال اتباعها لتحضير العديد من المركبات العضوية الأخرى في مختبر. على الرغم من ذلك ، فإن مؤهلات المواد غير العضوية والعضوية موجودة ، لأن المركبات غير العضوية مرتبطة بالمنتجات المعدنية والمركبات العضوية ، والتي هي في الواقع مركبات الكربون والهيدروجين ومشتقاتهما ، هي من النوع الذي تنتجه الكائنات الحية.
على الرغم من أن قوانين الكيمياء العامة تنطبق بالتساوي على كلا المركبين ، إلا أن هناك أسبابًا مختلفة تبرر وتجعل هذا التقسيم ضروريًا. وبالتالي ، تختلف المركبات العضوية وغير العضوية في خصائص مختلفة ، مثل: الذوبان يفضل في المذيبات العضوية (الأثير ، الكحول ، الكلوروفورم ، إلخ) وفي الماء ، على التوالي ، استقرار (تتحلل المركبات العضوية عند درجات حرارة منخفضة نسبيًا) ، و طابع ردود الفعل; بالنسبة للمركبات غير العضوية فهي أيونية وبسيطة وآنية عمليًا ، وبالنسبة للمركبات العضوية فهي تساهمية ومعقدة وبطيئة.
مركبات العضوية
تُعرف مركبات الكربون بسلاسل تصل إلى تسعين ذرة. ال السلاسل يمكن أن تكون ذرات الكربون خطية ومتفرعة ولها روابط تساهمية مفردة أو روابط ثنائية أو ثلاثية. من المعروف أن أكثر من 2500 مركب تحتوي فقط على الكربون والهيدروجين (الهيدروكربونات).
ايزومرية المركبات العضوية
في المركبات غير العضوية ، تمثل الصيغة بشكل عام مركبًا واحدًا ؛ وبالتالي ، هناك مادة واحدة فقط من الصيغة H.2جنوب غرب4. يحتوي جزيء حامض الكبريتيك على ذرتين هيدروجين ، واحدة من الكبريت وأربع ذرات أكسجين ، بترتيب محدد وفريد. في المركبات العضوية هو نادر الحدوث. وهكذا ، على سبيل المثال ، هناك مركبان يستجيبان للصيغة C2ح6أو الكحول الإيثيلي أو الإيثانول وثنائي ميثيل الأثير.

كلما زاد تعقيد الجزيء ، زاد عدد ذرات الكربون ، زاد عدد الأيزومرات الممكنة.
تحليل المركب العضوي
يشتمل تحليل المركب العضوي على التحليل النوعي، ال تحليل كمي و ال تحليل وظيفي. في حالة افتراض أن المركب في حالة نجسة ، يتم تنقيته مسبقًا بواسطة بلورة, التقطير, تسامي, استخلاص، إلخ. يمكن الحكم على معيار النقاء على أساس الثوابت الفيزيائية ، مثل نقطة الانصهار ، نقطة الغليان ، الكثافة ، الذوبان ، الشكل البلوري ، معامل الانكسار ، إلخ.
ال التحليل النوعي يتم التحقق من وجود العناصر المكونة للمركب وخاصة الكربون والهيدروجين والنيتروجين وأحيانًا الهالوجينات والكبريت والفوسفور.
ال تحليل كمي يتم تنفيذه باستخدام الأساليب المستخدمة في التحليل النوعي كأساس. نقطة البداية هي كمية معينة من المادة التي تخضع للاحتراق ، ويتم جمع ثاني أكسيد الكربون ووزنه. يتكون الكربون وبخار الماء لحساب النسبة المئوية للكربون والهيدروجين في مجمع. نتائج التحليل الكمي تسهل حساب الصيغة التجريبية، على الرغم من أنه لا يمكن العثور على الصيغة الجزيئية إلا بعد تحديد الوزن الجزيئي للمادة. لكن المشكلة لم تحل بعد ، لأن نفس الصيغة الجزيئية يمكن أن تتوافق مع أيزومرات مختلفة.
تصنيف المركبات العضوية
وفقًا لتركيبها ، تنقسم المركبات العضوية إلى مركبات أليفاتية, عطري ص حلقية غير متجانسة. ترتبط المركبات الأليفاتية بالميثان CH4، هي سلسلة مفتوحة ، باستثناء cycloparaffins ، وتدين باسمها لحقيقة أن الدهون الحيوانية والنباتية تنتمي إلى هذه المجموعة.
ال المركبات العطرية، سلسلة مغلقة ، وثيقة الصلة بالبنزين ، ج6ح6، وهم مدينون باسمهم لحقيقة أن العديد منهم لديهم روائح عطرة ورائعة.
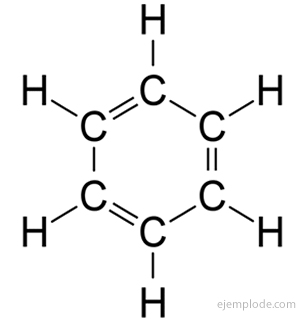
خاتم بنزين
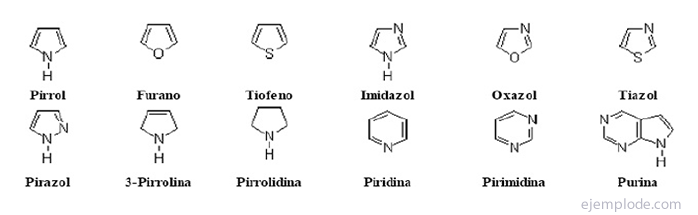
ال المركبات الحلقية غير المتجانسة إنها مركبات سلسلة مغلقة يوجد فيها عنصر آخر غير الكربون في الحلقة.
حسب دستورهم ، هم:
الهيدروكربونات، والتي بدورها ، نظرًا لنوع الروابط التي لديها ، يتم تصنيفها على أنها الألكانات, الألكينات ص ألكينز. بالإضافة إلى ذلك ، فإن السيكلو ألكانات والبنزين ومشتقاتهما تتكون فقط من الكربون والهيدروجين في هذه الفئة.
المركبات الحلقية غير المتجانسة
المشتقات المهلجنة:آر إكس
مركبات النيترو:R-NO2
أحماض السلفونيك:R-SO3ح
النتريل (أو ألكيل السيانيد) والإيزونتريل:R-CN و R-NC. وهي تختلف في كيفية ارتباط ذرة النيتروجين بالجزيء.
الكحوليات:R-OH
الفينولات: مركبات تعتمد على عمود فقري يتكون من حلقة بنزين مع مجموعة هيدروكسيل مضافة.

الاثيرات:R-O-R
مركابتان: R-SH
ثيويثرز:R-S-R
الأحماض:R-COSH
الألدهيدات:R-CHO
الكيتونات:R-CO-R
الأحماض الكربوكسيلية:R-COOH
انت اخرج:R-COOM (م للمعادن)
استرات: R-COO-R
أنهيدريد: R-CO-O-OC-R
الأمينات:R-NH2، R-NH-R ، 2R-N-R
الكربوهيدرات من نوع الدوسا:-CHOH- CHOH- CHO
الكربوهيدرات من نوع الكيتوز:-CHOH- CO-CH2أوه
المركبات العضوية الفلزية:R-M-R
هاليدات ألكيل المعدنية:R-MX (المعروف أيضًا باسم Grignard Reagents)