20 Примери за ковалентни връзки
Miscellanea / / July 04, 2021
Много химични съединения са съставени от молекули които от своя страна са съставени от атоми. За да образуват молекули, атомите се съединяват, образувайки се химически връзки.
Химическите връзки не са еднакви: те основно зависят от електронните характеристики на участващите атоми, техните стойности на електроотрицателност, наред с други фактори. Най-често срещаните видове връзки са: йонни връзки и ковалентни връзки.
Между неметални атоми на същите се образуват ковалентни връзки химичен елемент, между неметални атоми на различни елементи с разлика в електроотрицателността по-малка или равна на 1,7 и между a неметални и водород. Например: дихлор, молекулярен кислород, вода.
Ковалентната връзка се образува, когато два от тези атоми споделят електроните на последното си енергийно ниво, за да изпълнят Правило на октета, който установява, че йоните на различните химични елементи, открити в Периодичната таблица са склонни да завършат последните си енергийни нива с 8 електрона, за да могат молекулите да придобият стабилност, подобна на тази на Благородни газове.
Следователно начинът, по който тези вещества или химични съединения постигат стабилност, е чрез споделяне на двойка електрони (по един от всеки атом). По този начин споделената двойка електрони е обща за двата атома и в същото време ги държи заедно.
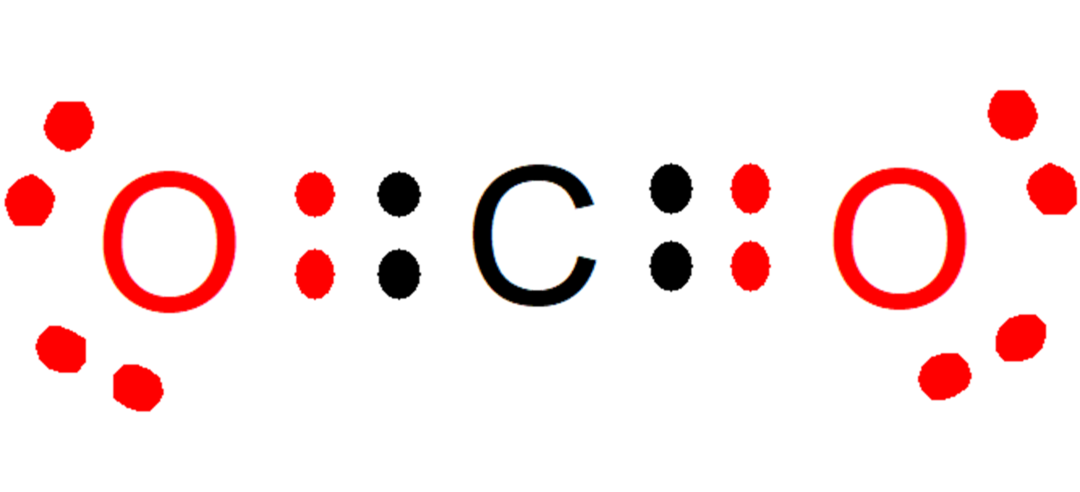
Например в въглероден диоксид (CO2), всеки кислород допринася два електрона (червен цвят) за връзката с въглерод, докато въглеродът допринася два електрона (черен цвят) за всяка връзка с всеки кислород. В образуваното съединение остават 8 електрона на всеки атом и по този начин се изпълнява Правилото на Октета.
Видове връзки
Има фундаментално три вида ковалентни връзки, въпреки че е важно да се изясни, че никоя връзка не е абсолютно ковалентна или абсолютно йонна. Всички връзки имат определен процент ковалентни и йонни, всъщност йонната връзка понякога се разглежда като „надценяване“ на ковалентната връзка. В този смисъл могат да възникнат следните видове ковалентна връзка:
Вещества, съставени от ковалентни молекули
The вещества които съдържат ковалентни молекули може да възникне във всяко състояние на материята (твърдо, течно или газообразно) и като цяло са лоши проводници на горещо и на електричество.
Има молекулярни ковалентни вещества и ретикулярни ковалентни вещества. The молекулярни коваленти те имат ниски точки на кипене и топене, разтворими са в неполярни разтворители (като бензен или въглероден тетрахлорид) и са меки в твърдо състояние. The решетка ковалентна Те образуват кристални решетки, поради което имат по-високи точки на топене и кипене и са твърди, неразтворими твърди вещества.
Примери за ковалентни връзки
Могат да се дадат многобройни примери за съединения или вещества, съдържащи ковалентни връзки:
- Дифлуор
- Дибромо
- Дихлор
- Дийодо
- Молекулен кислород
- Вода
- Амоняк
- Въглероден двуокис
- Метан
- Пропан
- Глюкоза
- Молекулен азот
- Кварц
- Парафин
- Дизел

Следвайте с:



