30 примера за алдехиди
Примери / / November 06, 2023
The алдехиди са органични съединения които са образувани от въглеродна верига, която има свързана крайна карбонилна група (= C = O) (разположена в единия край на молекула), който от своя страна е свързан с водороден атом.
Много често срещани алдехиди са метанал (формалдехид), етанал (ацеталдехид) и пропанал (пропалдехид).

Някои от тези съединения присъстват в природата, например ванилинът или ванилинът е естествен алдехид, който съставлява основния аромат на ванилията.
- Вижте също: Алдехиди и кетони
Номенклатура на алдехидите
Алдехидите могат да бъдат наименувани с помощта на номенклатурните правила, установени от Международния съюз за чиста и приложна химия (IUPAC).
За да се назове алдехид, се използват префикси, които показват броя на въглеродните атоми, които въглеродната верига е прикрепила към карбонилната група. Карбонилната група винаги е разположена в единия край на въглеродната верига, което означава, че винаги ще има позиция едно и не е необходимо да се посочва нейното местоположение във веригата. Освен това суфиксът -al се поставя в края на името на алдехида. Някои примери са:
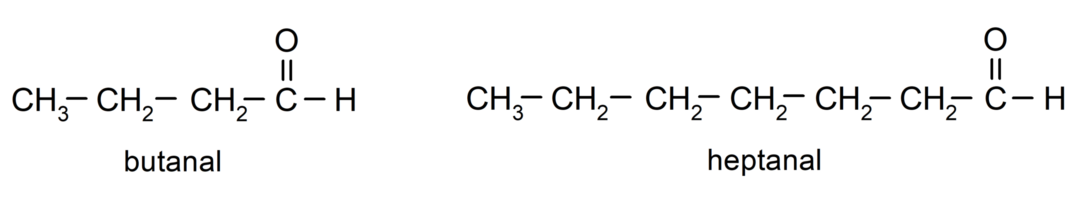
Ако алдехидът е разклонен, т.е. той е съставен от няколко въглеродни вериги, то главната верига като веригата, която има най-голям брой въглеродни атоми и която също съдържа групата карбонил. Останалите вериги са наречени като заместващи групи.
Освен това, всяка заместителна група трябва да бъде избрана така, че нейната позиция да заема най-ниското възможно номериране в главната въглеродна верига. От друга страна, въглеродните атоми на основната верига започват да се броят в края, който съдържа карбонилната група. Някои примери са:
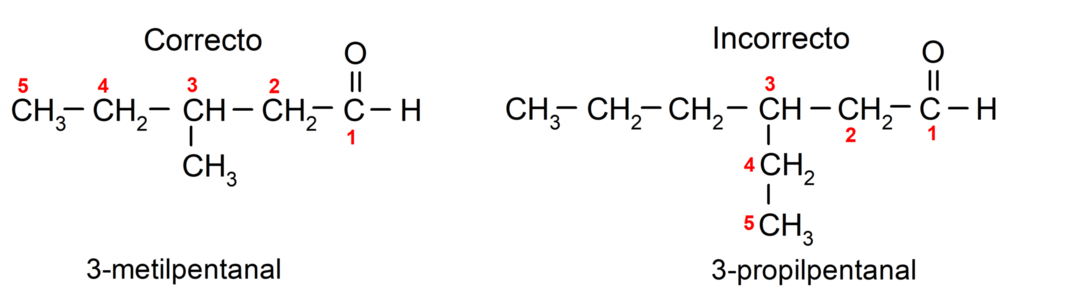
Ако алдехидът действа като заместител в молекулата, тъй като той също е изграден от групи функционални групи с по-висок приоритет, като киселини и естери, тогава алдехидната група е наречена като -оксо. Например:

Ако алдехидът има няколко карбонилни групи, той се наименува с помощта на префикси, които показват броя на тези групи, циферблат (две карбонилни групи), опит (три карбонилни групи) и т.н. Например:
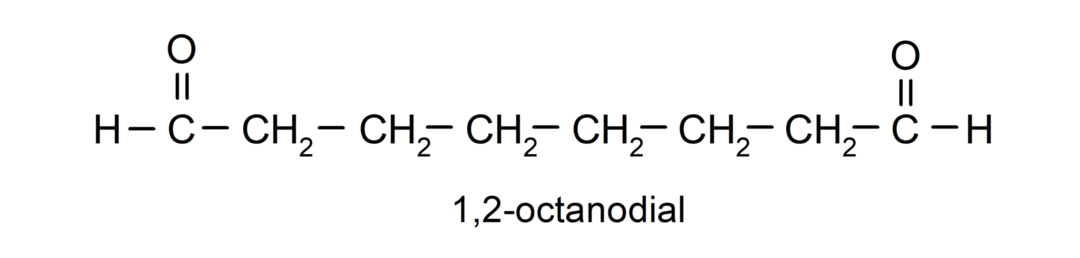
Когато карбонилната група е свързана с цикъл, алдехидите се наричат с термина карбалдехид. Например:

Физични свойства на алдехидите
Алдехидите обикновено имат някои вариации на същото физическо свойство. Това се случва, защото физичните свойства на алдехидите зависят от това как се образува въглеродната верига, която е прикрепена към карбонилната група.
Някои физични свойства на алдехидите са:
- Разтворимост. Водоразтворимостта на алдехидите зависи от количеството на атоми който има въглеродната верига. Алдехидите с по-къси въглеродни вериги (до около пет въглеродни атома) са разтворими във вода. Алдехидите с въглеродни вериги от много въглеродни атоми не са разтворими във вода. Метаналът и етаналът са много разтворими във вода.
- Плътност. Като цяло алдехидите са съединения с по-малка плътност от водата.
- Агрегационни състояния. Алдехидите, съставени от един и два въглеродни атома, са газове, тези, които съдържат между три и дванадесет въглеродни атома са течности, а тези, съставени от повече от дванадесет въглеродни атома, са твърди.
- Миризма. Някои алдехиди имат дразнеща миризма, докато други имат приятна миризма.
- Полярност. Карбонилната група им дава полярност.
- Точка на кипене. Те имат по-високи точки на кипене от алкани с подобно молекулно тегло и имат по-ниски точки на кипене от карбоксилни киселини и алкохоли със сравнимо молекулно тегло.
Химични свойства на алдехидите
Някои от химичните свойства на алдехидите са:
Алдехидите се окисляват, когато реагират с реагентите на Толенс, Бенедикт и Фелинг. за образуване на съответната карбоксилна киселина. Образуваната киселина ще има същия брой въглеродни атоми във въглеродната верига като алдехида, от който е образувана. Например:
- Окисляване с реагент на Толенс (амонячен сребърен комплекс в основен разтвор, [Ag (NH3)2]+). Тази реакция произвежда съответната киселина и метално сребро.

- Окисляване с реактив на Бенедикт и Фелинг (алкални разтвори на меден (II) сулфат (CuSO4) с различни състави). Тази реакция произвежда съответната киселина и меден оксид (Cu2ИЛИ).

Те претърпяват реакции на нуклеофилно присъединяване, където нуклеофилите се добавят към карбонилната група на алдехидите. Някои примери са:
- реакции на присъединяване алкохоли към карбонилната група на алдехидите, за да образуват ацетали и полуацетали.
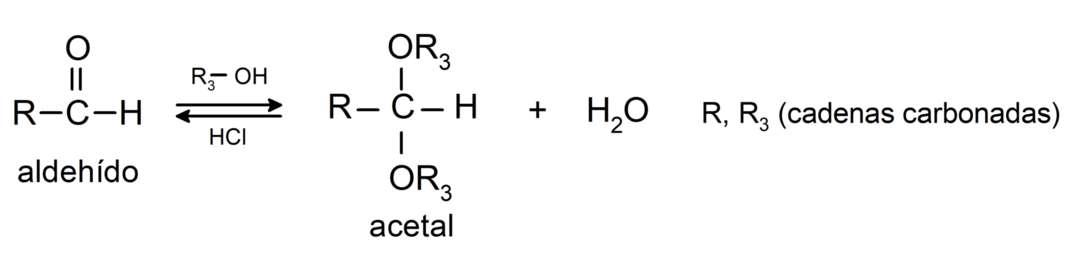
- реакции на присъединяване амини първичен към карбонилната група.

- Реакции на присъединяване на циановодородна киселина (HCN), при които се образуват цианохидрини или цианохидрини.

Те претърпяват реакции на алдолна кондензация. При този тип реакция два алдехида се кондензират, за да образуват алдол. Те са реакции, които протичат с натриев хидроксид (NaOH). Например:
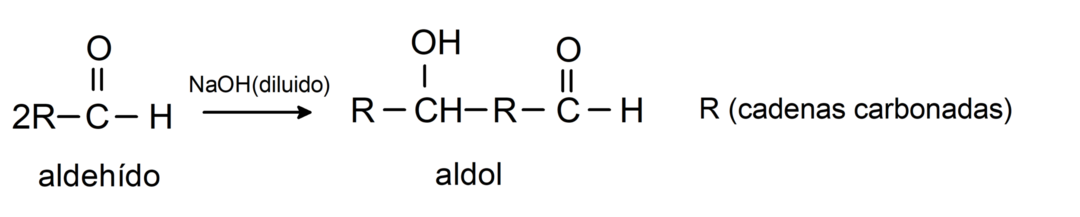
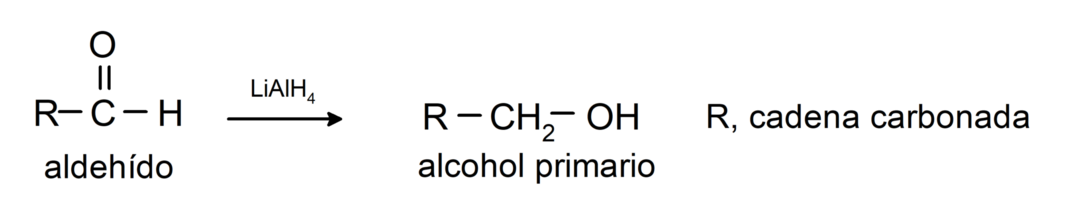
Те претърпяват редукционни реакции до първични алкохоли. В присъствието на натриев борохидрид (NaBH4) и литиево-алуминиев хидрид (LiAlH4) или чрез каталитично хидрогениране те се редуцират до първични алкохоли. Например:
Примери за алдехиди
- метанал (формалдехид)
- етанал (ацеталдехид)
- пропанал (пропалдехид)
- бутанал
- пентанал
- ванилин
- канелен алдехид
- пропенал
- бензалдехид
- хексанал
- 3-бромоциклопентанкарбалдехид
- циклохексанкарбалдехид
- 4,4-диметилпентанал
- 2-хидрокси-бутанал
- 2-хидрокси-2-метил-бутанал
- 2,3-диметилпентанал
- пентанедиал
- циклопентанкарбалдехид
- изобутанал
- 2-хлоро-бутанал

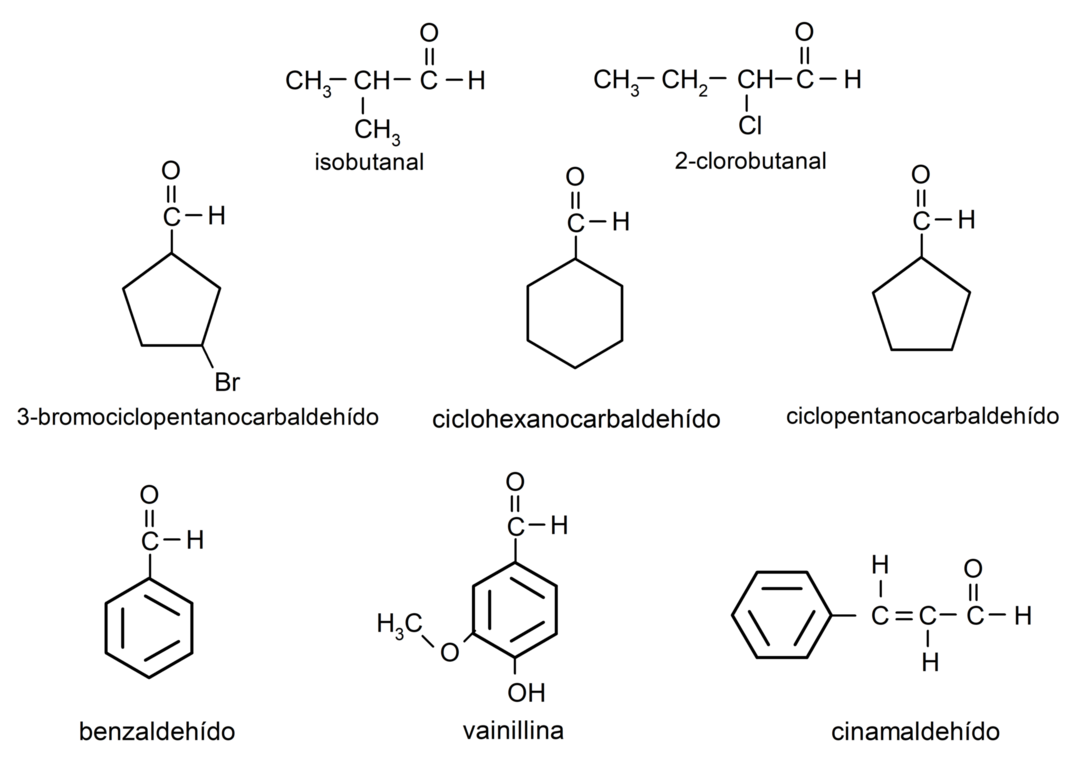
Алдехиди в природата
Някои алдехиди, присъстващи в природата, са:
- Бензалдехид, компонент на бадемите.
- Цинамалдехид, компонентът, който придава аромата на канелената есенция.
- Ванилин, компонентът, който придава вкуса на ванилията.
От друга страна, една от формите на глюкозата, отворената форма, има алдехидна функционална група.
Смята се, че ацеталдехидът, който се образува като междинен продукт при метаболизирането на алкохола, причинява симптоми на махмурлук при алкохолно опиянение.
Използване на алдехиди
Някои от основните приложения на алдехидите са:
- Използват се в производството на разтворители, бои, козметични продукти и есенции.
- Използват се при производството на смоли. Бакелитът се прави с формалдехид и е смола, която работи много добре като електрически изолатор.
- Те са били използвани като успокоителни. Паралдехидът е бил използван като успокоително и хипнотично средство, въпреки че вече не се използва поради неприятната си миризма.
- Използват се като консерванти за биологични проби и трупове. Формалдехидът се използва широко в този смисъл.
- Използват се като хранителни овкусители. Такъв пример е ванилинът, който се използва за придаване на ванилов аромат на десертите.
- Използват се като дезинфектанти.
Опасности от алдехиди
Няколко алдехида се считат за канцерогенни, например формалдехидът е обявен за канцерогенно съединение според СЗО (Световната здравна организация).
Излагането и контактът с много алдехиди причинява дразнене на кожата, очите и дихателните пътища. От друга страна причинява контактен дерматит и чернодробни заболявания.
Препратки
- Соломонс, T.W. Греъм и Мария Кристина Сангинес Франчини (1985). “органична химия” Мексико, D.F.: Limusa.
- Уитен, К. У., Гейли, К. Д., Дейвис, Р. Е., де Сандовал, М. T. ДА СЕ. О. и Мурадас, Р. М. ж. (1992). “Обща химия" (стр. 108-117). Макгроу-Хил.
- Артеага, П. М. (2017). “Кетони и алдехиди” Научен бюлетин на Подготвителното училище № 3, 4 (8).
Следвайте с:
- Захари
- Хидрациди
- Етилов алкохол
- Органични и неорганични съединения

