Пример за пептидна връзка
Химия / / July 04, 2021
The Пептидна връзка е тази, в която две молекули аминокиселини се свързват чрез кондензация.
За да се разберат по-добре пептидните връзки, първо трябва да се дефинират аминокиселините:
The Аминокиселините са органични молекули кратко, съдържащо поне амино група (-NH2), алкална по природа, и карбоксилна група (-COOH), киселинен характер.
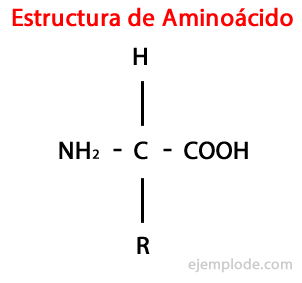
Въпреки че живите същества синтезират за различни цели много разнообразни видове аминокиселини, най-важните са тези, които са част от протеини, всички от които принадлежат към класа на а-аминокиселини.
Α-аминокиселините се характеризират с присъединяване на киселината и аминогрупите към един и същ въглероден атом, наречен α въглерод Освен това този α въглерод се свързва като трети заместител, водороден атом и като четвърти заместител, допълнителна група с различни размери и характеристики, която разграничава всяка аминокиселина от други.
Четвъртият заместител се нарича Странична верига Аминокиселина и често се представя в опростена форма с буквата R.
Тъй като четирите заместители на α-въглерода са различни и приемат тетраедрично разположение около него, наличните α-аминокиселини
оптична изомерия, което е, когато молекулата има a алтернативна форма което прилича на огледална картина неговата, която в крайна сметка не е еднаква молекула. На тези две изомерни форми на молекулата се присвояват буквите D или L, в зависимост от това как заместителите са подредени в пространството. Всички аминокиселини, които са в протеините, са L.Аминокиселините се класифицират според техния химичен характер в Полярен и Аполарен. Полярите от своя страна са разделени на Неутрално и заредено (които могат да бъдат киселинни или основни). The Неполярните могат да бъдат алифатни или ароматни.
Пептиди и пептидната връзка
Пептидите са продукт на ковалентното обединение на аминокиселини чрез амидни връзки, образуващи се от кондензация на карбоксилния край на единия и аминокрая на другия, освобождавайки водна молекула в реакция. Този съюз се нарича пептидна връзка.
Механизмът на тази реакция е представен по-долу, в който Амино и карбоксилни групи, и кондензацията на молекулите на аминокиселината се получава, за да образува пептида.
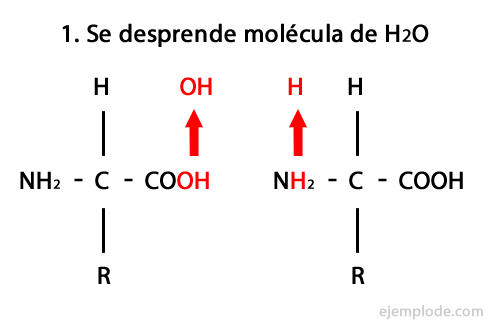
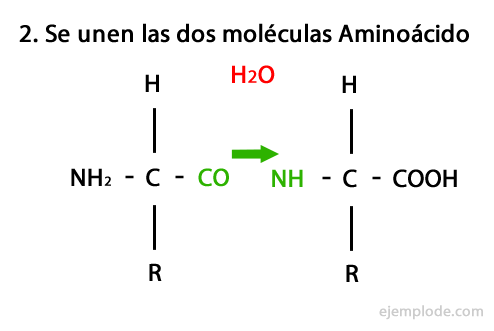

Пептиди, като аминокиселини и протеини, имат амино група и карбоксилна група в краищата си без да реагира.
За да се уточни формулата на обикновен пептид и дори протеин, е достатъчно да се изброят аминокиселините, които го съставят, като се започне с тази с безплатна Amino група, и завършва с този със свободната му карбоксилна група.
Някои пептиди, открити в тялото, са Вазопресин, който повишава кръвното налягане и увеличава реабсорбцията на вода в бъбреците; на Енкефалин, което намалява усещането за болка; и Окситоцин, което кара матката да се свива.
Характеристики на пептидната връзка
Кондензацията на аминогрупата на една аминокиселина с карбоксил на друга, се провежда във воден разтворител, така че не е спонтаннои следователно синтезът на протеини изисква доставка на енергия.
Пептидната връзка, както във всяка амидна връзка, представя резонанс между две крайни форми: неутралната форма, с единична връзка, свързваща карбонилния въглерод на първата аминокиселина и амино азота на втората (C-N), и формата с разделяне на таксите в която двата атома са свързани с двойна връзка (C = N). В действителност пептидната връзка не приема нито една от двете екстремни ситуации, но е резонансен хибрид и на двете.
Има обаждането Пептиден самолет, състояща се от всички атоми, участващи в пептидната връзка, които се присъединяват към двете първоначални аминокиселини. От една страна, атомите на азот и водород, със съответния им въглерод α в първата аминокиселина. От друга страна, въглеродът α на другата аминокиселина, с кислорода и въглерода на карбонилната група.
Разлики между пептидите и протеините
The пептидите имат малък брой аминокиселини, който варира от две до няколко десетки от тях и тяхната конформация в разтвор става гъвкава.
The малки протеини, структурно близки до големи пептиди, имат a дефинирана конформация и много по-малко гъвкава.
Има протеини, които, подобно на пептидите, имат неподредена и гъвкава конформация, но този ред, когато взаимодействат с други макромолекули в клетката.
20 примера за аминокиселини, които участват в пептидно свързване
- Глициния
- На момичето
- Валин
- Левцин
- Изолевцин
- Пролин
- Метионин
- Фенилаланин
- Тирозин
- Триптофан
- Серин
- Треонин
- Цистеин
- Аспарагин
- Глутамин
- Аспарагинова киселина
- Глутаминова киселина
- Лизин
- Аргинин
- Хистидин


