20 Příklady alkanů
Různé / / July 04, 2021
The alkany jsou jakési uhlovodíky ve kterém je proměnný počet atomů uhlíku spojen jednoduchými vazbami, jako je kostra, a každý atom uhlíku je zase připojen k atomům vodíku, které mohou být nakonec nahrazeny jinými atomy nebo funkční skupiny. Například: chloroform, methan, oktan.
The molekulární vzorec alkanů s otevřeným lineárním řetězcem je CnH2n + 2, kde C představuje uhlík, H představuje vodík a n představuje počet atomů uhlíku. Alkany jsou nasycené uhlovodíky, což znamená, že nemají dvojné nebo trojné vazby. Chcete-li je pojmenovat, použijte přípona „-Ano“ po pojmenování uhlíkového řetězce pomocí předpona odpovídající počtu atomů uhlíku (et- (2), pro- (3), but- (4), pen- (5), hex- (6), hep- (7) atd.).
Může vám sloužit:
Klasifikace alkanů
V rámci alkanů jsou obvykle rozpoznávány dvě velké skupiny: otevřený řetězec (také nazývaný acyklický) a uzavřený řetězec (nebo cyklický).
Když sloučeniny s otevřeným řetězcem Nepředstavují žádnou substituci vodíků, které doprovázejí každý atom uhlíku, nazývají se lineární alkany: jedná se o nejjednodušší alkany. Když představují substituci kteréhokoli ze svých vodíků jedním nebo více uhlíkovými řetězci, říká se jim rozvětvené alkany. Nejběžnějšími substituenty jsou ethylové skupiny (CH
3CH2-) a methyl (CH3-).Existují sloučeniny s jedním cyklem v molekule (monocyklické) a další s několika (polycyklickými). The cyklické alkany mohou být homocyklické (vytvářejí se výlučně pomocí atomů uhlíku) nebo heterocyklické (na kterých se podílejí jiné atomy, například kyslík nebo síra).
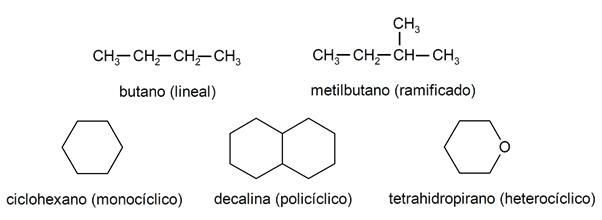
Fyzikální vlastnosti alkanů
Obecně, fyzikální vlastnosti alkanů je podmíněno molekulovou hmotností (následně spojenou s délkou uhlíkového řetězce). Ti s nejnižším počtem uhlíků jsou plynný na teplota prostředí, jsou v rozmezí od 5 do 18 atomů uhlíku kapalinya nad tímto číslem jsou pevný (podobně jako vosk).
Jelikož jsou méně husté než voda, mají tendenci se na nich vznášet. Obecně jsou alkany nerozpustné ve vodě a rozpustné v organických rozpouštědlech.
Jde o vařící a fúze alkanů závisí na jejich molekulová hmotnost, tj. na délce uhlíkového řetězce, i když také mnohokrát závisí na prostorovém uspořádání atomů. Lineární a cyklické alkany mají vyšší teploty varu než rozvětvené.
Chemické vlastnosti alkanů
Alkany se vyznačují tím, že jsou chemické sloučeniny velmi špatná reaktivita, proto jsou také známé jako „parafiny“ (v latině, parum affinis znamená „nízká afinita“). Jsou to sloučeniny, které mají při aktivaci velmi vysokou aktivační energii chemické reakce. Nejdůležitější reakcí, kterou alkany mohou podstoupit, je spalování za přítomnosti kyslíku, tepla, oxidu uhličitého a vody.
Alkany jsou základem pro důležitou škálu reakcí spojených s průmyslové procesy velmi důležité, protože jde o nejtradičnější paliva. Objevují se také jako konečné produkty biologických procesů, jako je methanogenní fermentace prováděná některými mikroorganismy.
Příklady alkanů
Některé příklady alkanů (včetně některých dobře známých lineárních a rozvětvených) jsou:
- Chloroform (ozdobný název trichlormethan; CHCI3). Páry této látky se dříve používaly jako anestetika. Z tohoto důvodu byla ukončena, protože bylo zjištěno, že je poškozena orgány důležité, jako jsou játra nebo ledviny. Dnes se používá hlavně jako rozpouštědlo nebo chladivo.
- Metan (CH4). Je to nejjednodušší alkan ze všech: je tvořen pouze jedním atomem uhlíku a čtyřmi vodíky. Je to plyn, který se přirozeně vyskytuje rozkladem různých organických substrátů a je hlavní složkou zemního plynu. V poslední době byl uznán jako jeden z plynů, který se nejvíce podílí na takzvaném skleníkovém efektu.
- Oktan (C8H18). Jedná se o osmikarbonový alkan a má velký význam, protože určuje konečnou kvalitu nafty, což je směs různých uhlovodíků. Tato kvalita se měří oktanovým číslem nebo oktanovým číslem paliva, které bere jako referenční nízko detonační (index 100) a vysoce detonující (index 0).
- Hexan (C6H14). Je to důležité rozpouštědlo, je třeba se vyvarovat jeho vdechování, protože je velmi toxický.
- Butan (C4H10). Spolu s propanem (C.3H8), tvoří tzv. zkapalněné ropné plyny (LPG), které se tvoří v plynových vakech během procesu těžby oleje. V současné době se prosazuje nahrazení benzinu nebo nafty LPG jako palivem ekologičtějšího uhlovodíku (během spalování emituje pouze oxid uhličitý a vodu).
- Icosano (C20H42). Je to alkan s dvaceti uhlíky (předpona „ico“ znamená dvacet)
- Cyklopropan (C3H6). Dříve to bylo používáno jako anestetikum
- n-heptan (C7H16). Je to ten, který je považován za referenční pro nulový bod stupnice benzínového oktanu, což by bylo nejméně žádoucí, protože hoří výbušně. Získává se z určité pryskyřice rostliny.
- 3-ethyl-2,3-dimethylpentan (C9H20)
- 2-methylbutan (C5H12)
- 3-chlor-4-n-propylheptan (C10H21Cl)
- 3,4,6-trimethylheptan (C10H22)
- L-brom-2-fenylethan (C8H9Br)
- 3-ethyl-4-methylhexan (C9H18)
- 5-isopropyl-3-methylnonan (C13H28)
- kubánský (C8H8)
- 1-brompropan (C3H7Br)
- 3-methyl-5-n-propyloktan (C12H26)
- 5-n-butyl-4,7-diethyldekan (C18H28)
- 3,3-dimethyldekan (C12H26)



