30 Příklady aldehydů
Příklady / / November 06, 2023
The aldehydy jsou organické sloučeniny které jsou tvořeny uhlíkovým řetězcem, který má připojenou koncovou karbonylovou skupinu (= C = O) (umístěnou na jednom konci molekula), který je zase vázán k atomu vodíku.
Velmi časté aldehydy jsou methanal (formaldehyd), ethanal (acetaldehyd) a propanal (propaldehyd).

Některé z těchto sloučenin jsou přítomny v přírodě, například vanilin nebo vanilin je přírodní aldehyd, který tvoří hlavní aroma vanilky.
- Viz také: Aldehydy a ketony
Názvosloví aldehydů
Aldehydy mohou být pojmenovány pomocí pravidel názvosloví stanovených Mezinárodní unií čisté a aplikované chemie (IUPAC).
Pro pojmenování aldehydu se používají předpony, které označují počet atomů uhlíku, které má uhlíkový řetězec připojen ke karbonylové skupině. Karbonylová skupina je vždy umístěna na jednom konci uhlíkového řetězce, což znamená, že bude mít vždy polohu jedna a není nutné uvádět její umístění v řetězci. Navíc je na konec názvu aldehydu umístěna přípona -al. Některé příklady:
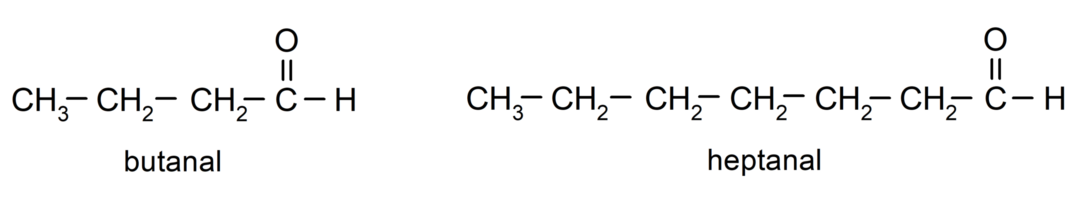
Pokud je aldehyd rozvětvený, to znamená, že se skládá z několika uhlíkových řetězců hlavní řetězec jako řetězec, který má největší počet atomů uhlíku a který také obsahuje skupinu karbonyl. Zbývající řetězce jsou pojmenovány jako substituční skupiny.
Dále musí být každá substituční skupina vybrána tak, aby její poloha zaujímala nejnižší možné číslování v hlavním uhlíkovém řetězci. Na druhé straně se atomy uhlíku hlavního řetězce začínají počítat na konci, který obsahuje karbonylovou skupinu. Některé příklady:
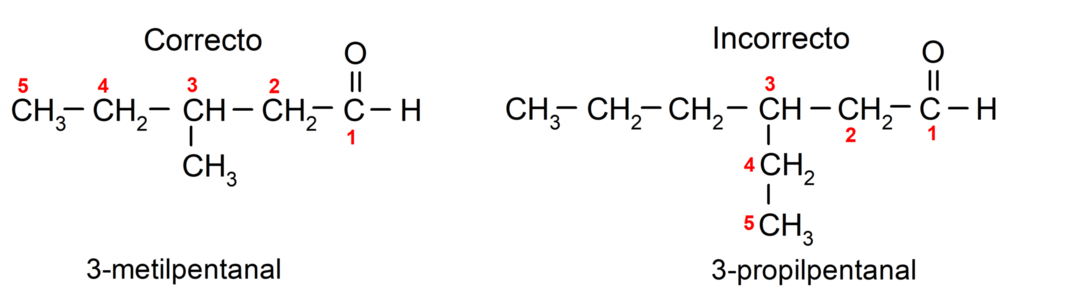
Působí-li aldehyd jako substituent v molekule, protože je také tvořen skupinami funkční skupiny s vyšší prioritou, jako jsou kyseliny a estery, pak je aldehydová skupina pojmenována jako -oxo. Například:

Pokud má aldehyd několik karbonylových skupin, je pojmenován pomocí předpon, které označují počet těchto skupin, dial (dvě karbonylové skupiny), trial (tři karbonylové skupiny) atd. Například:
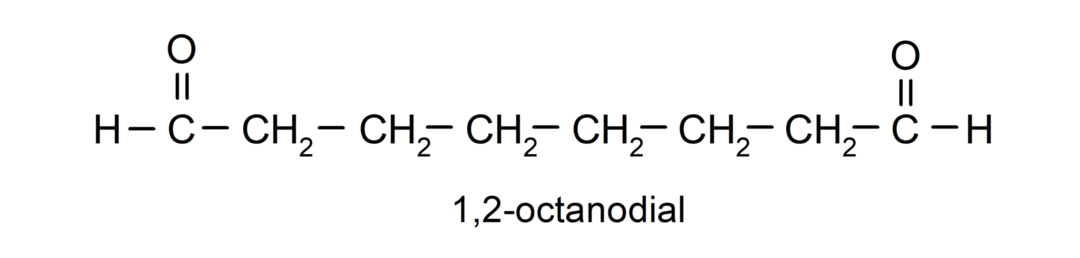
Když je karbonylová skupina spojena s cyklem, aldehydy jsou pojmenovány pomocí termínu karbaldehyd. Například:

Fyzikální vlastnosti aldehydů
Aldehydy mají obvykle určitou variaci stejné fyzikální vlastnosti. K tomu dochází, protože fyzikální vlastnosti aldehydů závisí na tom, jak se tvoří uhlíkový řetězec, který je připojen ke karbonylové skupině.
Některé fyzikální vlastnosti aldehydů jsou:
- Rozpustnost. Rozpustnost aldehydů ve vodě závisí na množství atomy která má uhlíkový řetězec. Aldehydy s kratšími uhlíkovými řetězci (asi do pěti atomů uhlíku) jsou rozpustné ve vodě. Aldehydy s uhlíkovými řetězci s mnoha atomy uhlíku nejsou rozpustné ve vodě. Methanal a ethanal jsou velmi dobře rozpustné ve vodě.
- Hustota. Obecně jsou aldehydy sloučeniny, které jsou méně husté než voda.
- Agregační státy. Aldehydy se skládají z jednoho a dvou atomů uhlíku plynyjsou ty, které obsahují tři až dvanáct atomů uhlíku kapalinya ty, které se skládají z více než dvanácti atomů uhlíku, jsou pevné.
- Vůně. Některé aldehydy mají dráždivý zápach, zatímco jiné mají příjemný zápach.
- Polarita. Karbonylová skupina jim dává polaritu.
- Bod varu. Mají vyšší body varu než alkany podobné molekulové hmotnosti a mají nižší body varu než karboxylové kyseliny a alkoholy srovnatelné molekulové hmotnosti.
Chemické vlastnosti aldehydů
Některé z chemických vlastností aldehydů jsou:
Aldehydy jsou oxidovány, když reagují s Tollensovými, Benedictovými a Fehlingovými činidly. za vzniku odpovídající karboxylové kyseliny. Vzniklá kyselina bude mít v uhlíkovém řetězci stejný počet uhlíků jako aldehyd, ze kterého vznikla. Například:
- Oxidace Tollensovým činidlem (amoniakový komplex stříbra v zásaditém roztoku, [Ag (NH3)2]+). Touto reakcí vzniká odpovídající kyselina a kovové stříbro.

- Oxidace Benediktovým a Fehlingovým činidlem (alkalické roztoky síranu měďnatého (CuSO)4) s různým složením). Tato reakce produkuje odpovídající kyselinu a oxid měďný (Cu2BUĎ).

Podléhají nukleofilním adičním reakcím, kde se ke karbonylové skupině aldehydů přidávají nukleofily. Některé příklady:
- adiční reakce alkoholy na karbonylovou skupinu aldehydů za vzniku acetalů a poloacetalů.
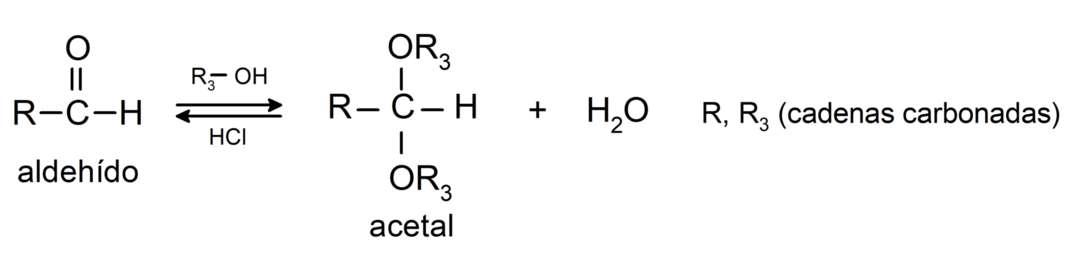
- adiční reakce aminy primární ke karbonylové skupině.

- Adiční reakce kyseliny kyanovodíkové (HCN), při kterých vznikají kyanhydriny nebo kyanhydriny.

Podléhají aldolovým kondenzačním reakcím. Při tomto typu reakce kondenzují dva aldehydy za vzniku aldolu. Jsou to reakce, ke kterým dochází s hydroxidem sodným (NaOH). Například:
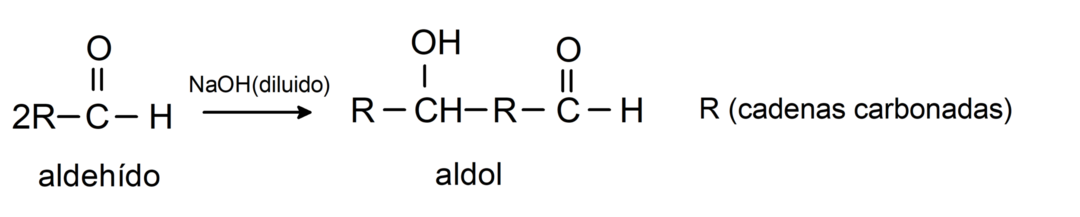
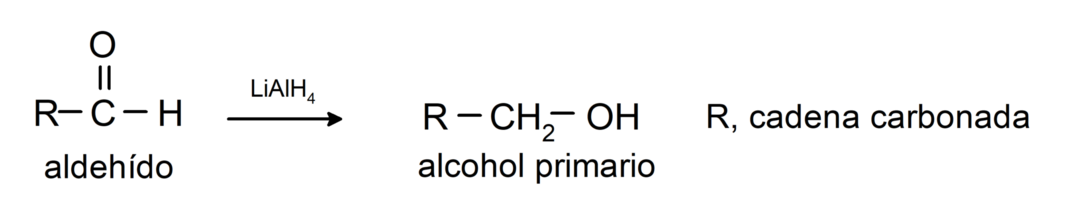
Podléhají redukčním reakcím na primární alkoholy. V přítomnosti borohydridu sodného (NaBH4) a lithiumaluminiumhydridu (LiAlH4) nebo katalytickou hydrogenací se redukují na primární alkoholy. Například:
Příklady aldehydů
- metan (formaldehyd)
- ethanal (acetaldehyd)
- propanal (propaldehyd)
- butanal
- pentanal
- vanilin
- cinnamaldehyd
- propenal
- benzaldehyd
- hexanal
- 3-bromcyklopentankarbaldehyd
- cyklohexankarbaldehyd
- 4,4-dimethylpentanal
- 2-hydroxybutanal
- 2-hydroxy-2-methylbutanal
- 2,3-dimethylpentanal
- pentanedial
- cyklopentankarbaldehyd
- isobutanal
- 2-chlor-butanal

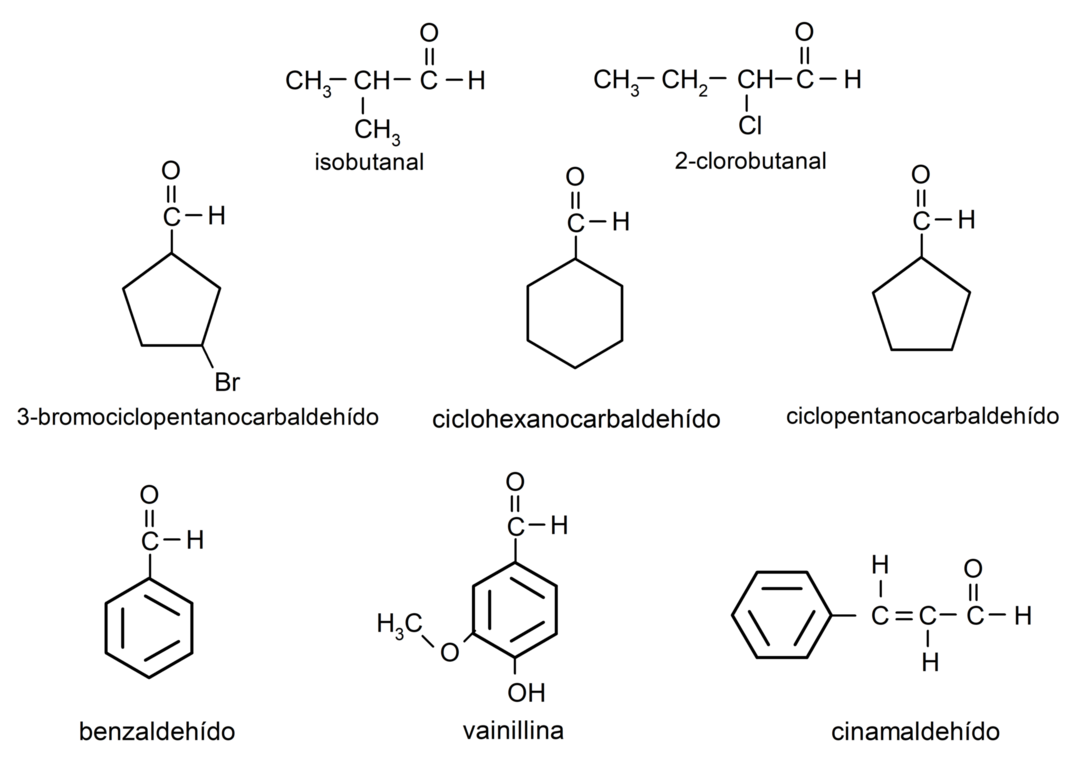
Aldehydy v přírodě
Některé aldehydy přítomné v přírodě jsou:
- Benzaldehyd, součást mandlí.
- Cinnamaldehyd, složka, která dává skořicové esenci její vůni.
- Vanilin, složka, která dává vanilce její chuť.
Na druhé straně jedna z forem glukózy, otevřená forma, má aldehydovou funkční skupinu.
Předpokládá se, že acetaldehyd, který vzniká jako meziprodukt při metabolizaci alkoholu, způsobuje při intoxikaci alkoholem příznaky kocoviny.
Použití aldehydů
Některé z hlavních použití aldehydů jsou:
- Používají se při výrobě rozpouštědel, barev, kosmetických produktů a esencí.
- Používají se při výrobě pryskyřic. Bakelit se vyrábí s formaldehydem a je to pryskyřice, která velmi dobře funguje jako elektrický izolant.
- Používaly se jako sedativa. Paraldehyd byl používán jako sedativum a hypnotikum, i když se nyní nepoužívá kvůli jeho nepříjemnému zápachu.
- Používají se jako konzervační prostředky pro biologické vzorky a mrtvoly. Formaldehyd je v tomto smyslu široce používán.
- Používají se jako dochucovadla potravin. Příkladem je vanilin, který dezertům dodává vanilkové aroma.
- Používají se jako dezinfekční prostředky.
Nebezpečí aldehydů
Několik aldehydů bylo považováno za karcinogenní, například formaldehyd byl podle WHO (Světová zdravotnická organizace) prohlášen za karcinogenní sloučeninu.
Expozice a kontakt s mnoha aldehydy způsobuje podráždění kůže, očí a dýchacích cest. Na druhou stranu způsobuje kontaktní dermatitidu a onemocnění jater.
Reference
- Solomons, T.W. Graham a María Cristina Sangines Franchini (1985). “organická chemieMexiko, D.F.: Limusa.
- Whitten, K. W., Gailey, K. D., Davis, R. E., de Sandoval, M. T. NA. O. & Muradás, R. M. G. (1992). “Obecná chemie" (str. 108-117). McGraw-Hill.
- Arteaga, P. M. (2017). “Ketony a aldehydy” Vědecký bulletin Svědomí Přípravné školy č. 3, 4(8).
Postupujte s:
- Cukry
- Hydracidy
- Ethylalkohol
- Organické a anorganické sloučeniny

