Vlastnosti lanthanidu
Chemie / / July 04, 2021
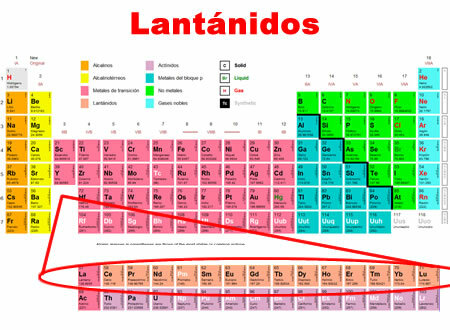
Lanthanidy jsou chemické prvky, které sahají od lanthanu po lutecium. Sdílejí společné charakteristiky, pro které jsou zařazeni do zvláštní kategorie ve spodní části periodické tabulky.
Hlavní vlastnosti lanthanoidů:
- Jsou umístěny v období 6 periodické tabulky.
- Zahrnují 15 prvků, od 57 do 71.
- Sdílejí strukturu lanthanu, ke kterému se přidává energetická hladina f, která je chemicky méně reaktivní.
- Říkali jim vzácné zeminy, protože v přirozeném stavu jsou vždy kombinovány za vzniku oxidů.
- Některé jsou poměrně hojné.
- Ačkoli mají proměnlivé valence, většina má +3 valence.
- Jak se jeho atomové číslo zvyšuje, jeho poloměr se zmenšuje.
- Všechny mají lesklý kovový vzhled.
Jednotlivé vlastnosti lanthanoidů:
Lanthan (La).
- Atomové číslo 57
- Atomová hmotnost: 139
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 920 ° C
- Bod varu: 3457 ° C
Bylo objeveno v roce 1839. V průmyslu se používá ve slitinách s jinými lanthanoidy k výrobě lehčích kamenů; v optice se používá pro optická skla. Používá se také pro vodíkové houby, které obsahují plyny. V medicíně se používá ve formě uhličitanu lanthanitého k léčbě selhání ledvin, protože má afinitu ke smíchání s fosfáty, což snižuje hyperfosfémii.
Cer (Ce)
- Atomové číslo 58
- Atomová hmotnost: 140
- Stav: Měkký pevný
- Vzhled: Kovový, stříbrně šedý, železný
- Valencie: +3, +4
- Teplota tání: 798 ° C
- Bod varu: 3426 ° C
Bylo objeveno v roce 1803. Je to nejhojnější lanthanid. Používá se k výrobě katalyzátorů, zejména pro automobily (katalyzátory) a pro krakování ropy. Ve formě oxidu se používá k leštění brýlí a čoček. Ačkoli nemá žádné známé biologické funkce, v medicíně se používá v mastích na popáleniny.
Praseodymium (Pr)
- Atomové číslo 59
- Atomová hmotnost: 144
- Stav: Měkký pevný
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 931 ° C
- Bod varu: 3520 ° C
Byl objeven v roce 1841 a izolován v roce 1885. V průmyslu se používá ve slitinách s hořčíkem k výrobě leteckých motorů; Používá se k získání skla a smaltů žluté barvy. Slitiny niklu mají magnetické vlastnosti. Reaguje s halogeny za vzniku fluoridů, chloridů, bromidů a jodidů.
Neodym (Nd)
- Atomové číslo 60
- Atomová hmotnost: 139
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 1024 ° C
- Bod varu: 3100 ° C
Bylo objeveno v roce 1885, kdy byl izolován praseodym; neodym byl izolován až do roku 1925. Je to jeden z nejreaktivnějších lanthanoidů. V průmyslu se používá k barvení skla a emailů. Díky své schopnosti absorbovat světlo se používá v astronomii k vytváření krystalů, pomocí kterých jsou kalibrovány infračervené spektrometry a filtry. Jedním z jeho hlavních použití je výroba magnetů o vysoké magnetické intenzitě. Tyto magnety se používají pro přesné přístroje, jako jsou magnety používané na pevných discích počítačů, a také pro některé tenkoformátové reproduktory.
Promethium (Pm)
- Atomové číslo 61
- Atomová hmotnost: 145
- Pevné skupenství
- Vzhled:?
- Valencie: +3
- Teplota tání: 1100 ° C
- Bod varu: 3000 ° C
Jeho existence byla předpovězena v roce 1902, ale mohla být prokázána až v roce 1944. Tento lanthanid se v přírodě nenachází, je zdrojem jeho získávání a studia štěpení uranu. Při štěpení uranu v jaderném reaktoru je jedním z atomů, které se produkují z této atomové separace, promethium. Má radioaktivní vlastnosti, které mu dodávají fosforescenci, a používá se pro kalibrátory a jaderné baterie používané v kosmických lodích.
Samarium (Sm)
- Atomové číslo 62
- Atomová hmotnost: 150
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 1072 ° C
- Bod varu: 1803 ° C
Byl objeven v roce 1853 a izolován v roce 1879. Má několik izotopů a nejméně dva z nich jsou radioaktivní. V průmyslu se v optice používá k výrobě krystalů, které absorbují infračervené světlo. Používá se také jako katalyzátor pro získání alkoholu a jako prvek v některých zářivkách a televizorech. Pokud jde o zdraví, může při vdechování (například oxidu použitém k leštění krystalů) způsobit plicní embolii nebo ovlivnit játra. Radioaktivní izotopy se používají při radioterapii nevyléčitelně nemocných pacientů.
Europium (EU)
- Atomové číslo 63
- Atomová hmotnost: 152
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +2, +3
- Teplota tání: 826 ° C
- Bod varu: 1527 ° C
Bylo objeveno v roce 1890. Je to nejreaktivnější z lanthanoidů. Používá se v zářivkách a televizorech, ale pokud je, způsobí plicní embolii vdechování nebo poškození jater, pokud se nahromadí v lidském těle, nemá téměř žádné průmyslové využití. V atomovém výzkumu se používá, protože absorbuje neutrony.
Gadolinium (Gd)
- Atomové číslo 64
- Atomová hmotnost: 157
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 1312 ° C
- Bod varu: 3250 ° C
Gadolinium má několik použití, hlavním je magnetické průmyslové chlazení, protože zvyšuje své magnetické vlastnosti při nízkých teplotách; ale protože tento typ chladičů vyžaduje použití arsenu, nepoužívají se v domácím chlazení. V medicíně se používá jako kontrastní látka pro magneticko-nukleární rezonanci.
Terbium (Tb)
- Atomové číslo 65
- Atomová hmotnost: 159
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +4
- Teplota tání: 1356 ° C
- Bod varu: 3230 ° C
Byl objeven v roce 1843 a izolován v roce 1905. Je to velmi důležité v elektronickém průmyslu, protože je to jeden z prvků používaných k výrobě polovodičů. Další využití je k výrobě zářivek a obrazovek. Používá se také jako katalyzátor v palivových článcích. Ačkoli nemá žádné biologické funkce, jeho vdechování nebo vstup do lidského těla má toxické účinky, zejména na játra.
Dysprosium (Dy)
- Atomové číslo 66
- Atomová hmotnost: 162,5
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +2, +3
- Teplota tání: 1407 ° C
- Bod varu: 2567 ° C
Byl objeven v roce 1843 a izolován v roce 1905. Je to velmi důležité v elektronickém průmyslu, protože je to jeden z prvků používaných k výrobě polovodičů. Další využití je k výrobě zářivek a obrazovek. Používá se také jako katalyzátor v palivových článcích. Ačkoli nemá žádné biologické funkce, jeho vdechování nebo vstup do lidského těla má toxické účinky, zejména na játra.
Holmium (Ho)
- Atomové číslo 67
- Atomová hmotnost: 166
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 1474 ° C
- Bod varu: 2700 ° C
Byl objeven v roce 1878 a jeho název je odvozen od města jeho objevu, Stockholmu, latinsky Holmia. Nemá téměř žádné praktické využití; v některých průmyslových odvětvích se však používá jako katalyzátor chemických reakcí i pro některé elektronické součástky. Používá se také ke změně frekvence a intenzity laserového paprsku.
Erbium (Er)
- Atomové číslo 68
- Atomová hmotnost: 167
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 1795 ° C
- Bod varu: 2863 ° C
Bylo objeveno v roce 1843. Používá se v jaderném průmyslu jako neutronový nárazník. Ve formě oxidu je to barvivo pro krystaly, které jim dodává růžový odstín; Tyto krystaly se používají v optice a špercích. Používá se také k výrobě optických vláken.
Thulium (Tm)
- Atomové číslo 69
- Atomová hmotnost: 167
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 1545 ° C
- Bod varu: 1947 ° C
Bylo objeveno v roce 1879. I přes nízkou dostupnost, vzhledem k radioaktivním vlastnostem, se používá hlavně jako rentgenový paprsek v přenosných zařízeních a pro polovodičové lasery.
Ytterbium (Yb)
- Atomové číslo 70
- Atomová hmotnost: 173
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 824 ° C
- Bod varu: 1194 ° C
Byl objeven v roce 1878 a izolován v roce 1907. Radioaktivní izotopy se používají pro přenosná rentgenová zařízení, která fungují bez elektřiny. Používá se také ke zlepšení ocelových slitin a ke zvýšení jejich odolnosti, což je vlastnost používaná ve stomatologii, díky zlepšení mechanických vlastností oceli. Musí se s ním zacházet opatrně, protože může způsobit podráždění a popáleniny. Kromě toho může při reakci se vzduchem způsobit výbuch nebo požár.
Lutetium (Lu)
- Atomové číslo 71
- Atomová hmotnost: 175
- Pevné skupenství
- Vzhled: Kovový, stříbřitě bílý
- Valencie: +3
- Teplota tání: 1652 ° C
- Bod varu: 3402 ° C
Bylo objeveno v roce 1907. Je to nejméně hojný chemický prvek v zemské kůře. Přes svou nízkou dostupnost se používá k rafinaci oleje a jako katalyzátor pro reakce organické chemie. Některé radioaktivní izotopy byly také testovány na léčbu radiační terapií.

