Příklad Charlesova zákona
Fyzika / / July 04, 2021
Charlesův plynový zákon nebo zákon stálého tlaku je dalším ze zákonů o plynu, vysvětlil Gay-Lussac, který vydal dílo Jacques Charles, publikoval kolem 20 před lety.
Charlesův zákon předpovídá chování masy plynu, když tlak zůstává konstantní a teplota a objem se mění.
Charlesův zákon je stanoven následovně:
Při konstantním tlaku je objem plynu přímo úměrný změně jeho teploty.
Konstantní tlak: odkazuje na skutečnost, že tlak vyvíjený plynem na stěny nádoby se nebude během celého zážitku měnit.
Objem: je to obsazený prostor, který plyn zabírá, obecně je považován za nádobu se stěnami, které se nedeformují, a jejíž víko funguje jako píst.
Teplota: Jedná se o nárůst nebo ztrátu tepla, kterému plyn podléhá během experimentování. Pokud se teplota zvýší, zvýší se hlasitost. Pokud teplota klesne, sníží se také hlasitost.
Algebraicky je Charlesův zákon vyjádřen následujícím vzorcem:

Kde:
V = objem plynu
T = teplota plynu
k = konstanta proporcionality pro tuto hmotnost plynu.
To znamená, že pro danou hmotnost plynu je při konstantním tlaku vztah mezi objemem a teplotní variace, budou mít vždy stejný vztah proporcionality představovaný konstantou k:

Jakmile je tedy konstanta určena, můžeme z ostatních známých dat vypočítat kteroukoli z dalších hodnot:
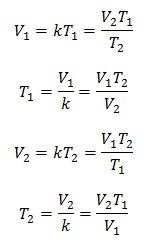
3 Příklady Charlesova zákona aplikovaného na problémy:
Příklad 1: Vypočítejte nový objem, pokud je v nádobě hmota plynu, která zaujímá objem 1,3 litru, při teplotě 280 K. Vypočítejte objem při dosažení teploty 303 K.
PROTI1 = 1,3 l.
T1 = 280 K.
PROTI2 = ?
T2 = 303 K.
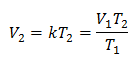
Nahrazení hodnot:
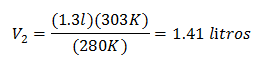
Nový objem 303 K je 1,41 litru.
Příklad 2. Pokud máme plyn, který při 10 stupních Celsia zabírá 2,4 litru, vypočítejte konečnou teplotu, pokud na konci zabírá 2,15 litru.
PROTI1 = 2,4 l
T1 = 10 ° C = 283 K.
PROTI2 = 2,15 l
T2 = ?
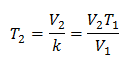
Nahrazení hodnot:
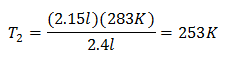
Nová teplota je 253 K, což se rovná -20 ° C.
Příklad 3. Máme plyn, jehož počáteční teplota je 328 K, jeho konečný objem je 3,75 la jeho konstanta poměru je 0,00885.
PROTI1 = ?
T1 = 328 K.
PROTI2 = 3,75 l
T2 = ?
k = 0,00885
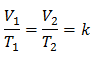
Nahrazení hodnot:
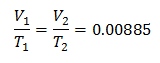
Znalost počátečního objemu:
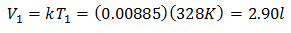
Počáteční objem je 2,90 l.
Zjištění konečné teploty:
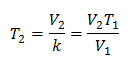
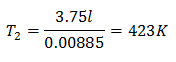
Konečná teplota bude 423 K, což se rovná 150 ° C.