50 Eksempler på aldehyder og ketoner
Eksempler / / November 06, 2023
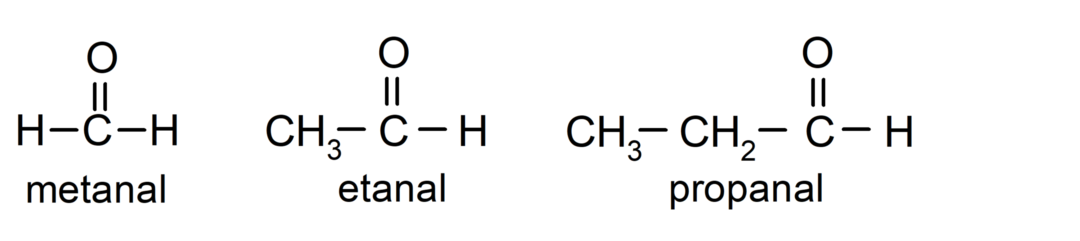
Det aldehyder er organiske forbindelser der i deres struktur har en funktionel carbonylgruppe (= C = O), der er bundet til en carbonkæde og et hydrogenatom. For eksempel: methanal (også kaldet formaldehyd), ethanal (også kaldet acetaldehyd) og propanal (også kaldet propaldehyd).
Det ketoner De er organiske forbindelser, der i deres struktur har en carbonylgruppe knyttet til to carbonatomer. For eksempel: propanon (også kaldet acetone), butanon og 2-pentanon.
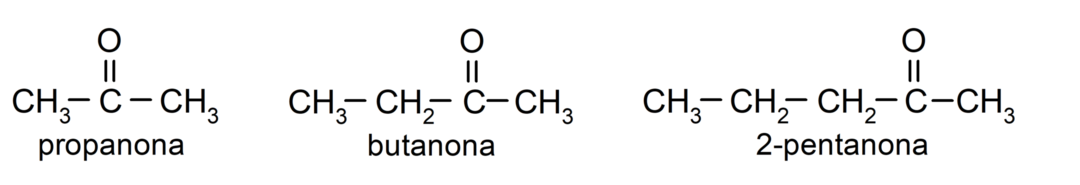
Forskelle mellem aldehyder og ketoner
De vigtigste forskelle mellem aldehyder og ketoner er:
- Aldehyder har i deres struktur en funktionel carbonylgruppe placeret i den ene ende, mens ketoner har carbonylgruppen placeret i ikke-terminale positioner af deres struktur.
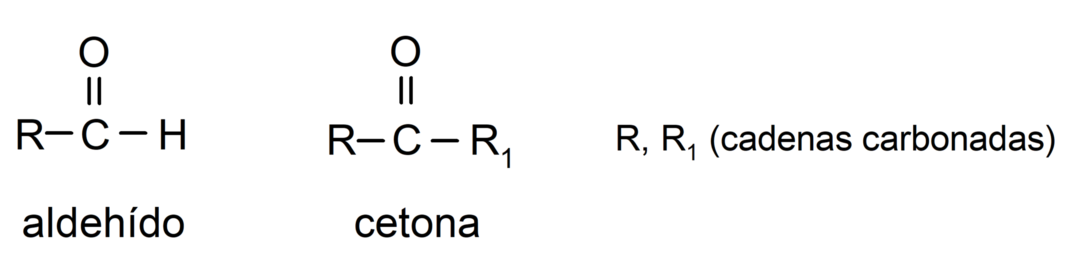
- Aldehyder oxideres ved reaktion med Tollens' reagens og danner metallisk sølv. De oxiderer også mod Benedicts reagens og danner kobber(II)oxid. Ketoner oxideres ikke af nogen af reagenserne.
- Aldehyder reduceres til primære alkoholer, mens ketoner reduceres til sekundære alkoholer.
Fysiske egenskaber
Fysiske egenskaber af aldehyder
De fysiske egenskaber af aldehyder er meget forskellige, fordi de afhænger af sammensætningen af carbonkæden, der er knyttet til carbonylgruppen.
Nogle er:
- De aldehyder, der er mest opløselige i vand, er dem, der er mindre i størrelse, såsom methanal og ethanal.
- Flygtige aldehyder har skarpe og endda irriterende lugte.
- Carbonylgruppen giver dem polaritet.
- De har normalt højere kogepunkter end kemiske forbindelser af lignende molekylstørrelse.
Fysiske egenskaber af ketoner
Ketonernes fysiske egenskaber afhænger af, hvordan carbonkæden, der er knyttet til carbonylgruppen, dannes.
- Mange ketoner har behagelige lugte.
- Dens opløselighed i vand afhænger af størrelsen af carbonkæden knyttet til carbonylgruppen. Jo mindre kulstofkæden er, jo mere opløselig vil ketonen være i vand.
- Carbonylgruppen giver dem en markant polaritet.
- De har ret høje kogepunkter sammenlignet med kemiske forbindelser af sammenlignelig molekylær størrelse.
Kemiske egenskaber
Aldehyders kemiske egenskaber
Blandt de kemiske egenskaber af aldehyder kan vi finde:
De oxideres til dannelse af den tilsvarende carboxylsyre, det vil sige, at den dannede syre vil have det samme antal kulstofatomer i kulstofkæden som aldehyd der gav anledning til det. For eksempel:
- Oxidation med Tollens-reagens (ammoniaksølvkompleks i basisk opløsning, [Ag (NH3)2]+) fra ethanal producerer ethansyre og metallisk sølv.
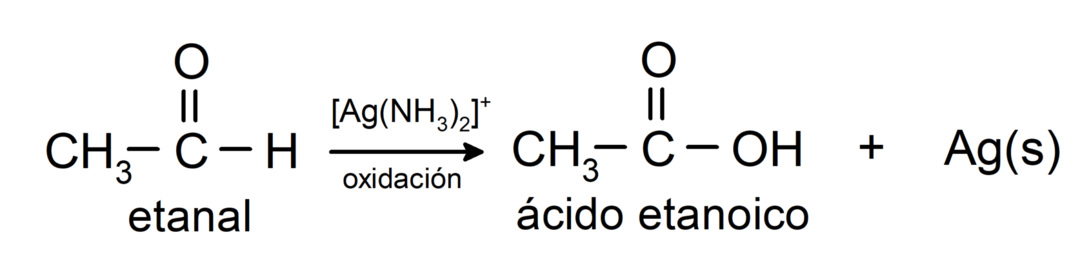
- Oxidation med Benedicts reagens (alkalisk opløsning af kobbersulfat) af ethanal producerer ethansyre og kobber(II)oxid.
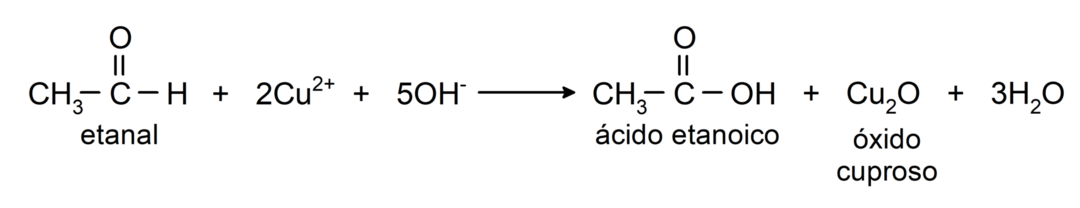
De gennemgår nukleofile additionsreaktionerdet vil sige tilføjelse af en nukleofil til carbonylgruppen. For eksempel:
- Tilsætning af blåsyre for at danne cyanohydriner eller cyanohydriner.
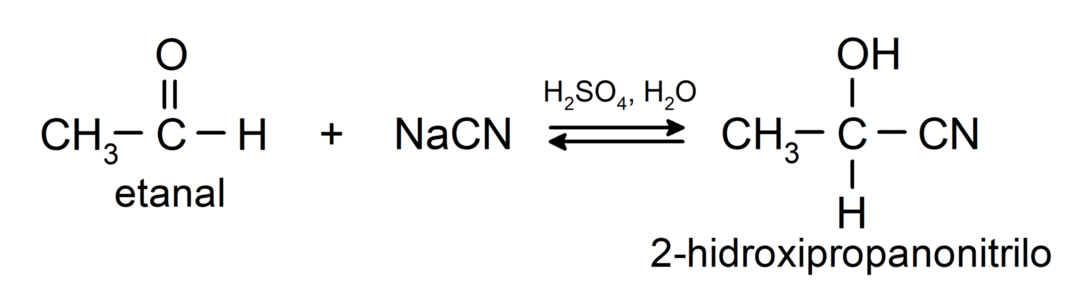
- I nærvær af vandfrie syrer tilsættes alkoholer til carbonylgruppen af aldehyder for at danne acetaler og hemiacetaler.
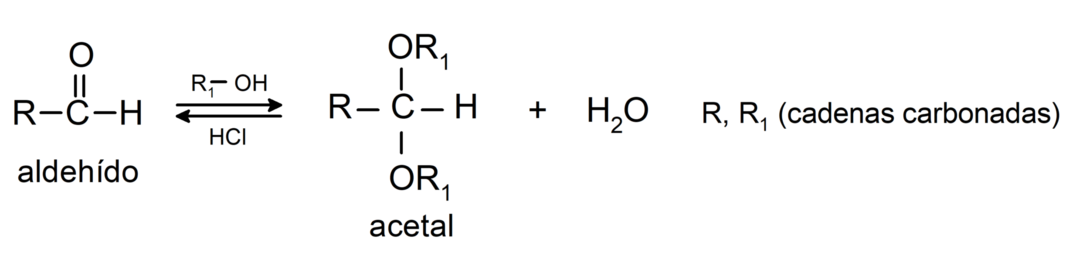
De gennemgår aldolkondensationsreaktioner. I disse reaktioner sker foreningen af to aldehyder i nærvær af natriumhydroxid (NaOH) og kemisk forbindelse resulterende kaldes aldol. For eksempel:
- Kondensationsreaktion af ethanal i nærværelse af fortyndet NaOH.
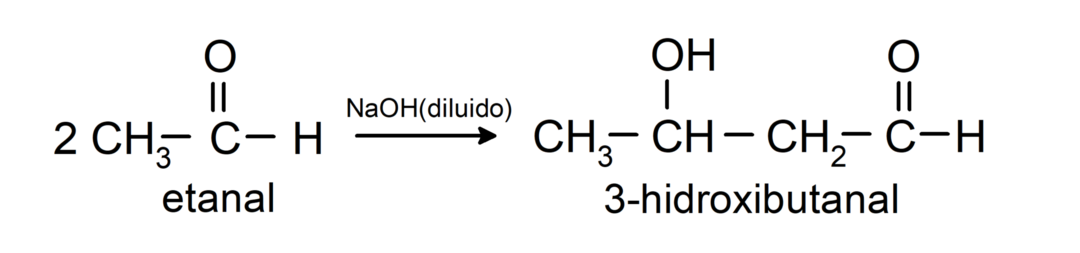
De reduceres til primære alkoholer. Aldehyder kan reduceres til primære alkoholer ved katalytisk hydrogenering eller ved reduktion med natriumborhydrid (NaBH).4) og lithiumaluminiumhydrid (LiAlH4).
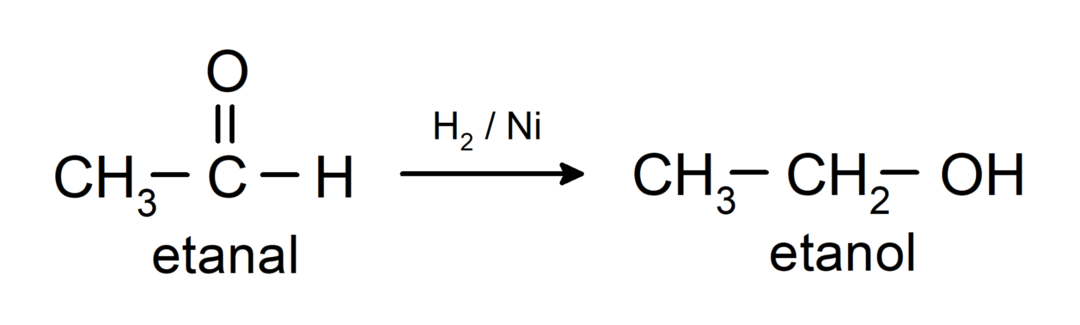
Ketoners kemiske egenskaber
Blandt de kemiske egenskaber af ketoner kan vi finde:
De gennemgår nukleofile additionsreaktioner. For eksempel:
- Tilsætning af blåsyre for at danne cyanohydriner eller cyanohydriner.
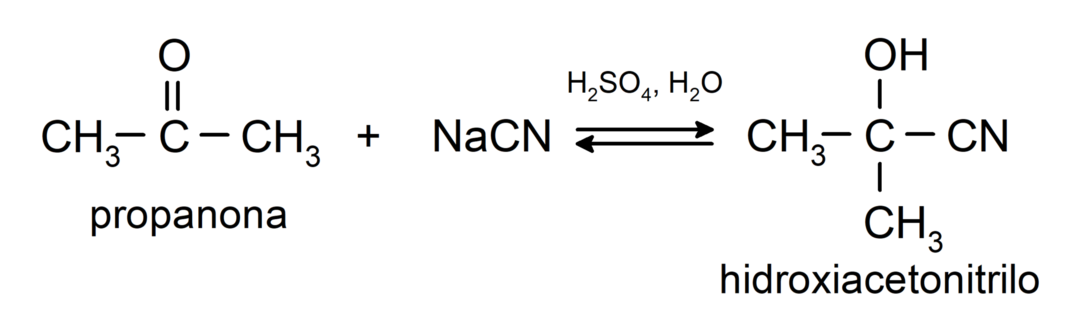
De tilføjer alkoholer (i nærvær af vandfrie syrer) til carbonylgruppen af ketoner for at danne ketaler og hemiketaler. For eksempel:
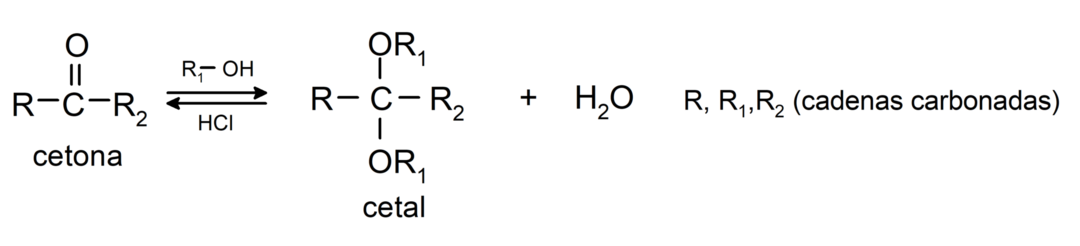
De gennemgår halogeneringsreaktioner. Ketoner, der har et alfa-brinte (α) reagerer ved at erstatte dette hydrogen med halogener (chlor (Cl), brom (Br), jod (I), fluor (F)) i nærværelse af sure eller basiske katalysatorer. Substitution sker næsten udelukkende i kulstof α, altså det kulstof, der har bundet sig til brint α. For eksempel:
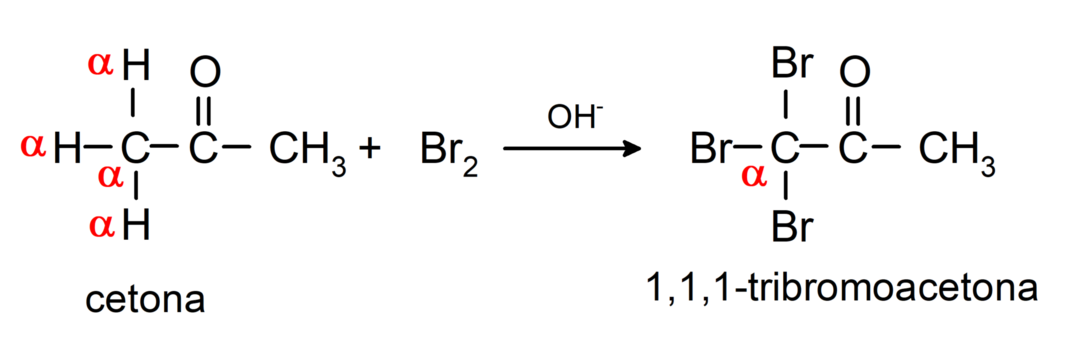
De reduceres til sekundære alkoholer ved katalytisk hydrogenering eller ved reduktion med natriumborhydrid (NaBH4) og lithiumaluminiumhydrid (LiAlH4). For eksempel:
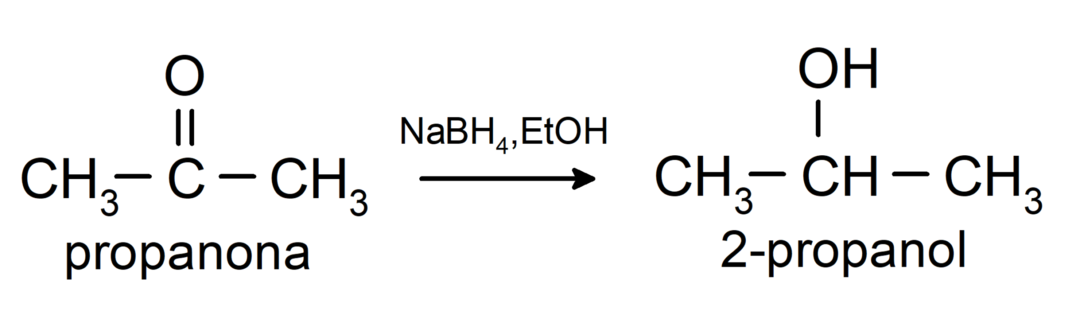
Ketoner oxideres ikke af Tollens og Benedict reagenser.
Nomenklatur for aldehyder
I henhold til reglerne fastsat af International Union of Pure and Applied Chemistry (IUPAC), Aldehyder er navngivet ved hjælp af præfikser, der angiver antallet af kulstof i kæden. kulsyreholdige. Det er ikke nødvendigt at specificere positionen af carbonylgruppen, da den altid er i position et, i den ene ende af molekylet. Derudover er suffikset -al skrevet i slutningen af aldehydnavnet. For eksempel:
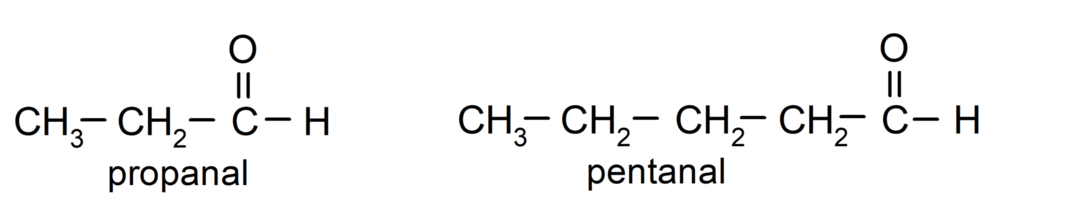
Hvis aldehydet består af flere kulstofkæder, det vil sige at det har forgreninger, vælges kulstofkæden med det største antal kulstofatomer som hovedkæde. De andre kæder er navngivet som substituentgrupper, og hver substituents position er valgt, så den optager det mindst mulige antal i kæden. Derudover begynder carbonatomerne at blive talt fra den ende, der har carbonylgruppen. For eksempel:
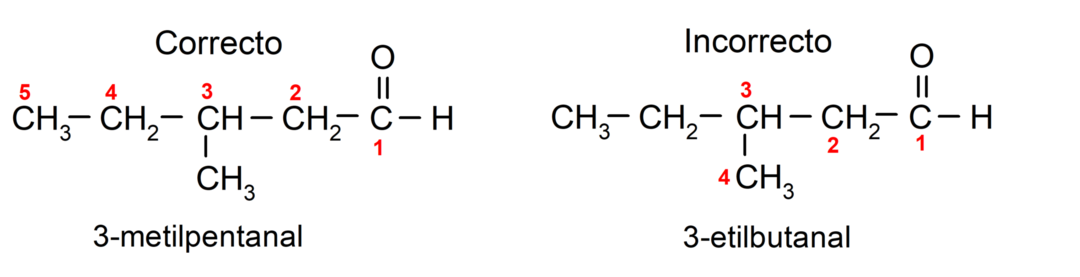
Aldehyder, der har to carbonylgrupper, navngives ved hjælp af suffikset -skiven. For eksempel:
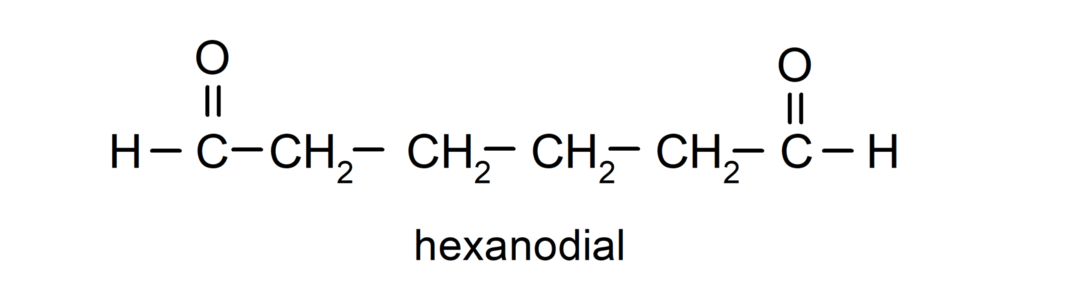
Ketonnomenklatur
Ifølge International Union of Pure and Applied Chemistry (IUPAC) er ketoner navngivet ved hjælp af præfikser, der angiver antallet af kulstoffer i kulstofkæden.
På den anden side er navnet på acetone skrevet ved hjælp af suffikset -en, efterfulgt af et tal, der angiver carbonylgruppens position i carbonkæden. Placeringen af carbonylgruppen bør vælges på en sådan måde, at den svarer til den lavest mulige nummerering. For eksempel:
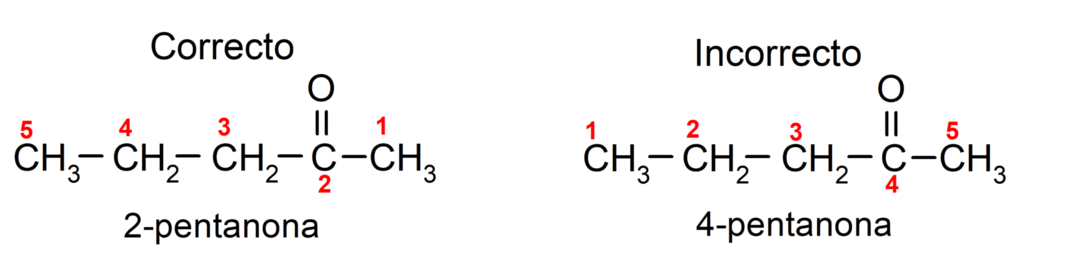
For at nævne en keton, der består af flere kulstofkæder, altså med forgreninger, vælger vi som hovedkæde, kulstofkæden med det største antal kulstofatomer og som indeholder gruppen carbonyl. Resten af kæderne er navngivet som substituentgrupper. For eksempel:
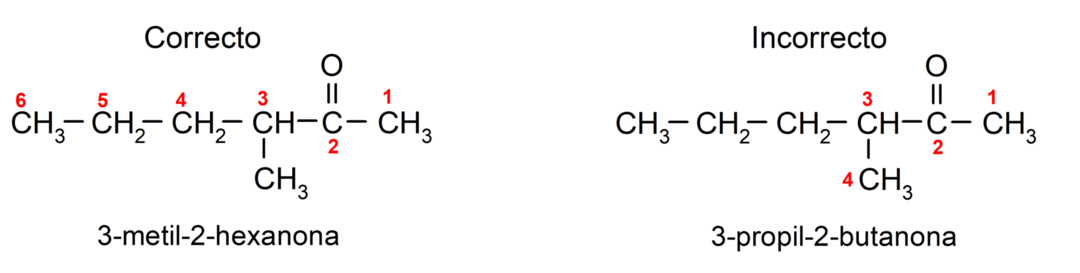
Der er ketoner, der har to carbonylgrupper, de kaldes dioner. For eksempel:
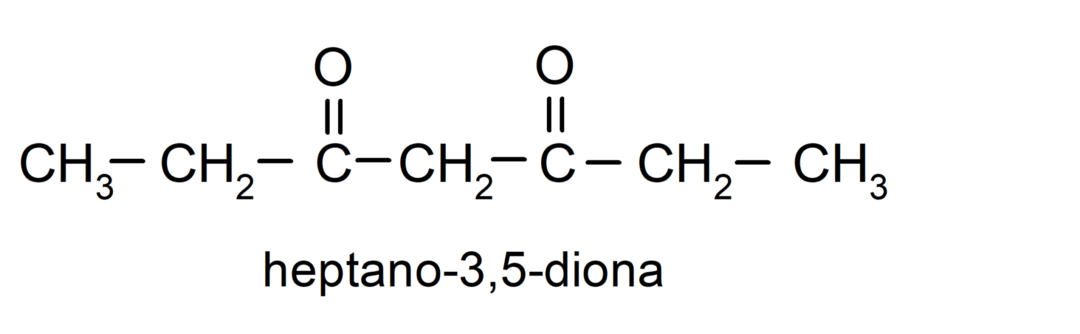
Eksempler på aldehyder
- methanal (formaldehyd)
- ethanal (acetaldehyd)
- propanal (propaldehyd)
- butanal
- pentanal
- hexanal
- 3-bromcyclopentancarbaldehyd
- cyclohexancarbaldehyd
- benzaldehyd
- 4,4-dimethylpentanal
- 2-hydroxy-butanal
- 2-hydroxy-2-methyl-butanal
- 2,3-dimethylpentanal
- pentanedial
- 4-hydroxy-3-methoxybenzaldehyd
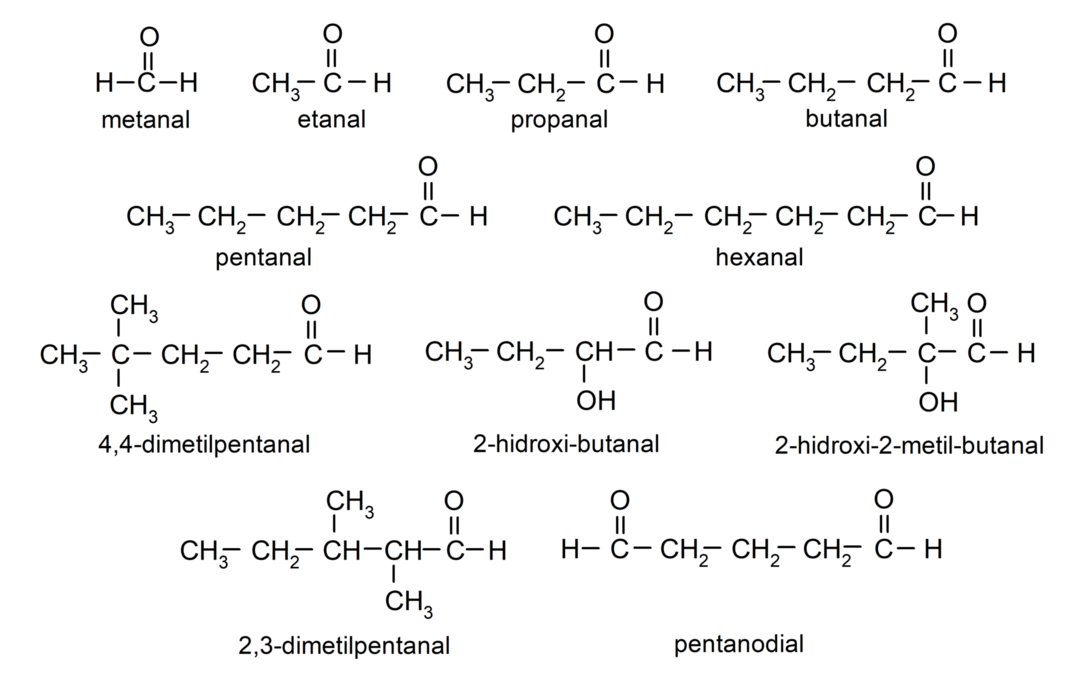
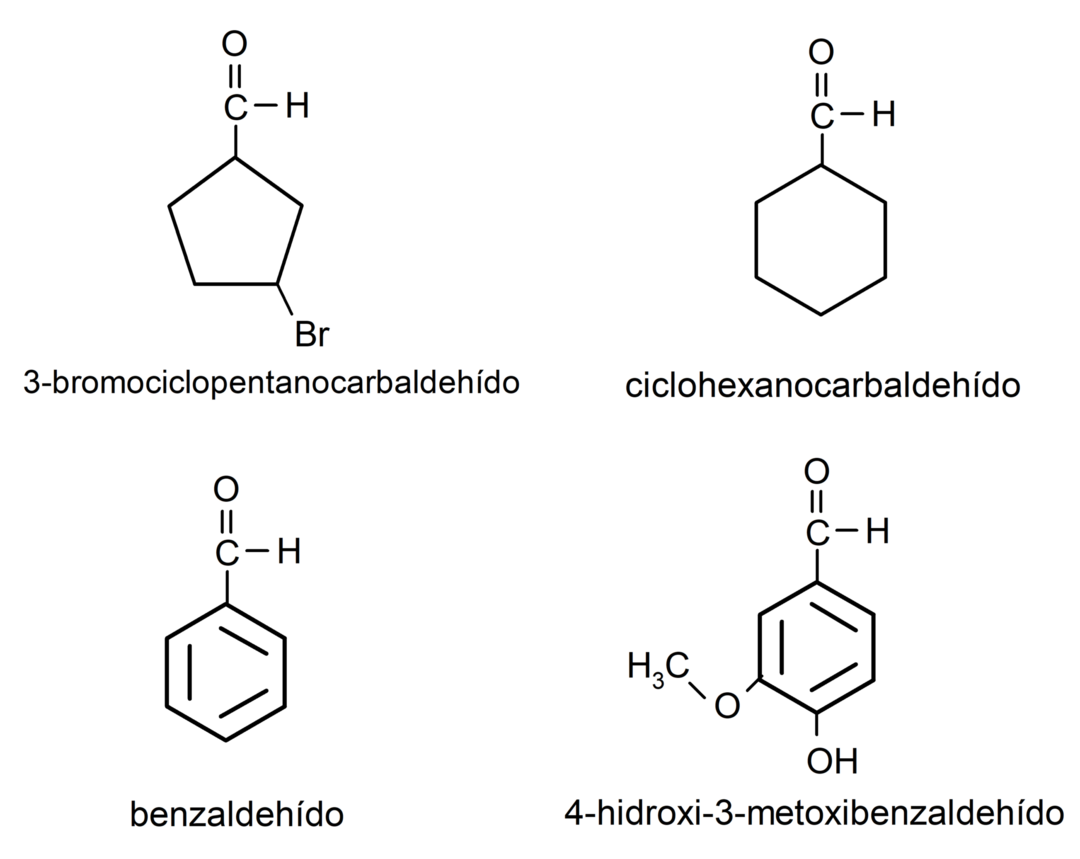
Eksempler på ketoner
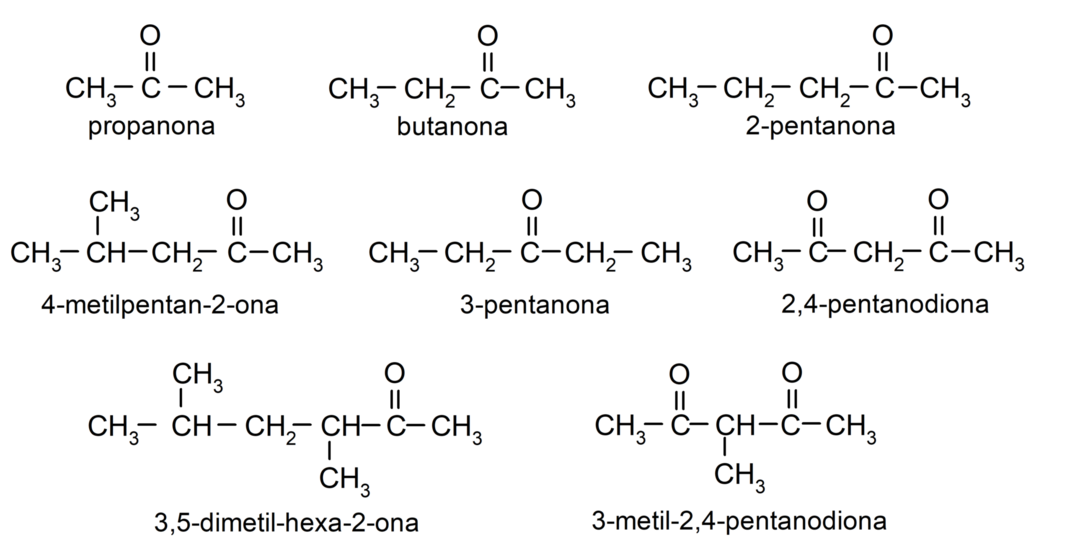
- propanon (acetone)
- butanon
- 2-pentanon
- 4-methylpentan-2-on
- 3-methylcyclohexanon
- cyclohexylmethylketon
- 3,4-dimethyl-hexan-2-on
- ethylphenylketon
- 2,4-pentandion
- cyclohexanon
- 3-pentanon
- 3-methyl-2,4-pentandion
- 1-phenylpropanon
- cyclopentanon
- diphenylketon
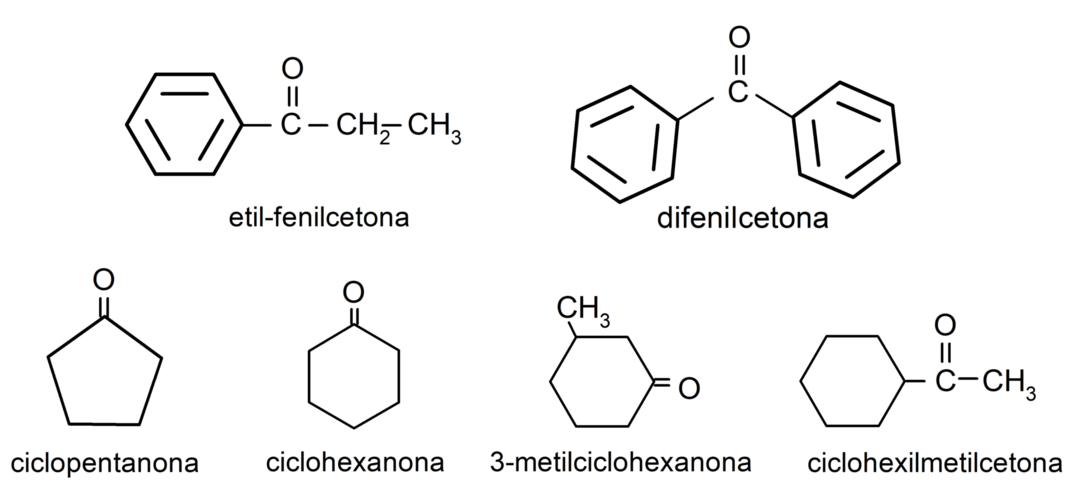
Brug af aldehyder i hverdagen
Nogle anvendelser af aldehyder er:
- De bruges til at fremstille opløsningsmidler, maling, parfume, harpiks og essenser.
- De bruges som konserveringsmidler i kosmetiske produkter, biologiske prøver og lig. Formaldehyd er det mest anvendte til disse formål.
- De bruges til at producere plast, som tillader udskiftning af metaldele i bilindustrien.
- De bruges som smagsstoffer til nogle fødevarer.
- De bruges som desinfektionsmidler.
- De er blevet brugt til at fremstille nogle sprængstoffer, såsom pentaerythritoltetranitrat (TNPE).
Brug af ketoner i dagligdagen
Nogle anvendelser af ketoner er:
- De bruges til fremstilling af opløsningsmidler. Især acetone er meget brugt til at fjerne maling og lakker.
- De bruges til fremstilling af nogle gummier og smøremidler.
- De bruges til at fremstille maling, lakker og lakker.
- De bruges til at fremstille medicin og kosmetik.
Aldehyd og keton toksicitet
- Aldehyderne. Kontakt med aldehyder forårsager irritation af hud, øjne og luftveje. Derudover er eksponering for aldehyder blevet forbundet med sygdomme som cancer, kontaktdermatitis og lever- og neurodegenerative sygdomme. Formaldehyd anses for eksempel af WHO (World Health Organization) for at være en kræftfremkaldende forbindelse.
- ketoner. Gentagen eksponering for ketoner kan forårsage skade på centralnervesystemet. Dette kan føre til hukommelsestab, svaghed, muskelsmerter og kramper. Derudover, hvis huden kommer i kontakt med ketoner, opstår der tørhed og revner. På den anden side, hvis ketoner indåndes, opstår luftvejsirritation og hoste.
Referencer
- Llorens Molina, JA. (2018). “Aldehyder og ketoner: Nogle eksempler.” http://hdl.handle.net/
- Gabriel Pinto Cañón, Manuela Martín Sánchez, José María Hernández Hernández, María Teresa Martín Sánchez (2015) “Tollens-reagenset: fra identifikation af aldehyder til deres anvendelse i nanoteknologi. Historiske aspekter og didaktiske anvendelser."Vol. 111 Nr. 3. Royal Spanish Society of Chemistry.
- William Bauer, Jr. (2000) «Metakrylsyre og derivater»i Ullmanns Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a16_441.
- "De afslører en ny mekanisme for toksicitet i en gruppe af kræftfremkaldende forbindelser afledt af kost og miljø" (2022) I: www.conicet.gov.ar Tilgængelig i: https://www.conicet.gov.ar/ Tilgået: 20. juni 2023.
Følg med:
- Alkoholer
- Sukker
- Alkaner

