30 Eksempler på aldehyder
Eksempler / / November 06, 2023
Det aldehyder er organiske forbindelser som er dannet af en carbonkæde, der har en terminal carbonylgruppe (= C = O) knyttet (placeret i den ene ende af molekyle), som igen er bundet til et hydrogenatom.
Meget almindelige aldehyder er methanal (formaldehyd), ethanal (acetaldehyd) og propanal (propaldehyd).

Nogle af disse forbindelser er til stede i naturen, for eksempel er vanillin eller vanillin et naturligt aldehyd, der udgør hovedaromaen af vanilje.
- Se også: Aldehyder og ketoner
Nomenklatur for aldehyder
Aldehyder kan navngives ved hjælp af nomenklaturreglerne fastsat af International Union of Pure and Applied Chemistry (IUPAC).
For at navngive et aldehyd bruges præfikser, der angiver antallet af carbonatomer, som carbonkæden har knyttet til carbonylgruppen. Carbonylgruppen er altid placeret i den ene ende af carbonkæden, hvilket betyder, at den altid vil have position 1, og det er ikke nødvendigt at angive dens placering i kæden. Derudover er suffikset -al placeret i slutningen af aldehydnavnet. Nogle eksempler er:
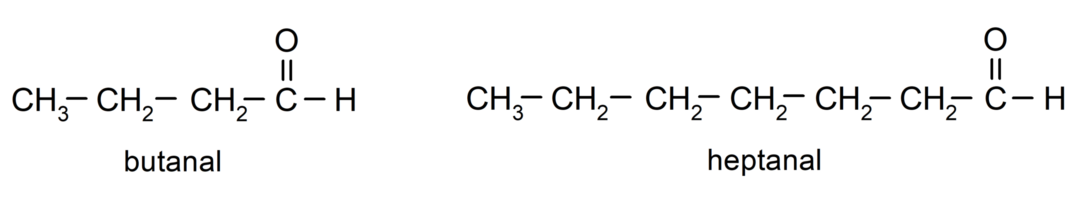
Hvis aldehydet er forgrenet, det vil sige, at det består af flere kulstofkæder, dvs hovedkæde som den kæde, der har det største antal carbonatomer, og som også indeholder gruppen carbonyl. Resten af kæderne er navngivet som substituentgrupper.
Endvidere skal hver substituentgruppe vælges således, at dens position optager den lavest mulige nummerering i hovedcarbonkæden. På den anden side begynder carbonatomerne i hovedkæden at blive talt i den ende, der indeholder carbonylgruppen. Nogle eksempler er:
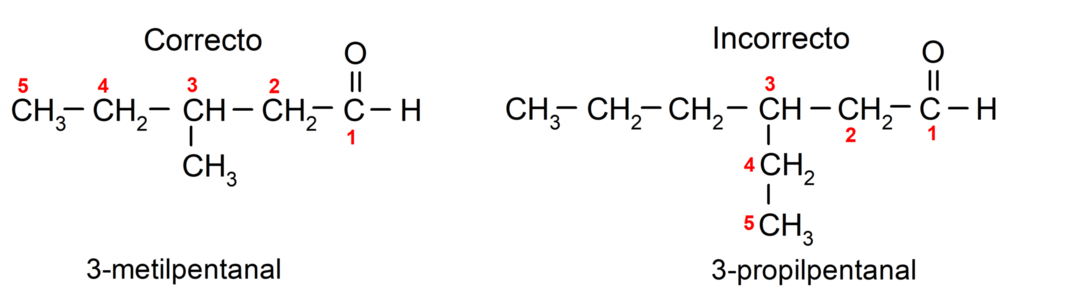
Hvis aldehydet fungerer som en substituent i molekylet, fordi det også består af grupper højere prioriterede funktionaliteter, såsom syrer og estere, så er aldehydgruppen navngivet som -oxo. For eksempel:

Hvis et aldehyd har flere carbonylgrupper, navngives det ved hjælp af præfikser, der angiver antallet af disse grupper, skive (to carbonylgrupper), forsøg (tre carbonylgrupper) osv. For eksempel:
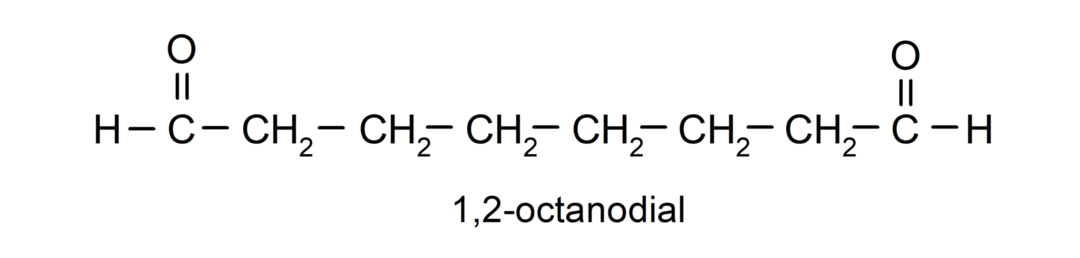
Når carbonylgruppen er knyttet til en cyklus, navngives aldehyder ved hjælp af udtrykket carbaldehyd. For eksempel:

Fysiske egenskaber af aldehyder
Aldehyder har normalt en variation af den samme fysiske egenskab. Dette sker, fordi aldehydernes fysiske egenskaber afhænger af, hvordan carbonkæden, der er knyttet til carbonylgruppen, dannes.
Nogle fysiske egenskaber ved aldehyder er:
- Opløselighed. Vandopløseligheden af aldehyder afhænger af mængden af atomer der har kulstofkæden. Aldehyder med kortere kulstofkæder (op til omkring fem kulstofatomer) er opløselige i vand. Aldehyder med kulstofkæder af mange kulstofatomer er ikke opløselige i vand. Methanal og ethanal er meget opløselige i vand.
- Massefylde. Generelt er aldehyder forbindelser, der er mindre tætte end vand.
- Aggregationsstater. Aldehyder opbygget af et og to carbonatomer er gasser, er dem, der indeholder mellem tre og tolv carbonatomer væsker, og dem, der består af mere end tolv carbonatomer, er faste.
- Lugt. Nogle aldehyder har irriterende lugte, mens andre har behagelige lugte.
- Polaritet. Carbonylgruppen giver dem polaritet.
- Kogepunkt. De har højere kogepunkter end alkaner med tilsvarende molekylvægt, og de har lavere kogepunkter end carboxylsyrer og alkoholer med sammenlignelig molekylvægt.
Aldehyders kemiske egenskaber
Nogle af de kemiske egenskaber ved aldehyder er:
Aldehyder oxideres, når de reagerer med Tollens, Benedict og Fehling reagenser. at danne den tilsvarende carboxylsyre. Den dannede syre vil have det samme antal kulstofatomer i kulstofkæden som det aldehyd, hvorfra den blev dannet. For eksempel:
- Oxidation med Tollens-reagens (ammoniaksølvkompleks i basisk opløsning, [Ag (NH3)2]+). Denne reaktion producerer den tilsvarende syre og metallisk sølv.

- Oxidation med Benedict og Fehling reagens (alkaliske opløsninger af kobber (II) sulfat (CuSO4) med forskellige sammensætninger). Denne reaktion producerer den tilsvarende syre og kobber(II)oxid (Cu2ENTEN).

De gennemgår nukleofile additionsreaktioner, hvor nukleofiler er tilføjet til carbonylgruppen af aldehyder. Nogle eksempler er:
- additionsreaktioner alkoholer til carbonylgruppen af aldehyder for at danne acetaler og hemiacetaler.
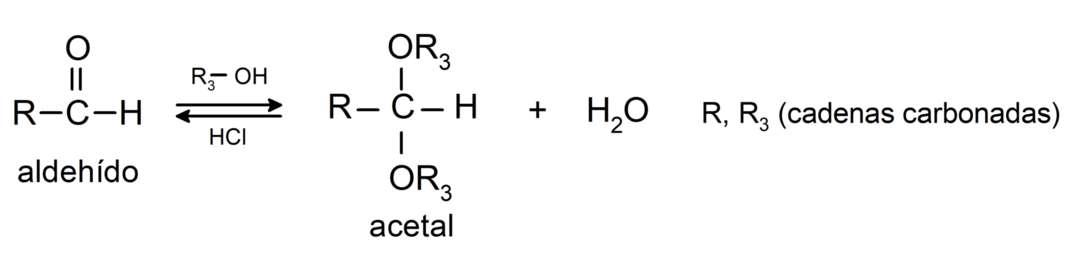
- additionsreaktioner aminer primært til carbonylgruppen.

- Hydrocyanic acid (HCN) additionsreaktioner, hvor cyanohydriner eller cyanohydriner dannes.

De gennemgår aldolkondensationsreaktioner. I denne type reaktion kondenserer to aldehyder for at danne en aldol. De er reaktioner, der opstår med natriumhydroxid (NaOH). For eksempel:
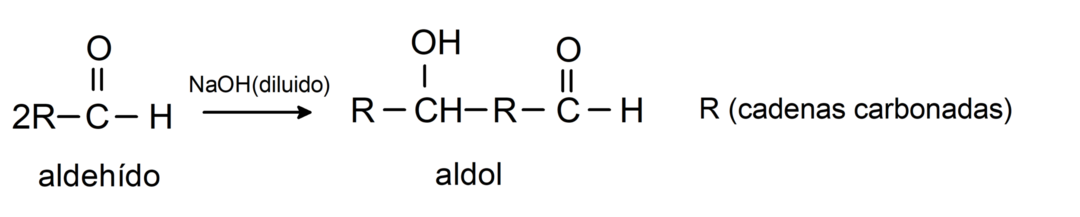
De gennemgår reduktionsreaktioner på primære alkoholer. I nærvær af natriumborhydrid (NaBH4) og lithiumaluminiumhydrid (LiAlH4) eller ved katalytisk hydrogenering reduceres de til primære alkoholer. For eksempel:
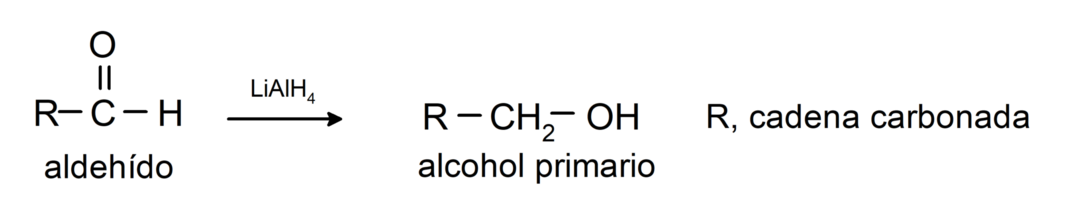
Eksempler på aldehyder
- methanal (formaldehyd)
- ethanal (acetaldehyd)
- propanal (propaldehyd)
- butanal
- pentanal
- vanillin
- kanelaldehyd
- propenal
- benzaldehyd
- hexanal
- 3-bromcyclopentancarbaldehyd
- cyclohexancarbaldehyd
- 4,4-dimethylpentanal
- 2-hydroxy-butanal
- 2-hydroxy-2-methyl-butanal
- 2,3-dimethylpentanal
- pentanedial
- cyclopentancarbaldehyd
- isobutanal
- 2-chlor-butanal

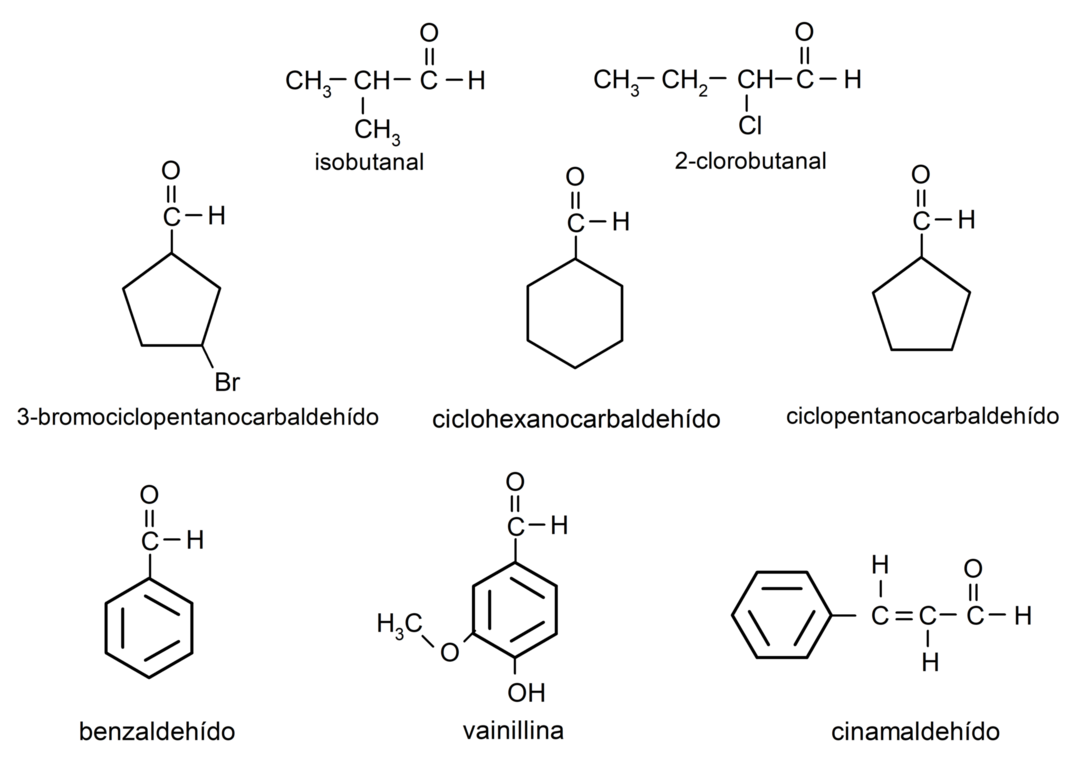
Aldehyder i naturen
Nogle aldehyder til stede i naturen er:
- Benzaldehyd, en bestanddel af mandler.
- Kanelaldehyd, den komponent, der giver kanelessensen dens lugt.
- Vanillin, den komponent, der giver vanilje sin smag.
På den anden side har en af glucoseformerne, den åbne form, en aldehydfunktionel gruppe.
Acetaldehyd, som dannes som et mellemprodukt i omsætningen af alkohol, menes at forårsage tømmermændssymptomer, når det er beruset af alkohol.
Anvendelse af aldehyder
Nogle af de vigtigste anvendelser af aldehyder er:
- De bruges til fremstilling af opløsningsmidler, maling, kosmetiske produkter og essenser.
- De bruges til fremstilling af harpikser. Bakelit er lavet med formaldehyd og er en harpiks, der fungerer meget godt som en elektrisk isolator.
- De er blevet brugt som beroligende midler. Paraldehyd er blevet brugt som et beroligende og hypnotisk middel, selvom det nu er ude af brug på grund af dets ubehagelige lugt.
- De bruges som konserveringsmidler til biologiske prøver og lig. Formaldehyd er meget udbredt i denne forstand.
- De bruges som smagsstoffer til fødevarer. Et eksempel er vanillin, som bruges til at give desserter en vaniljearoma.
- De bruges som desinfektionsmidler.
Farer ved aldehyder
Flere aldehyder er blevet betragtet som kræftfremkaldende, for eksempel er formaldehyd blevet erklæret kræftfremkaldende ifølge WHO (World Health Organization).
Eksponering og kontakt med mange aldehyder forårsager irritation af hud, øjne og luftveje. På den anden side forårsager det kontakteksem og leversygdomme.
Referencer
- Solomons, T.W. Graham og María Cristina Sangines Franchini (1985). “organisk kemi” Mexico, D.F.: Limusa.
- Whitten, K. W., Gailey, K. D., Davis, R. E., de Sandoval, M. T. TIL. O., & Muradás, R. M. g. (1992). “Generel kemi" (s. 108-117). McGraw-Hill.
- Arteaga, P. M. (2017). “Ketoner og aldehyder” Con-Science Scientific Bulletin for Forberedelsesskolen nr. 3, 4(8).
Følg med:
- Sukker
- Hydracider
- Ætanol
- Organiske og uorganiske forbindelser


