Eksempel på peptidbinding
Kemi / / July 04, 2021
Det Peptid Bond er den, hvori to aminosyremolekyler er forbundet med kondens.
For bedre at forstå peptidbindinger skal aminosyrer først defineres:
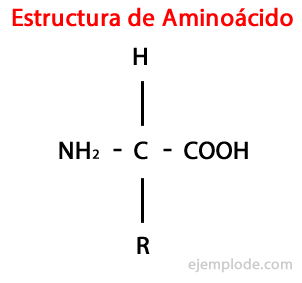
Det Aminosyrer er organiske molekyler kort indeholdende mindst en aminogruppe (-NH2), alkalisk i naturen, og en carboxylgruppe (-COOH), sur i karakter.
Selvom levende væsener til forskellige formål syntetiserer meget forskellige typer aminosyrer, er de vigtigste dem, der er en del af proteiner, som alle hører til klassen for a-aminosyrer.
Α-aminosyrerne er karakteriseret ved at have syre- og aminogrupperne bundet til det samme carbonatom, kaldet α Carbon. Desuden binder dette α-carbon som et tredje substituent et hydrogenatom og som et fjerde substituent, en yderligere gruppe af forskellig størrelse og karakteristika, der adskiller hver aminosyre fra andre.
Den fjerde substituent kaldes Sidekæde Aminosyre og er ofte repræsenteret i forenklet form med bogstavet R.
Da de fire substituenter af α-carbon er forskellige og anvender et tetraedrisk arrangement omkring det, er de tilstedeværende a-aminosyrer
optisk isomerisme, hvilket er når et molekyle har en alternativ form der ligner en spejlbillede hans, som i sidste ende ikke er et lige molekyle. Disse to isomere former af molekylet tildeles bogstaverne D eller L, afhængigt af hvordan substituenterne er arrangeret i rummet. Alle aminosyrerne i proteiner er L.Aminosyrer klassificeres i henhold til deres kemiske karakter Polar og Apolar. Polarerne er igen opdelt i Neutral og opladet (som kan være sure eller basiske). Det Ikke-polær kan være alifatisk eller aromatisk.
Peptider og peptidbindingen
Peptider er produktet af den kovalente forening af aminosyrer gennem amidbindinger og dannes ved kondensering af Carboxyl-enden af den ene og aminoenden af den anden, frigivelse af et vandmolekyle i reaktion. Denne union kaldes Peptide Bond.
Mekanismen for denne reaktion er vist nedenfor, hvori Amino- og carboxylgrupper, og kondensering af aminosyremolekylerne forekommer til dannelse af peptidet.
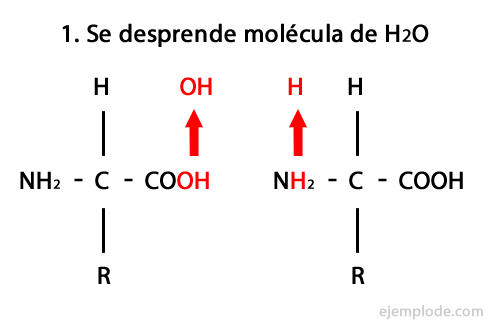
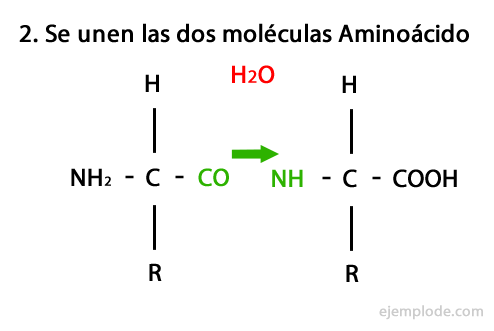

Peptider, som aminosyrer og proteiner, har en aminogruppe og en carboxylgruppe ved deres ender uden at reagere.
For at specificere formlen for et simpelt peptid og endda et protein er det nok at liste de aminosyrer, der sammensætter det, startende med den med en gratis Amino-gruppeog slutter med den med dens gratis Carboxyl-gruppe.
Nogle peptider, der findes i kroppen, er Vasopressin, hvilket hæver blodtrykket og øger vandabsorptionen i nyrerne; det Enkephalin, hvilket reducerer følelsen af smerte; og Oxytocin, som får livmoderen til at trække sig sammen.
Peptidbindingsegenskaber
Kondensationen af aminogruppen i en aminosyre med carboxylen i en anden, finder sted i vandigt opløsningsmiddel, så det det er ikke spontantog derfor kræver proteinsyntese en tilførsel af energi.
Peptidbindingen, som i enhver amidbinding, præsenterer resonans mellem to ekstreme former: den neutrale form, med en enkeltbinding, der forbinder carbonylcarbonet i den første aminosyre og aminonitrogenet i den anden (C-N), og formularen med adskillelse af afgifter hvor de to atomer er forbundet med en dobbeltbinding (C = N). I virkeligheden antager peptidbindingen ikke nogen af de to ekstreme situationer, men er en resonanshybrid af begge.
Der er opkaldet Peptidplan, bestående af alle atomer involveret i peptidbindingen, som forbinder de to indledende aminosyrer. På den ene side nitrogenerne og hydrogenatomer med deres respektive kulstof α i den første aminosyre. På den anden side Carbon α fra den anden aminosyre med ilt og kulstof i Carbonyl-gruppen.
Forskelle mellem peptider og proteiner
Det peptider har et lavt antal aminosyrer, der spænder fra to til et par dusin af dem, og deres konformation i løsning bliver fleksibel.
Det små proteiner, strukturelt tæt på store peptider, har en defineret konformation og meget mindre fleksibel.
Der er proteiner, der ligesom peptider har en uordnet og fleksibel konformation, men den rækkefølge, når de interagerer med andre makromolekyler i cellen.
20 eksempler på aminosyrer, der deltager i peptidbinding
- Blåregn
- Til pigen
- Valine
- Leucin
- Isoleucin
- Proline
- Methionin
- Phenylalanin
- Tyrosin
- Tryptofan
- Serine
- Threonine
- Cystein
- Asparagine
- Glutamin
- Asparaginsyre
- Glutaminsyre
- Lysin
- Arginin
- Histidin