Eksempel på kemisk energi
Kemi / / July 04, 2021
Det Kemisk energi er den, der kommer fra kemiske reaktioner. Samspillet mellem kemiske arter genererer brud og / eller dannelse af bindinger, hvilket indebærer henholdsvis frigivelse eller absorption af energi. Kemisk energi kaldes frigivet energi, som f.eks. Kan bruges som termisk energi og elektrisk energi.
Energi i kemiske reaktioner
Kemisk energi kan opnås i dets maksimale ekspression fra to hovedkilder: Forbrænding og elektrolytiske løsninger. På den anden side er det på niveau med den menneskelige krop muligt at opnå energi gennem kemisk opløsning af mad.
Forbrændingsenergi
For eksempel når brændstofmetan CH4, det enkleste carbonhydrid, begynder at brænde i nærvær af oxygenoxidatoren, det vil gå i opløsning og danne kuldioxid-CO-produkter.2 og vand H2ELLER. Derudover frigør bruddet på hydrogenatomernes bindinger med kulstofatomer energi i form af varme.
CH4 (g) + 202 (g) → CO2 (g) + 2H2 O (l) ∆H = -212,8 Kcal / mol
Metanforbrændingsligning. Varmen fra denne reaktion er repræsenteret af ΔH. Det negative tegn angiver frigivelse af energi. Reaktionen er eksoterm.
 Forbrænding af metangas. Reaktionen manifesteres med en flamme.
Forbrænding af metangas. Reaktionen manifesteres med en flamme.
Eksempler på opvarmning ved forbrænding af organiske forbindelser ved 25 ° C.
Forbindelse |
Formel |
ΔH (Kcal / mol) |
Metan (g) |
CH4 |
-212.80 |
Ethan (g) |
C2H6 |
-372.82 |
Propan (g) |
C3H8 |
-530.60 |
n-butan (g) |
C4H10 |
-687.98 |
n-pentan (g) |
C5H12 |
-845.16 |
Ethylen (g) |
C2H4 |
-337.23 |
Acetylen (g) |
C2H2 |
-310.62 |
Benzen (g) |
C6H6 |
-787.20 |
Benzen (l) |
C6H6 |
-780.98 |
Toluen (l) |
C7H8 |
-934.50 |
Naphthalen (e) |
C10H8 |
-1,228.18 |
Saccharose (r) |
C12H22ELLER11 |
-1,348.90 |
Methanol (l) |
CH3Åh |
-173.67 |
Ethanol (l) |
C2H5Åh |
-326.70 |
Eddikesyre (l) |
CH3COOH |
-208.34 |
Benzoesyre (r) |
C6H5COOH |
-771.20 |
For at et brændstof kan levere al den forbrændingsvarme, det er i stand til, skal det være i gasform. Som anført i tabellen tilvejebringer flydende benzen en forbrændingsvarme, der er 6,22 Kcal / mol mindre end den, der frigives af gasformigt benzen. Dette betyder, at der skal investeres 6,22 Kcal / mol for at skifte fra væske til gas.
Klik for at få flere oplysninger om Brændstoffer.
Elektrolytiske løsninger Energi
En elektrolytisk leder er et medium, hvor en eller flere ioniske arter er involveret, hvilket er spredt med sin elektriske ladning, hvilket muliggør passage af en elektrisk strøm gennem dens Forfatning. Elektrolytiske løsninger er elektrolytiske ledere.
Elektrolytiske ledere inkluderer ud over elektrolytopløsninger også Smeltede salte og også nogle faste salte, såsom natriumchlorid NaCl og sølvnitrat AgNO3.
Overførslen af elektroner sker ved ionisk migration, positiv og negativ, mod elektroderne. Denne migration involverer ikke kun en overførsel af elektricitet, men også transport af materie fra en del af lederen til en anden.
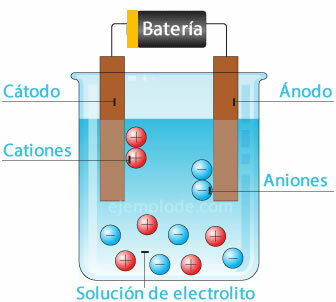 Elektrokemisk celle
Elektrokemisk celle
Tilslutning af en potentiel kilde til de metalliske elektroder (katode og anode) og nedsænkning af disse i en Vandig opløsning, elektronerne vil rejse gennem anoden for at flygte fra opløsningen til den positive pol i springvand. Dette er for eksempel tilfældet med en chlorion, der frigøres fra sin elektron, og som allerede er neutral, forbinder den et andet kloratom for at danne det diatomiske molekyle. Klorgas vil undslippe fra opløsningen.
2Cl- = 2Cl + 2e-
Elektroner, der forlader kildens negative pol, vil blive anbragt i den nedsænkede katode. Arterne til stede i den vandige opløsning (ioner) tager elektronerne fra katoden. For eksempel tog de brintioner, der udgør vand, efter at have været i en positiv ladning en elektron, der skal neutraliseres, og forbindes med et andet hydrogenatom for at danne molekylet diatomisk. Det vil undslippe som brintgas fra opløsningen.
2H+ + 2e- = 2H
2H = H2 (g)
Denne udveksling af elektroner kan understøtte driften af bilbatterier, som består af bly-Pb-elektroder nedsænket i en opløsning af svovlsyre H2SW4.
Den samme energi opnås i alle typer batterier, der håndteres på hjemmemarkedet: 9V, AA, AAA, D for at nævne nogle få eksempler.
Fødevareenergi
Mennesker assimilerer den energi, der frigøres ved at nedbryde den mad, vi spiser i vores krop. Den energi er, hvad vores krop bruger til ikke-bevidste funktioner (fordøjelse, hjerterytme, cellulære funktioner) og dem, vi udfører.
Så længe du ikke har intens fysisk aktivitet, og dit stofskifte er langsomt, anbefales det at have et regelmæssigt kalorieindtag, fordi mad med højt indhold af Komplekse lipider og kulhydrater, som har meget store strukturer, er sværere at nedbryde, hvilket resulterer i en vending af Energi. I så fald ville effekten være et øjeblik modsat.
Det tilrådes at indtage frugt, når du skal arbejde om natten, fordi frugten indeholder fruktose, et simpelt kulhydrat, der er let at nedbryde og vil have energi til rådighed for os efter din forbrug.
Kemisk energi og dens transformationer
Termoelektriske anlæg
Tunge brændstoffer bruges i termoelektriske kraftværker for at have en høj og langvarig brændværdi. Generelt er det brændselsolie (brændselsolie). Forbrænding, som er det kemiske trin i processen, vil tjene som et opvarmningsmiddel for en kedel, som vil generere mættet damp. Denne damp kommer ud under tryk gennem dampdistributionsnetværket og begynder at flytte generatorturbinerne. Disse enheder producerer elektrisk energi for at levere den tilsvarende befolkning.
Kemisk energi → Mekanisk energi → Elektrisk energi
Drift af biler
Biler er afhængige af en strømkilde, som er batteriet. I batteriet er der allerede kendt, at der forekommer elektrolytisk ledning, som driver tændingssystemet, instrumentbrættilbehør og ekstra strømudtag. Takket være denne tilgængelige elektricitet vil bilen være i stand til at flytte for at føre føreren til det ønskede sted.
Kemisk energi → Elektrisk energi → Mekanisk energi
