Lanthanide egenskaber
Kemi / / July 04, 2021
Lanthanider er de kemiske grundstoffer, der spænder fra Lanthanum til Lutetium. De har fælles karakteristika, for hvilke de er klassificeret i en særlig kategori nederst i det periodiske system.
Hovedtræk ved lanthanider:
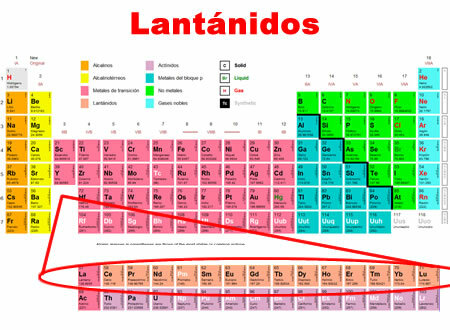
- De er placeret i periode 6 i det periodiske system.
- De dækker 15 elementer fra 57 til 71.
- De deler strukturen af Lanthanum, hvortil der tilføjes et energiniveau f, som er mindre kemisk reaktivt.
- De blev kaldt sjældne jordarter, fordi de i en naturlig tilstand altid kombineres til dannelse af oxider.
- Nogle er relativt rigelige.
- Selvom de har variable valenser, har de fleste valenser +3.
- Når dets atomnummer stiger, falder dets radius.
- De har alle et skinnende metallisk look.
Individuelle egenskaber ved lanthanider:
Lanthanum (La).
- Atomnummer 57
- Atomvægt: 139
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 920 ° C
- Kogepunkt: 3457 ° C
Det blev opdaget i 1839. I industrien bruges det i legeringer med andre lanthanider til fremstilling af lettere sten; i optik bruges det til optiske briller. Det bruges også til brintsvampe, der bruges til at indeholde gasser. I medicin bruges det i form af lanthancarbonat til behandling af nyresvigt, da det har en affinitet til at blande sig med phostates, hvilket reducerer hyperphosphemia.
Cerium (Ce)
- Atomnummer 58
- Atomvægt: 140
- Tilstand: Blødt fast stof
- Udseende: Metallisk, sølvgrå, jernlignende
- Valencias: +3, +4
- Smeltepunkt: 798 ° C
- Kogepunkt: 3426 ° C
Det blev opdaget i 1803. Det er den mest rigelige lanthanid. Det bruges til at fremstille katalysatorer, hovedsageligt til biler (katalysatorer) og til olie krakning. I oxidform bruges det til at polere briller og linser. Selvom det ikke har nogen kendte biologiske funktioner, bruges det i medicin i brændesalver.
Praseodymium (Pr)
- Atomnummer 59
- Atomvægt: 144
- Tilstand: Blødt fast stof
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 931 ° C
- Kogepunkt: 3520 ° C
Det blev opdaget i 1841 og isoleret i 1885. I branchen bruges det i legeringer med magnesium til at fremstille flymotorer; Det bruges til at give glas og emaljer en gul farve. Nikkellegeringer har magnetiske egenskaber. Reagerer med halogener til fremstilling af fluorider, chlorider, bromider og iodider.
Neodym (Nd)
- Atomnummer 60
- Atomvægt: 139
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 1024 ° C
- Kogepunkt: 3100 ° C
Det blev opdaget i 1885, da praseodymium blev isoleret; neodym blev isoleret indtil 1925. Det er en af de mest reaktive lanthanider. I industrien bruges det til at farve glas og emaljer. På grund af dets evne til at absorbere lys bruges det i astronomi til at skabe krystaller, hvormed infrarøde spektrometre og filtre er kalibreret. En af dens vigtigste anvendelser er at fremstille magneter med høj magnetisk intensitet. Disse magneter bruges til præcisionsinstrumenter, såsom dem, der bruges i computerharddiske, samt nogle tyndtformede højttalere.
Promethium (Pm)
- Atomnummer 61
- Atomvægt: 145
- Fast tilstand
- Udseende:?
- Valencias: +3
- Smeltepunkt: 1100 ° C
- Kogepunkt: 3000 ° C
Dens eksistens blev forudsagt i 1902, men kunne ikke bevises før 1944. Dette lanthanid findes ikke i naturen, da det er kilden til dets opnåelse og undersøgelse af fission af uran. Når uranfission i en atomreaktor er et af atomerne, der produceres ved denne atomseparation, promethium. Det har radioaktive egenskaber, som giver det fosforescens og bruges til kalibratorer og nukleare batterier, der anvendes i rumfartøjer.
Samarium (Sm)
- Atomnummer 62
- Atomvægt: 150
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 1072 ° C
- Kogepunkt: 1803 ° C
Det blev opdaget i 1853 og isoleret i 1879. Den har flere isotoper, og mindst to af dem er radioaktive. I industrien bruges det i optik til at fremstille krystaller, der absorberer infrarødt lys. Det bruges også som en katalysator til opnåelse af alkohol og som et element i nogle lysstofrør og fjernsyn. Med hensyn til sundhed kan det, hvis det inhaleres (såsom det oxid, der bruges til polering af krystaller), forårsage lungeemboli eller påvirke leveren. Radioaktive isotoper anvendes til strålebehandling af terminalt syge patienter.
Europium (Eu)
- Atomnummer 63
- Atomvægt: 152
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +2, +3
- Smeltepunkt: 826 ° C
- Kogepunkt: 1527 ° C
Det blev opdaget i 1890. Det er den mest reaktive af lanthaniderne. Det er blevet brugt i lysstofrør og fjernsyn, dog til at forårsage lungeemboli, hvis det er tilfældet indåndes eller beskadiger leveren, hvis den akkumuleres i menneskekroppen, har den næsten ingen industrielle anvendelser. I atomforskning bruges det, da det absorberer neutroner.
Gadolinium (Gd)
- Atomnummer 64
- Atomvægt: 157
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 1312 ° C
- Kogepunkt: 3250 ° C
Gadolinium har få anvendelser, hvoraf den vigtigste er magnetisk industriel køling, da det øger sine magnetiske egenskaber ved lave temperaturer; men da denne type kølere kræver brug af arsen, bruges de ikke til huskøling. I medicin bruges det som kontrastmiddel til magnetisk-nuklear resonans.
Terbium (Tb)
- Atomnummer 65
- Atomvægt: 159
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +4
- Smeltepunkt: 1356 ° C
- Kogepunkt: 3230 ° C
Det blev opdaget i 1843 og isoleret i 1905. Det er meget vigtigt i elektronikindustrien, da det er et af de elementer, der bruges til at fremstille halvledere. Andre anvendelser er at fremstille lysstofrør og billedrør. Det bruges også som en katalysator i brændselsceller. Selvom det ikke har biologiske funktioner, har dets indånding eller indtræden i menneskekroppen toksiske virkninger, der hovedsagelig påvirker leveren.
Dysprosium (Dy)
- Atomnummer 66
- Atomvægt: 162,5
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +2, +3
- Smeltepunkt: 1407 ° C
- Kogepunkt: 2567 ° C
Det blev opdaget i 1843 og isoleret i 1905. Det er meget vigtigt i elektronikindustrien, da det er et af de elementer, der bruges til at fremstille halvledere. Andre anvendelser er at fremstille lysstofrør og billedrør. Det bruges også som en katalysator i brændselsceller. Selvom det ikke har biologiske funktioner, har dets indånding eller indtræden i menneskekroppen toksiske virkninger, der hovedsagelig påvirker leveren.
Holmium (Ho)
- Atomnummer 67
- Atomvægt: 166
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 1474 ° C
- Kogepunkt: 2700 ° C
Det blev opdaget i 1878, og dets navn stammer fra byen, hvor det blev opdaget, Stockholm, på latin, Holmia. Det har næsten ingen praktiske anvendelser; det bruges dog i nogle industrier som en katalysator for kemiske reaktioner såvel som til nogle elektroniske komponenter. Det bruges også til at ændre laserstrålens frekvens og intensitet.
Erbium (Er)
- Atomnummer 68
- Atomvægt: 167
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 1795 ° C
- Kogepunkt: 2863 ° C
Det blev opdaget i 1843. Det bruges i atomindustrien som en neutronbuffer. I oxidform er det et farvestof til krystaller, hvilket giver dem en lyserød nuance; Disse krystaller bruges i optik og smykker. Det bruges også til at fremstille fiberoptik.
Thulium (Tm)
- Atomnummer 69
- Atomvægt: 167
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 1545 ° C
- Kogepunkt: 1947 ° C
Det blev opdaget i 1879. På trods af dets lave tilgængelighed på grund af dets radioaktive egenskaber er dens vigtigste anvendelse som en røntgenkilde i bærbart udstyr og til solid state-lasere.
Ytterbium (Yb)
- Atomnummer 70
- Atomvægt: 173
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 824 ° C
- Kogepunkt: 1194 ° C
Det blev opdaget i 1878 og isoleret i 1907. Radioaktive isotoper bruges til bærbart røntgenudstyr, der fungerer uden elektricitet. Det bruges også til at forbedre stållegeringer og øge deres modstand, et kendetegn, der anvendes i tandpleje på grund af forbedring af ståls mekaniske egenskaber. Det skal håndteres med forsigtighed, da det kan forårsage irritation og forbrændinger. Når det reagerer med luft, kan det også forårsage eksplosion eller brand.
Lutetium (Lu)
- Atomnummer 71
- Atomvægt: 175
- Fast tilstand
- Udseende: Metallisk, sølvhvid
- Valencias: +3
- Smeltepunkt: 1652 ° C
- Kogepunkt: 3402 ° C
Det blev opdaget i 1907. Det er det mindst forekommende kemiske element i jordskorpen. På trods af dets lave tilgængelighed bruges det til olieraffinering og som en katalysator for organiske kemiske reaktioner. Nogle radioaktive isotoper er også blevet testet for behandling med strålebehandling.