Eksempel på overfladespænding
Fysik / / July 04, 2021
Det Overfladespænding er den kraft, der udøves på overfladen af en væske, der er i ro, for at modvirke vægten af en let genstand, der hviler på den. Desuden kan overfladespændingen defineres som Kraft udøvet af en væske til at modstå at blive brudt på overfladen. Det er den vigtigste egenskab, der holder sæbebobler, konsistente og faste.
Væsker har som en af deres vigtigste egenskaber et fast volumen, hvis form vil variere alt efter beholderen, der indeholder dem. Væsker tilpasser sig beholderens form og optager altid den laveste del af den ved tyngdekraften. På denne måde efterlader de en fri overflade, ikke helt flad, eller antager specielle former som dråber, bobler eller bobler.
Der er så Overfladestyrker, opkald Samhørighed og vedhæftning, som forklares nedenfor:
Samhørighed: Det er når to forskellige flydende overflader påvirkes af en tiltrækningskraft til hinanden, som aktiveres i de yderste molekyler.
Tiltrædelse: Det er når en væske inkorporeres ved tiltrækning til overfladen af et fast stof, der diffunderer i dette område.
Disse to Overfladekræfter er ansvarlige for forskellige biologiske fænomener, baseret på begreberne Surface Tension and Capillarity.
Overfladespænding
I en væske er hvert molekyle omgivet af flere molekyler; på denne måde kompenseres tiltrækningen i alle retninger på hvert punkt af væsken undtagen på overfladen, hvor der ikke er nogen molekyler over, men kun luft kræfter ledes ind i væskenog genererer således en nettotiltrækning mod dette indhold.
Væsken har derefter tendens til at skabe sammenhæng, hvilket er det samme som ikke at dispergere, og minimere overfladen og danne dråber. Væskens overflade vil have en film der tilbyder modstandsdygtighed over for dens deformation, og derfor modstand mod brud.
For at måle denne samhørighedskraft overvejes en trådkonstruktion med en glidende side, hvori et lag af væske placeres. En simpel sammenligning af denne struktur er med en sæbebobleblæsningsring, hvor du kan glide ledningen lidt for at gøre ringen større.
Det væske vil forsøge at minimere overfladen, betegnet af S, der udøver en kraft F på den glidende side, som kan måles. Det konkluderes, at beregningen af styrken forbliver:
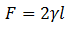
Hvor γ er overfladespændingen, og l er længden på kablet, der glider.
Det Overfladespænding γ er en væskes egenskab. Kraften F afhænger af l, længden på glidekablet, men ikke af overfladen S. Faktoren 2 introduceres, fordi der er to overflader, som er den indvendige og den udvendige af glidetråden, som er i kontakt med væsken.
Det Overfladespænding γ er kraften pr. Længdeenhed, der udøves af en overflade af en væske på en hvilken som helst linje, der er placeret på den som en fastspændingskant.
Kraften, der stammer fra overfladespændingen er vinkelret på overfladelinjen og tangent til den.
Overfladespændingen γ kan også defineres som Energi pr. Enhedsareal der er nødvendigt for at øge et areal og udtrykkes med følgende formel:
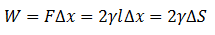
Da der kræves energi til dannelse af en overflade, har væsker tendens til at reducere deres eksponerede areal i forhold til omgivelserne. Det er for denne sags skyld, at overfladerne på vandområder som søer, have og oceaner i en rolig tilstand er flade.
Overfladespænding måles i Newton hver meter (N / m)og for hvert stof falder det med stigende temperatur. Vandets er større end i de fleste væsker og skyldes også, at det er en af de tætteste væsker med 1 g / cm3 massefylde.
Nedenfor er en tabel med værdierne for nogle stoffer, der er typiske for en række temperaturer.
Væske |
T (° C) |
γ (N / m) |
Helium |
-270 |
0.0002 |
Brint |
-255 |
0.002 |
Neon |
-247 |
0.005 |
Ilt |
-193 |
0.016 |
Ethanol |
20 |
0.022 |
Sæbevand |
20 |
0.025 |
Vand |
100 |
0.059 |
Vand |
60 |
0.062 |
Vand |
20 |
0.073 |
Vand |
0 |
0.076 |
Kviksølv |
20 |
0.465 |
Sølv |
970 |
0.800 |
Surfaktanter eller overfladeaktive stoffer
Nogle gange er det nødvendigt at reducere overfladespændingen af en væske. Opnås opløsning af stofferne kaldet overfladeaktive stoffer eller overfladeaktive stoffer, som danner en overfladefilm, hvis molekyler næppe tiltrækkes af molekylerne i den indre væske.
Takket være overfladeaktive stoffer er det lettere for den pågældende væske at blive våd.
Eksempler på overfladespænding
Myggen, der lander på vandet, forbliver ophængt på overfladen.

En isopor eller isoporplade ophængt i vand.

Det vandark, der dannes på ringen, inden der sprænges en sæbeboble.

De letteste sand- eller støvpartikler forbliver ophængt på vandoverfladen, hvis de ikke omrøres.

Når der er vand og olie i et glas, er der overfladespænding i adskillelsen mellem de to efter densitet.

Når en aromatiseret drik rystes meget, forbliver de dannede bobler på overfladen, hver enkelt involveret i den samlede overfladespænding.

Skummet af sæbevand ved betjening af en vaskemaskine har bobler og bobler, der dannes inden skylning.

Skibe drager fordel af denne egenskab af vand for at holde sig flydende takket være det faktum, at de fører luft indeni. De er som en flydende boble på overfladen af vandet.

Surfbrætter skaber overfladespænding, når vandet er i ro, og når der er bevægelse, holder de fast.

Når rå mælk koges, begynder dannelsen af en creme, som konsolideres, når mælken køler af. Det er et tykt lag fedt oven på den flydende del.

Glem ikke at efterlade dine kommentarer.