Begriff in Definition ABC
Verschiedenes / / April 22, 2022
Begriffsdefinition
Azeotrope sind Gemische chemischer Verbindungen definierter Zusammensetzung, die bei bestimmten Temperaturen sieden. Das grundlegende Merkmal ist, dass sich das Gemisch verhält, als wäre es ein einziger reiner Stoff, wobei seine Eigenschaften erhalten bleiben und eine einfache Handhabung ermöglicht wird.

Chemieingenieur
Die Mischung kann aus zwei oder mehr Komponenten bestehen und sein Komposition es ist sowohl in der Flüssigphase als auch in der Gasphase gleich, dies erzeugt Ähnlichkeiten mit reinen Substanzen. Daraus ist leicht abzuleiten, dass dieses Gemisch nicht durch Verfahren wie z. B. in seine Bestandteile getrennt werden kann fraktionierte Destillationen, da es, wie oben erwähnt, seine Proportionen behält und sich so verhält, als wäre es eine einzige Komponente.
Ein weiteres Merkmal ist, dass der Siedepunkt dieser Mischung höher, niedriger oder sogar gleich dem einer ihrer Komponenten sein kann. Siedet das Azeotrop bei a Temperatur
Bei maximaler Siedetemperatur wird es als maximales Azeotrop bezeichnet, und wenn es dies bei der niedrigstmöglichen Temperatur tut, ist es als minimales Azeotrop bekannt. Das heißt, das minimale Azeotrop hat einen niedrigeren Siedepunkt als seine reinen Bestandteile und umgekehrt das maximale Azeotrop. Beispielsweise ist in der Mischung Methanol - Benzol das Azeotrop minimal (0,61 Benzol - 0,39 Methanol in Fraktionen molar) mit einem Siedepunkt von 58 °C in einem Tank, in dem der Siedepunkt von Benzol 80 °C und der von Methanol beträgt 65 °CMinimale und maximale Azeotrope
Nun… woher kommt ein Azeotrop? Bei einer Abweichung von der Gesetz Raoult, das heißt, der Dampfdruck des azeotropen Gemisches steht nicht in direktem Zusammenhang mit seinem Molenbruch, sondern wenn der Begriff des azeotropen Gemisches entsteht. Diese Abweichungen treten auf, wenn sich die Komponenten stark anziehen oder abstoßen, das heißt, die zwischenmolekularen Kräfte in verschiedenen Verbindungen sehr unterschiedlich sind.
Wenn die Abweichung positiv ist, haben wir das minimale Azeotrop, während wir bei negativer Abweichung das maximale Azeotrop haben. Um dieses Konzept besser zu verstehen, schauen wir uns einige Grafiken an:
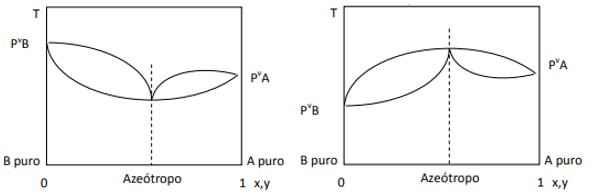
Hier beobachten wir, dass bei einer idealen Mischung nach dem Gesetz von Raoult die Dampfdrücke der reinen Komponenten durch eine gerade Linie verbunden werden sollten, da Nun, es gibt eine Abweichung von diesem Gesetz, die die Bildung von minimalen und maximalen Azeotropen verursacht, je nachdem, ob zwischen ihnen eine größere oder geringere Affinität besteht Komponenten. Wenn die Abweichung vom Gesetz von Raoult negativ ist, wie in der Abbildung links, ist sie minimal bei Diagramm des Drucks, aber ein Maximum im Temperaturdiagramm (daher Azeotrop des Maximums). Wenn andererseits die Abweichung positiv zum Gesetz von Raoult ist, wird sie ein Maximum im Druck vs. Zusammensetzung, aber ein Minimum im Diagramm Temperatur vs. Zusammensetzung (hier haben wir ein minimales Azeotrop). Verwechseln Sie nicht die Diagramme Druck vs. Zusammensetzung und Temperatur vs. Komposition.
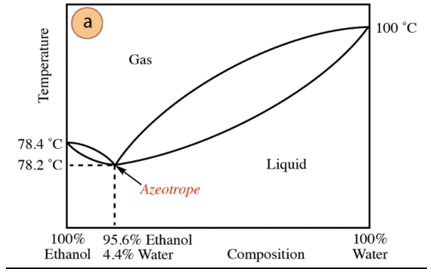
Bei der Ethanol-Wasser-Mischung liegt ein Minimalazeotrop vor, dessen Zusammensetzung 95,6 % Ethanol und 4,4 % Wasser beträgt. Die Siedetemperatur des azeotropen Gemisches liegt um 78,2 °C niedriger als die der reinen Komponenten. Angenommen, Sie destillieren ein Wasser-Ethanol-Gemisch mit einem hohen Wassergehalt (nahezu 100 %). Es wird nicht möglich sein, reinen Alkohol zu erhalten, da in jeder Destillationsstufe größere Fraktionen erhalten werden. von Ethanol, aber niemals 100 % erreicht, nähert es sich allmählich der Zusammensetzung des azeotropen Gemischs (dem niedrigsten Punkt unter). Deshalb neigt es, wie Wasser, dazu, minimale Azeotrope mit zu bilden organische Verbindungen (angesichts der Art der intermolekularen Kräfte, die interagieren), ist es erforderlich, zuvor das Wasser aus der Mischung zu entfernen, um die reine Verbindung zu erhalten. Oder, sobald das Azeotrop erhalten ist, Verfahren von Extraktion von zusätzlichem Wasser.
Basierend auf dem oben Gesagten ist es kein Zufall, Alkohol zu finden (im Supermarkt u Apotheke) ist mit 95 % das billigste Produkt, das erhältlich ist. Um reinen Alkohol zu erhalten, ist es notwendig, das Azeotrop mit zu "brechen". Technik zusätzlich, wie die Verwendung von Trocknungsmitteln oder azeotrope Destillationen. Die azeotrope Destillation besteht darin, der Mischung eine zusätzliche Komponente zuzusetzen, die durch Mitreißen und Durchziehen wirkt Interaktion mit irgendeiner der Komponenten der Mischung (höhere Affinität) kann aus der Mischung entfernt werden.
Themen in Azeotrope