30 Beispiele für Alkohole
Beispiele / / November 06, 2023
Der Alkohole Sind organische chemische Verbindungen die in ihrer Struktur die funktionelle Hydroxylgruppe (-OH) enthalten, die an einen Kohlenstoff (-C) gebunden ist. Die Gruppe (-C – OH) wird „Carbinol“ genannt. Einige Beispiele für Alkohole sind: Methanol, Ethanol und 1-Propanol.
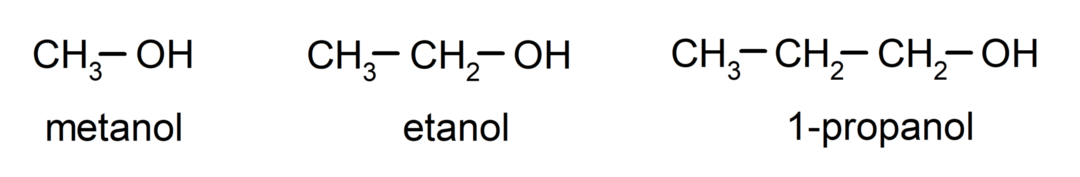
Alkohole sind chemische Verbindungen mit vielfältiger Verwendung im Alltag, da sie antibakterielle und antiseptische Eigenschaften haben. Andererseits können sie bei unkontrollierter Einnahme gesundheitsgefährdend sein.
Ebenso können nicht alle Alkohole vom Menschen aufgenommen werden.
- Siehe auch: Amine und Ketone
Arten von Alkoholen
Abhängig von der Anzahl der Kohlenstoffatome, an die das Kohlenstoffatom mit der Hydroxylgruppe gebunden ist, kann ein Alkohol sein:
- Primärer Alkohol. Das Kohlenstoffatom, an das die Hydroxylgruppe gebunden ist, ist auch an ein einzelnes Kohlenstoffatom gebunden. Zum Beispiel:
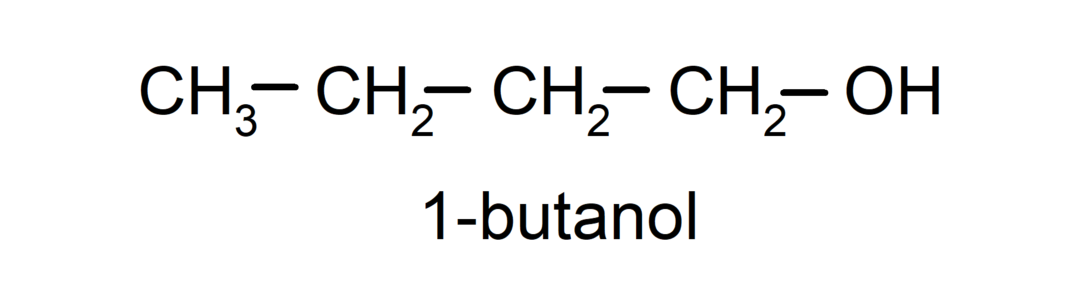
- Sekundärer Alkohol. Das Kohlenstoffatom, an das die Hydroxylgruppe gebunden ist, ist auch an zwei andere Kohlenstoffatome gebunden. Zum Beispiel:
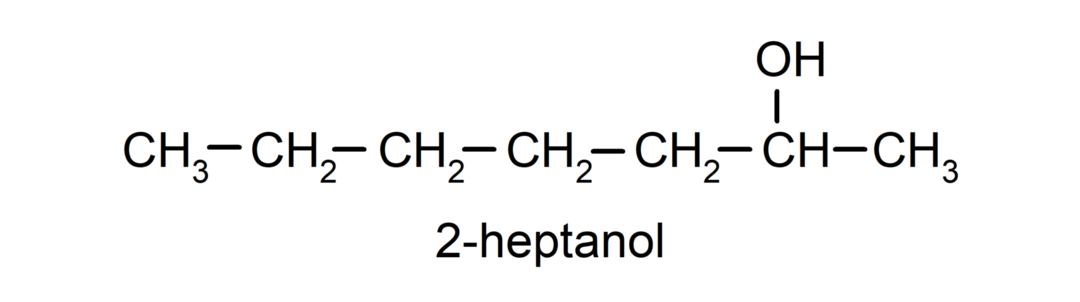
- Tertiärer Alkohol. Das Kohlenstoffatom, an das die Hydroxylgruppe gebunden ist, ist auch an drei Kohlenstoffatome gebunden. Zum Beispiel:
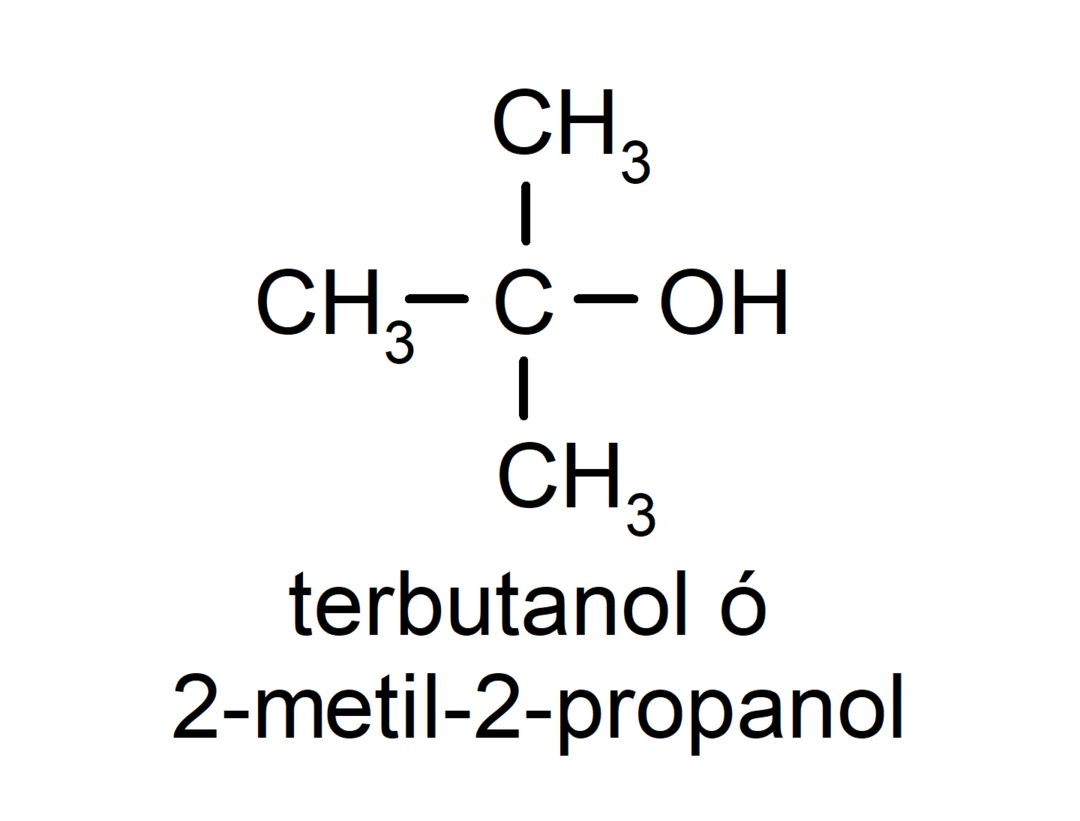
Abhängig von der Anzahl seiner Hydroxylgruppen kann ein Alkohol sein:
- Diol. Es hat zwei Hydroxylgruppen in seiner Struktur. Zum Beispiel:
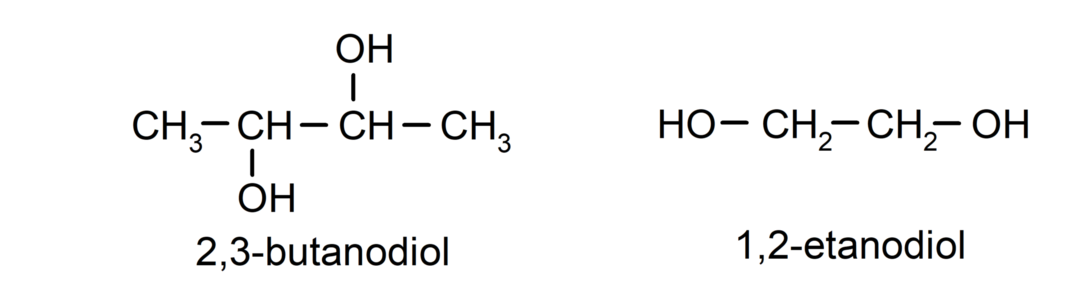
- Triol. Es hat drei Hydroxylgruppen in seiner Struktur. Zum Beispiel:
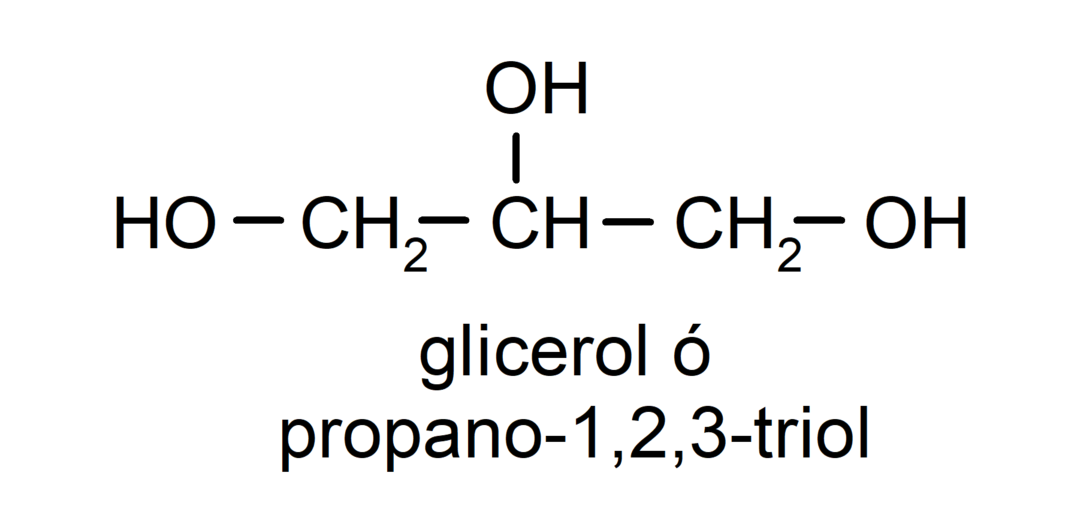
- Polyalkohol. Es hat viele Hydroxylgruppen in seiner Struktur. Zum Beispiel:
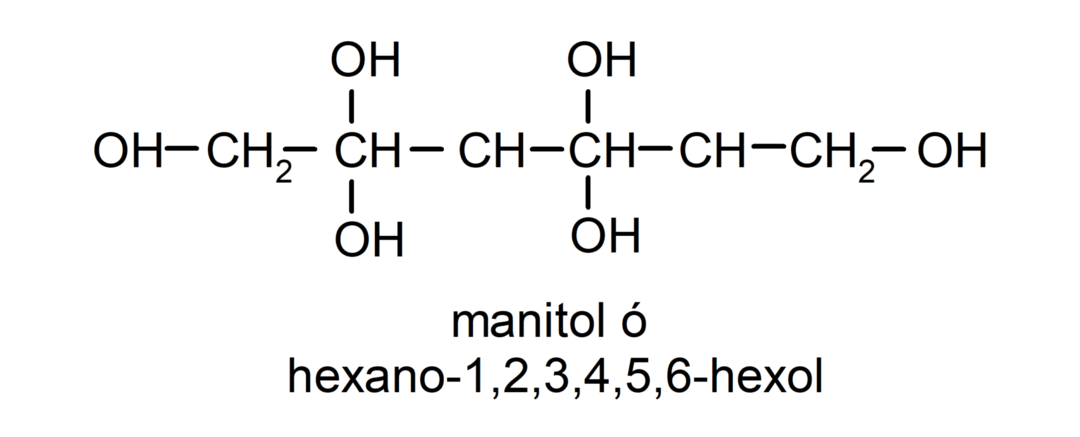
Physikalische Eigenschaften von Alkoholen
Einige der physikalischen Eigenschaften von Alkoholen sind:
- Siedepunkt. Der Siedepunkt in Alkoholen ist aufgrund der Anwesenheit der Hydroxylgruppe, die die Bildung von Wasserstoffbrückenbindungen ermöglicht, recht hoch. Darüber hinaus gilt: Je mehr hydroxylfunktionelle Gruppen in der Kohlenstoffkette vorhanden sind, desto höher ist die Siedepunkt von Alkoholen.
- Polarität. Alkohole sind recht polare Verbindungen.
- Löslichkeit. Alkohole mit niedrigem Molekulargewicht sind wasserlöslich. Andererseits ist die Löslichkeit von Alkoholen in Wasser umso geringer, je größer die Kohlenstoffkette ist. Darüber hinaus gilt: Je mehr Hydroxylgruppen Alkohole haben, desto besser ist ihre Wasserlöslichkeit.
- Aggregatzustand. Die meisten Alkohole sind bei Raumtemperatur (25 °C) flüssig und haben charakteristische Gerüche.
Chemische Eigenschaften von Alkoholen
Einige der chemischen Eigenschaften von Alkoholen sind:
- Alkohole verhalten sich wie Säuren und Basen.. Ihr Verhalten als Säuren zeigt sich in Reaktionen mit aktiven Metallen, bei denen Wasserstoffgas freigesetzt und Alkoxide gebildet werden.

Ihr Verhalten als Basen zeigt sich in Reaktionen wie der Reaktion von Methanol mit Bromwasserstoff zu Methyloxoniumbromid.
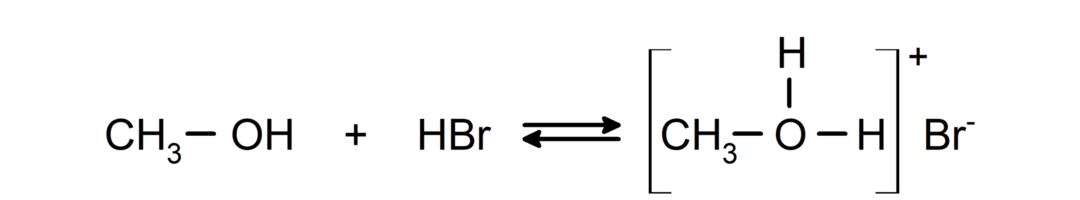
- Alkohole unterliegen Halogenierungsreaktionen. Sie reagieren mit Halogenwasserstoffen zu Alkylhalogeniden.
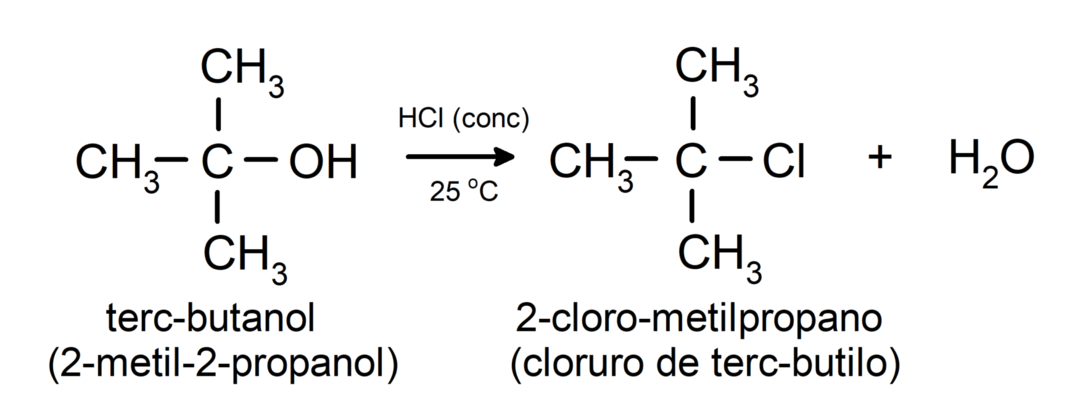
-
Alkohole unterliegen Oxidationsreaktionen wenn sie mit bestimmten oxidierenden Verbindungen reagieren. Die Produkte von Oxidationsreaktionen hängen von der Art des reagierenden Alkohols ab, d. h. davon, ob es sich um primären, sekundären oder tertiären Alkohol handelt.
Oxidation von primärem Alkohol zu Aldehyd oder Carbonsäure.
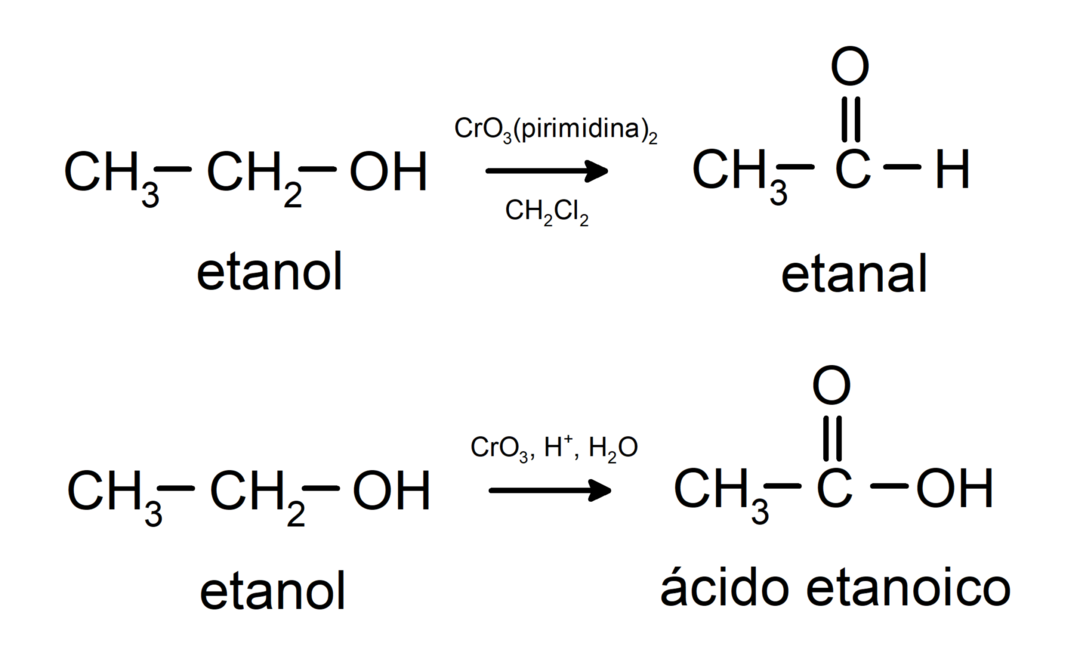
Oxidation von sekundärem Alkohol zu Keton.
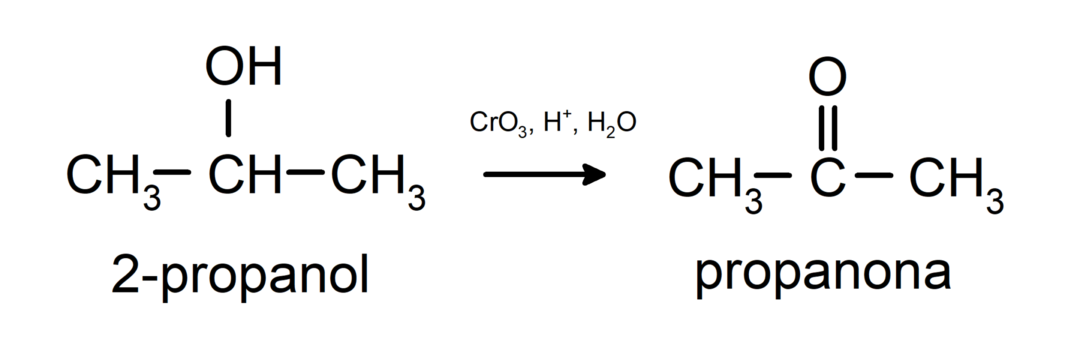
Tertiäre Alkohole oxidieren nicht mit üblichen Oxidationsmitteln. Mit sehr starken Oxidationsmitteln können sie in Alkene umgewandelt werden, die dann oxidiert werden können.
Alkohole mit zwei Hydroxylgruppen an benachbarten Kohlenstoffatomen werden mit Bleitetraacetat zu zwei Ketonen oxidiert.
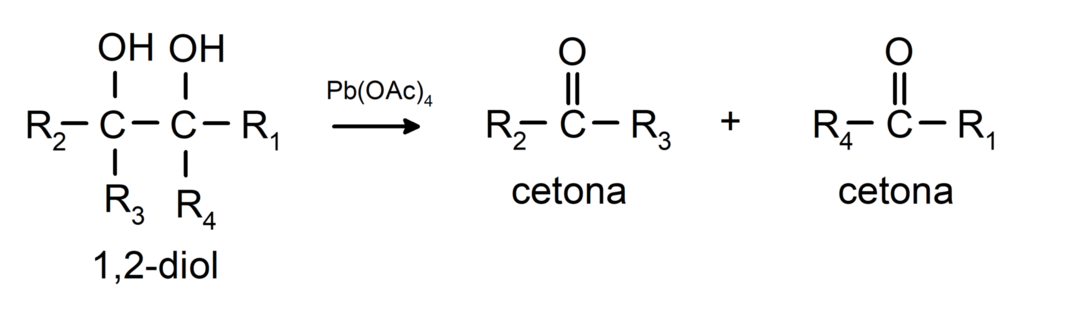
- Alkohole durchlaufen Dehydrierungsreaktionen. Diese Reaktionen finden nur mit primären und sekundären Alkoholen statt, die bei hohen Temperaturen in Gegenwart von Katalysatoren Wasserstoff freisetzen.
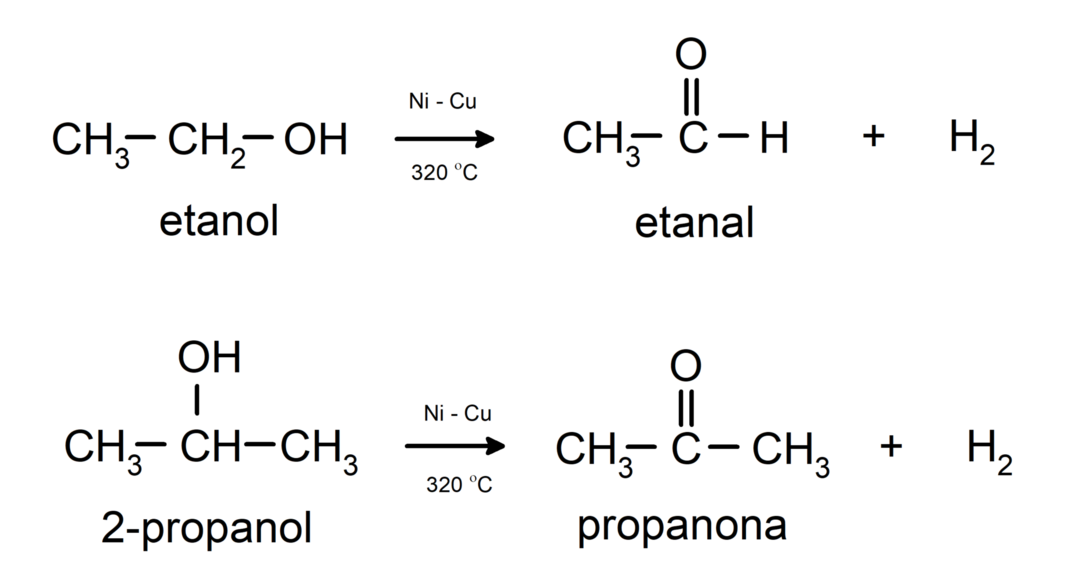
- Alkohole unterliegen Dehydratisierungsreaktionen. Alkohole dehydrieren unter Bildung der entsprechenden Alkene. Diese Reaktion findet in Gegenwart von Säure und mittleren Temperaturen statt.
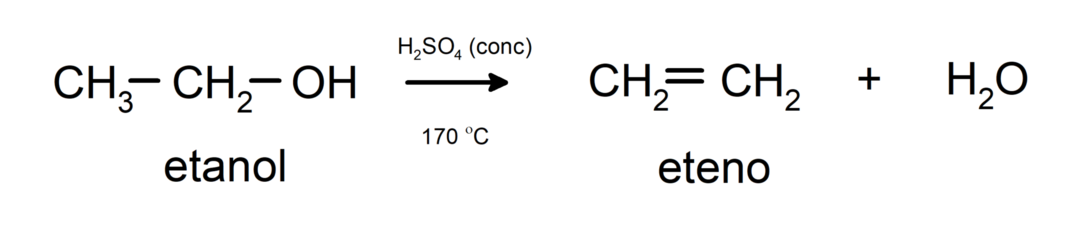
Alkoholnomenklatur
Gemäß der von der IUPAC (International Union of Pure and Applied Chemistry) festgelegten Nomenklatur werden Alkohole nach folgenden Regeln benannt:
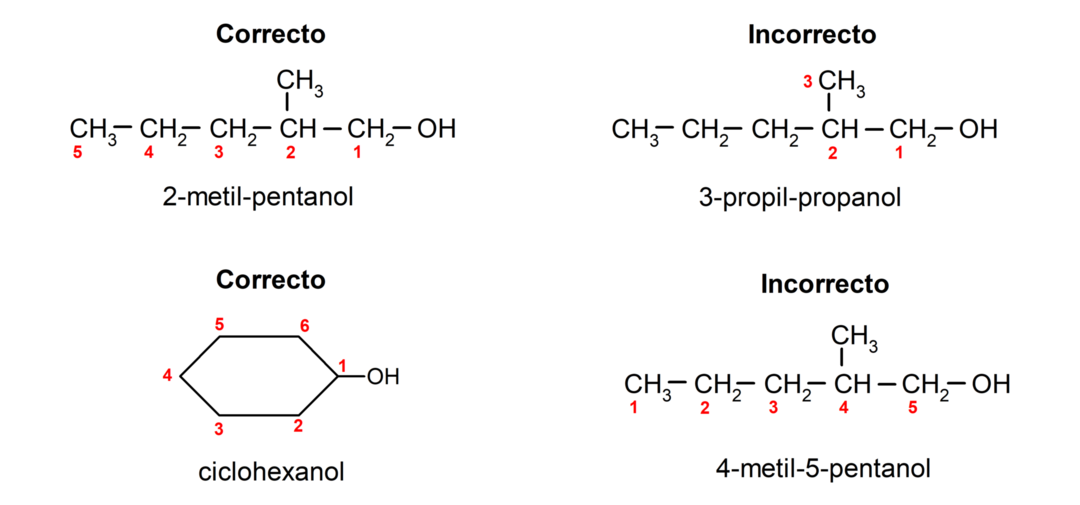
- Die Position der Hydroxylgruppe wird unter Berücksichtigung der Tatsache gewählt, dass sie die geringstmögliche Zahl in der Kohlenstoffkette einnimmt. Wenn die Struktur des Alkohols zyklisch ist, wird die 1. Position am Kohlenstoff berücksichtigt, an die die Hydroxylgruppe gebunden ist, und das Präfix cyclo- wird zur Benennung verwendet.
- Der Name des Alkohols wird mit Präfixen geschrieben, die die Anzahl der Atome in der Kohlenstoffkette angeben, und zusätzlich wird das Suffix -ol platziert.
- Wenn die Struktur des Alkohols Verzweigungen aufweist, wird die längste Kette, die auch die Hydroxylgruppe enthält, als Hauptkohlenstoffkette gewählt.
Gemäß der traditionellen Nomenklatur werden Alkohole benannt, indem man das Wort „Alkohol“ und dann den Namen des Alkohols schreibt. Alkan, das der Kohlenstoffkette entspricht, aber anstelle der -an-Endung des Alkans wird die Endung verwendet -yllic.
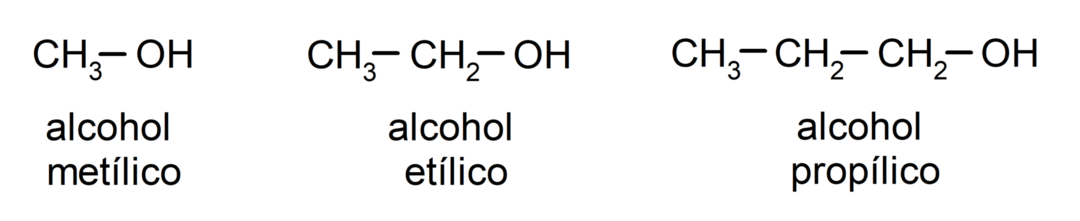
Beispiele für Alkohole
- Methanol
- Ethanol
- 1-Propanol
- 2-Propanol
- 1-Butanol
- 3-Ethylhexan-2-ol
- Glycerin
- Phenol
- 2-Methyl-2-butanol
- 1,2-Ethandiol
- 1,5-Heptadien-3-ol
- 3-Methyl-2-butanol
- Benzylmethanol
- 3-Pentanol
- 2-Methylphenol
- 1,2-Dihydroxyphenol
- Cyclohexanol
- 1-Phenylethanol


Verwendung von Alkoholen
Die häufigsten Verwendungszwecke von Alkoholen sind:
- Sie werden als Desinfektionsmittel und Antiseptika eingesetzt, da sie bei einigen das Wachstum stoppen Mikroorganismen oder sie zerstören. Zu diesem Zweck werden am häufigsten Ethanol und Isopropylalkohol verwendet.
- Sie werden bei der Synthese verschiedener verwendet Chemische Komponenten. Zur Gewinnung von Methanal (Formaldehyd) wird beispielsweise Methanol verwendet.
- Sie werden zur Herstellung von Frostschutzmitteln verwendet. Zu diesem Zweck wird am häufigsten Methanol verwendet.
- Sie werden als Lösungsmittel in der Pharmaindustrie verwendet. Ethanol ist in diesem Sinne eines der am häufigsten verwendeten.
- Sie werden als Lösungsmittel für Lacke, Farben und Tinten verwendet. Zu diesem Zweck wird häufig Methanol verwendet.
- Sie werden als Brennstoff verwendet und es besteht die starke Tendenz, die Verwendung teilweise zu ersetzen fossile Brennstoffe durch den Einsatz von Bioethanol-Kraftstoff.
- Sie werden zur Herstellung von Harzen verwendet. In diesem Sinne wird Phenol verwendet.
Gefahren des Alkoholkonsums
Obwohl Alkoholkonsum heute gesellschaftlich akzeptiert ist, führt der Missbrauch dieser Substanz zu Abhängigkeit und Sucht.
Ethanol ist der in alkoholischen Getränken enthaltene Alkohol, der bei übermäßigem Konsum Auswirkungen hat kognitive Fähigkeiten und kann Herz-Kreislauf-Erkrankungen, Leberzirrhose usw. verursachen Krebs.
Wenn außerdem der Grad der Alkoholvergiftung erreicht ist, also ein Zustand der Trunkenheit, wenn die Dosis des Ist der Alkoholgehalt zu hoch, kann es zu einem alkoholischen Koma kommen, das zu Atemlähmungen und sogar zum Tod führen kann. Tod.
Verweise
- T. ZU. Geißmann. (1974) „Principles of Organic Chemistry“, Zweite Auflage. Editorial Reverté, S.A. ISBN: 8429171800
- Ahumada-Cortez, J. G., Gámez-Medina, M. E., & Valdez-Montero, C. (2017). Alkoholkonsum als Problem der öffentlichen Gesundheit. Ra Ximhai, 13(2), 13-24.
- Morrison, R. T., & Boyd, R. N. (1998). Organische Chemie. Pearson Ausbildung.
- Weininger, S. J., & Stermitz, F. R. (1988). Organische Chemie. Ich habe umgekehrt.
Folge mit:
- Ethylalkohol
- Kraftstoffe
- organische Chemie


