Beispiel für eine Peptidbindung
Chemie / / July 04, 2021
Das Peptidbindung ist derjenige, in dem zwei Aminosäuremoleküle werden durch Kondensation verbunden.
Um Peptidbindungen besser zu verstehen, müssen zunächst Aminosäuren definiert werden:
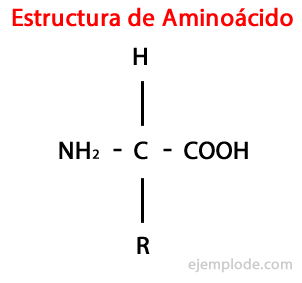
Das Aminosäuren sind organische Moleküle kurz mit mindestens eine Aminogruppe (-NH2), alkalisch, und eine Carboxylgruppe (-COOH), säuerlicher Charakter.
Obwohl Lebewesen für unterschiedliche Zwecke sehr unterschiedliche Arten von Aminosäuren synthetisieren, sind die wichtigsten diejenigen, die sind Bestandteil von Proteinen, die alle zur Klasse der gehören α-Aminosäuren.
Die α-Aminosäuren sind dadurch gekennzeichnet, dass die Säure- und Aminogruppen an das gleiche Kohlenstoffatom gebunden sind, das als α-Kohlenstoff bezeichnet wird. Außerdem bindet dieser α-Kohlenstoff als dritten Substituenten ein Wasserstoffatom und als vierten Substituent, eine zusätzliche Gruppe unterschiedlicher Größe und Eigenschaften, die jede Aminosäure von. unterscheidet Andere.
Der vierte Substituent heißt Seitenkette Aminosäure und wird oft vereinfacht durch den Buchstaben R dargestellt.
Da die vier Substituenten des α-Kohlenstoffs unterschiedlich sind und eine tetraedrische Anordnung darum einnehmen, sind die vorhandenen α-Aminosäuren optische Isomerie, das heißt, wenn ein Molekül a. hat Alternative Form das sieht aus wie ein Spiegelbild sein, das am Ende kein gleiches Molekül ist. Diesen beiden isomeren Molekülformen werden je nach räumlicher Anordnung der Substituenten die Buchstaben D oder L zugeordnet. Alle Aminosäuren, die in Proteinen enthalten sind, sind L.
Aminosäuren werden nach ihrem chemischen Charakter eingeteilt in classified Polar und Apolar. Die Polars wiederum sind unterteilt in Neutral und aufgeladen (die sauer oder basisch sein können). Das Unpolar kann aliphatisch oder aromatisch sein.
Peptide und die Peptidbindung
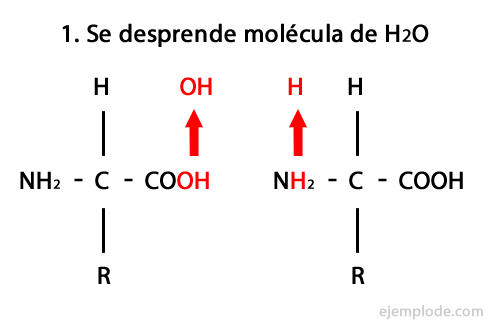
Peptide sind das Produkt der kovalenten Vereinigung von Aminosäuren durch Amidbindungen, die durch Kondensation des Carboxyl-Endes des einen und des Amino-Endes des anderen, wodurch ein Wassermolekül im. freigesetzt wird Reaktion. Diese Verbindung wird Peptidbindung genannt.
Der Mechanismus dieser Reaktion ist unten dargestellt, in dem die Amino- und Carboxylgruppen, und die Kondensation der Aminosäuremoleküle findet statt, um das Peptid zu bilden.
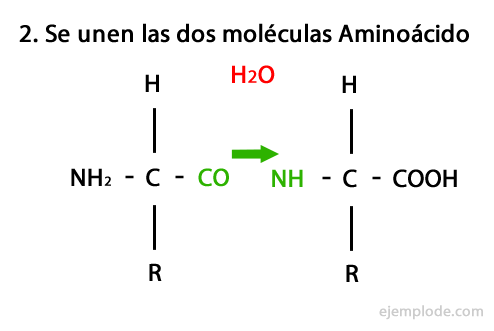

Peptide, wie Aminosäuren und Proteine, haben eine Aminogruppe und eine Carboxylgruppe an ihren Enden ohne zu reagieren.
Um die Formel eines einfachen Peptids und sogar eines Proteins anzugeben, reicht es aus, die Aminosäuren aufzulisten, aus denen es besteht. beginnend mit dem mit einer freien Aminogruppe, und endet mit dem mit seiner freien Carboxylgruppe.
Einige im Körper vorkommende Peptide sind die Vasopressin, das den Blutdruck erhöht und die Wasserresorption in der Niere erhöht; das Enkephalin, die das Schmerzempfinden reduziert; und der Oxytocin, wodurch sich die Gebärmutter zusammenzieht.
Eigenschaften der Peptidbindung
Die Kondensation der Aminogruppe einer Aminosäure mit dem Carboxyl einer anderen, erfolgt in wässrigem Lösungsmittel, so dass es ist nicht spontan, und daher erfordert die Proteinsynthese eine Zufuhr von Energie.
Die Peptidbindung, wie bei jeder Amidbindung, präsentiert Resonanz zwischen zwei Extremformen: die neutrale Form, mit einer Einfachbindung, die den Carbonylkohlenstoff der ersten Aminosäure und den Aminostickstoff der zweiten (C-N) verbindet, und das Formular mit Ladungstrennung bei dem die beiden Atome durch eine Doppelbindung (C = N) verbunden sind. In Wirklichkeit nimmt die Peptidbindung keine der beiden Extremsituationen an, sondern ist ein resonanter Hybrid aus beiden.
Da ist der Anruf Peptidebene, bestehend aus alle Atome, die an der Peptidbindung beteiligt sind, die die beiden ursprünglichen Aminosäuren verbinden. Einerseits die Atome von Stickstoff und Wasserstoff mit ihrem jeweiligen Kohlenstoff α in der ersten Aminosäure. Andererseits der Kohlenstoff α der anderen Aminosäure, mit dem Sauerstoff und Kohlenstoff der Carbonylgruppe.
Unterschiede zwischen Peptiden und Proteinen
Das Peptide haben eine geringe Anzahl an Aminosäuren, die von zwei bis zu einigen Dutzend reicht, und ihre Konformation in Lösung wird flexibel.
Das kleine Proteine, strukturell nahe bei großen Peptiden, haben a definierter Körperbau und viel weniger flexibel.
Es gibt Proteine, die wie Peptide eine ungeordnete und flexible Konformation haben, aber diese Reihenfolge, wenn sie mit anderen Makromolekülen in der Zelle interagieren.
20 Beispiele für Aminosäuren, die an der Peptidbindung beteiligt sind
- Glyzinien
- An das Mädchen
- Valin
- Leucin
- Isoleucin
- Prolin
- Methionin
- Phenylalanin
- Tyrosin
- Tryptophan
- Serin
- Threonin
- Cystein
- Asparagin
- Glutamin
- Asparaginsäure
- Glutaminsäure
- Lysin
- Arginin
- Histidin
