Beispiel für die Nomenklatur organischer Verbindungen
Chemie / / July 04, 2021
Organische Verbindungen sind Moleküle, deren Eigenschaft darin besteht, dass sie aus einer Basis von Kohlenstoffmolekülen bestehen und Wasserstoff, auch als Skelett bekannt, und kombiniert mit anderen Elementen, hauptsächlich Sauerstoff, Stickstoff und Schwefel.
Das IUPAC (International Union of Pure and Applied Chemistry, International Union of Pure and Applied Chemistry) hat allgemeine Regeln für die Klassifizierung und Nomenklatur organischer Moleküle aufgestellt, von denen wir die wichtigsten erläutern.
Kohlenwasserstoffe
Kohlenwasserstoffe sind die einfachsten organischen Moleküle, die aus einem Kohlenstoffgerüst und Wasserstoffatomen bestehen. Es gibt drei Arten von Kohlenwasserstoffen:
Alkane
Sie sind die einfachsten und bestehen aus Kohlenstoffatomen, die durch einfache kovalente Bindungen mit den Atomen von. verbunden sind Wasserstoff, mit der allgemeinen Formel H = 2n + 2, dh die Wasserstoffatome sind doppelt so viele Wasserstoffatome. Kohlenstoff plus 2. Seine Nomenklatur wird mit den numerischen Präfixen met- für 1 Kohlenstoffatom, et- für 2, prop- für 3 und but- für 4 gebildet; ab 5 Kohlenstoffatomen werden die üblichen Vorsilben pent-, hex-, hept-, oct-, etc. verwendet. Allen Alkanen wird die Endung -ano hinzugefügt.
Beispiel: CH4: Methan; C2H6: Ethan; C4H10: Butan; C6H14: Hexan
Alkene
Sie werden durch ein Kohlenstoffgerüst gebildet, in dem eine Doppelbindung zwischen den Kohlenstoffatomen besteht. Seine allgemeine Formel ist H = 2n, dh seine Wasserstoffatome haben die doppelte Anzahl von Kohlenstoffatomen. Wie Alkane verwenden sie Präfixe, die die Anzahl der Kohlenstoffatome angeben, und in diesem Fall wird die Endung -eno hinzugefügt. Darüber hinaus ist in Molekülen mit mehr als drei Kohlenstoffatomen die Kohlenstoff, wo sich die Doppelbindung befindet, beginnend mit dem Kohlenstoff, der am nächsten zu liegt ist.
Beispiele: C2H4: Ethen; C3H6: Propen; C4H8: Buten, 2-Buten; C6H12: Hexen, 2-Hexen (Doppelbindung an Atom 2), 3-Hexen (Doppelbindung an Atom 3).
Alkine
Alkine enthalten an ihren Kohlenstoffatomen eine Dreifachbindung. Seine allgemeine Formel ist H = 2n-2, was darauf hinweist, dass das Molekül zwei Wasserstoffatome enthält, die weniger als doppelt so viele Kohlenstoffatome aufweisen. An das Präfix, das die Anzahl der Kohlenstoffe angibt, wird die Endung -ino angehängt. Wie bei Alkenen wird der Kohlenstoff mit der Dreifachbindung erwähnt, gezählt vom äußersten nächsten.
Beispiele: C2H2: Ethin; C3H4: Trinkgeld; C4H6: Butin, 2-Butin; C6H12: Hexino, 2-Hexen (Dreifachbindung an Atom 2), 3-Hexin (Dreifachbindung an Atom 3).
Funktionelle Gruppen
Funktionelle Gruppen sind Kombinationen von Atomen, die als Ion fungieren und ein Wasserstoffatom in der Formel eines Alkans ersetzen.
Radikale
Das Alkan ohne das Wasserstoffatom heißt Radical, und zur Identifizierung wird die Endung -ilo hinzugefügt:
Beispiele CH4: Methan - CH3+ Methyl; C2H6: Ethan - C2H5+ Ethyl; C4H10: Butan - C4H9+ Butyl; C6H14: Hexan - C6H13+ Hexyl.
Kombination von Kohlenwasserstoffen
Einer der Fälle, die auftreten können, ist die Kombination von zwei oder mehr Kohlenwasserstoffen in einem Molekül. Die Kohlenwasserstoffe, mit denen es kombiniert wird, werden Arboreszenzen genannt. In diesen Fällen ist der basische Kohlenwasserstoff der mit der längsten Kette, und die Anzahl der Kohlenstoffatome ist die Arboreszenzen werden gefunden, gefolgt vom Namen des Radikals mit der Endung -il und dann dem Namen des Kohlenwasserstoffs Base. Die Nummer wird so oft genannt, wie die Bäume, die ihr zugeordnet sind. Für den Fall, dass die Arboreszenzen in verschiedenen Kohlenstoffatomen denselben Rest aufweisen, werden die durch Kommas getrennten Zahlen gefolgt von einem Bindestrich angegeben. der Name des Rests, dann die Nummern der Atome, an die der andere Rest gebunden ist, falls vorhanden, ein Bindestrich, der Name des Rests und der Name des Kohlenwasserstoffs Base. Falls zwei Reste an das gleiche Kohlenstoffatom gebunden sind, wird die Zahl zweimal genannt. Handelt es sich um unterschiedliche Reste, so wird dies einmal vor dem Namen jedes Restes genannt; wenn die Reste gleich sind, wird die Zahl zweimal genannt. Wir beginnen damit, dass wir zuerst die einfachsten Arboreszenzen (die mit der geringsten Menge an Kohlenstoff) und dann die mit der höchsten Menge erwähnen.
Beispiel: Ein Pentanmolekül mit zwei Ethanradikalen, gebunden an Kohlenstoff 2 und 3:
2,3-Ethylpentan. Ein Oktanmolekül, ein Propanradikal an Kohlenstoff 6, Methanradikale an Kohlenstoff 4 und 5 und Ethanradikale, gebunden an Kohlenstoff 2, 3 und 4: 4,5-Methyl-2,3,4-ethyl-6-propyl -Oktan.
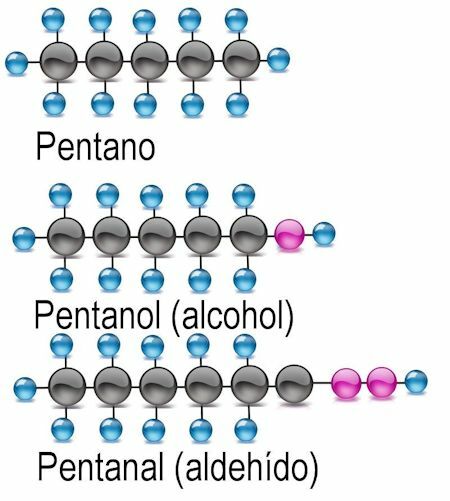
Alkoholfunktionelle Gruppe
Die einfachste der funktionellen Gruppen ist Alkohol, bei dem ein Wasserstoffatom durch eine Hydroxylgruppe (OH) ersetzt ist. Bei diesen Verbindungen wird die Endung -anol an den Namen des Restes angehängt. Gegebenenfalls ist das Kohlenstoffatom, an dem sich die funktionelle Gruppe befindet, zu nennen:
Beispiele CH3OH: Methanol: C2H5OH-Ethanol; C4H9OH-Butanol oder 2-Butanol; C6H13OH-Hexanol, 2-Hexanol (funktionelle Gruppe an Atom 2), 3-Hexanol (funktionelle Gruppe an Atom 3).
Aldehyd-Funktionsgruppe
Bei Aldehyden wird das Wasserstoffatom gegen die funktionelle Gruppe ausgetauscht -CHO. Um sie zu identifizieren, wird die Endung -anal hinzugefügt und das Kohlenstoffatom, an dem sich die funktionelle Gruppe befindet, wird auch erwähnt:
Beispiele CH3COH: Methanal: C2H5Ethanal COH; C4H9COH-Butanal oder 2-Butanal; C6H13COH-Hexanal, 2-Hexanal (funktionelle Gruppe an Atom 2), 3-Hexanal (funktionelle Gruppe an Atom 3).
Säurefunktionelle Gruppe
In organischen Säuren wird das Wasserstoffatom gegen die funktionelle Gruppe ausgetauscht -COOH. Um sie zu identifizieren, wird das Wort Säure erwähnt und die Endung -anoic hinzugefügt, und das Kohlenstoffatom, an dem sich die funktionelle Gruppe befindet, wird auch erwähnt:
Beispiele CH3COOH: Methansäure: C2H5COOH-Ethansäure; C4H9COOH-Butansäure oder 2-Butansäure; C6H13COH-Hexansäure, 2-Hexansäure (funktionelle Gruppe an Atom 2), 3-Hexansäure (funktionelle Gruppe an Atom 3).
