20 Παραδείγματα χημικών φαινομένων
Miscellanea / / July 04, 2021
ο χημικά φαινόμενα (ή χημικές αντιδράσεις) είναι εκείνα τα φαινόμενα στα οποία εμφανίζονται αλλαγές στην ύλη, και σχηματίζονται νέες ουσίες που ονομάζονται "προϊόντα" και άλλες αποκαλούνται "αντιδραστήρια" αποσυντίθενται. Για παράδειγμα: σήψη ξύλου, καύση χαρτιού, κομποστοποίηση.
Οι χημικές αντιδράσεις μπορεί να είναι αυθόρμητος (αντιδράσεις που συμβαίνουν χωρίς την ανάγκη ενέργειας ή καταλυτών) ή όχι αυθόρμητα (αντιδράσεις που χρειάζονται τη συμβολή ενέργειας, καταλύτες ή κάποια εξωτερική παρέμβαση). Πολλές φορές, για να εμφανιστεί μια αντίδραση είναι απαραίτητο για τα αντιδραστήρια να έχουν θερμοκρασία συγκεκριμένη, α pH μια καθορισμένη τιμή πίεσης κ.λπ.
Μπορεί επίσης να είναι απαραίτητο για τον έλεγχο του ταχύτητα στις οποίες εμφανίζονται χημικές αντιδράσεις. ο καταλύτες Είναι ουσίες που προστίθενται σε μια χημική αντίδραση για να αυξήσουν την ταχύτητά της, ενώ οι αναστολείς είναι ουσίες που επιβραδύνουν την ταχύτητα των χημικών αντιδράσεων. Άλλοι παράγοντες που επηρεάζουν το ρυθμό μιας χημικής αντίδρασης είναι η θερμοκρασία, η πίεση, η συγκέντρωση των αντιδρώντων και η ίδια η φύση της αντίδρασης.
Μπορεί να σας εξυπηρετήσει:
Τύποι χημικών φαινομένων
Οι χημικές αντιδράσεις μπορεί να είναι:
Ανόργανες αντιδράσεις. Παρεμβαίνω ανόργανες ενώσεις και μπορεί να ταξινομηθεί σύμφωνα με:
- Η έννοια με την οποία εμφανίζεται η αντίδραση.
-
Αναστρέψιμες αντιδράσεις. Εμφανίζονται αμφότερα, έτσι ώστε τα προϊόντα να διασπώνται και να σχηματίζουν ξανά τα αντιδραστήρια.
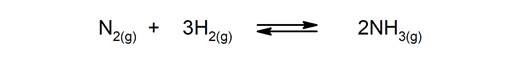
-
Μη αναστρέψιμες αντιδράσεις. Συμβαίνουν μόνο με έναν τρόπο.

-
Αναστρέψιμες αντιδράσεις. Εμφανίζονται αμφότερα, έτσι ώστε τα προϊόντα να διασπώνται και να σχηματίζουν ξανά τα αντιδραστήρια.
- Ο τύπος των σωματιδίων που αντιδρά.
-
Αντιδράσεις οξέος-βάσης. Πραγματοποιείται μεταφορά ιόντων Η+.

-
Αντιδράσεις μείωσης οξείδωσης. Ένα από τα αντιδραστήρια οξειδώνεται (αυξάνει τον αριθμό του οξείδωση), ενώ το άλλο μειώνεται (ο αριθμός οξείδωσης μειώνεται). Σε αυτές τις αντιδράσεις συμβαίνει μεταφορά ηλεκτρονίων.

-
Αντιδράσεις οξέος-βάσης. Πραγματοποιείται μεταφορά ιόντων Η+.
- Ο ρυθμός αντίδρασης.
-
Γρήγορες αντιδράσεις. Εμφανίζονται σε πολύ σύντομο χρονικό διάστημα.
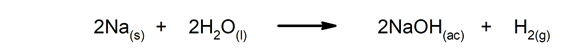
-
Αργές αντιδράσεις Χρειάζονται πολύς χρόνος για να ολοκληρωθούν.
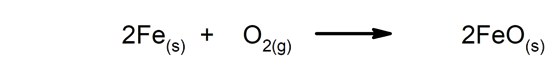
-
Γρήγορες αντιδράσεις. Εμφανίζονται σε πολύ σύντομο χρονικό διάστημα.
- Η μορφή της ενέργειας που εκπέμπει ή απορροφά.
-
Εξωθερμικές αντιδράσεις. Καθώς εμφανίζονται, απελευθερώνουν θερμότητα.
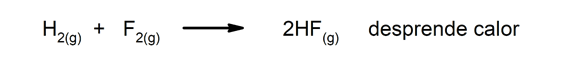
-
Ενδοθερμικές αντιδράσεις. Όταν συμβαίνουν, απορροφούν τη θερμότητα.

-
Εξωφρενικές αντιδράσεις. Όταν συμβαίνουν, εκπέμπουν φως.

-
Ενδοφλεβικές αντιδράσεις. Για να συμβούν, χρειάζονται φως.

-
Εξωθερμικές αντιδράσεις. Καθώς εμφανίζονται, απελευθερώνουν θερμότητα.
- Ο τύπος του μετασχηματισμού.
-
Αντιδράσεις σύνθεσης ή προσθήκης. Δύο ουσίες συνδυάζονται για να σχηματίσουν μια νέα ουσία.
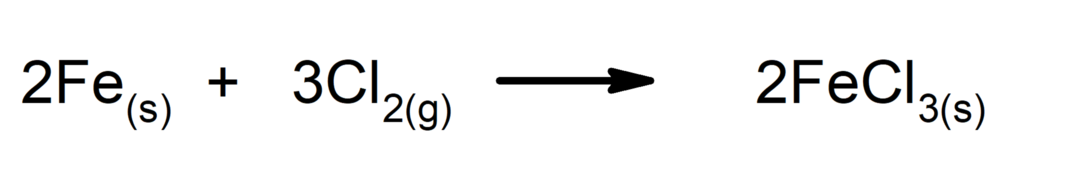
-
Αντιδράσεις αποσύνθεσης. Μία ή περισσότερες ουσίες διασπώνται στα απλούστερα συστατικά τους.
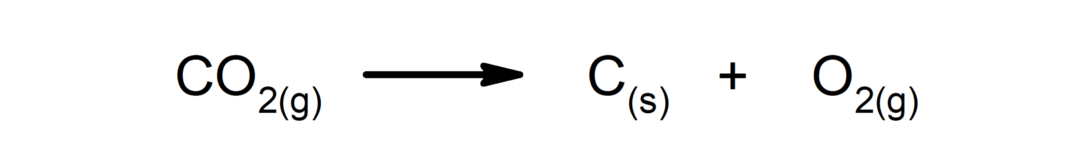
-
Αντιδράσεις μετατόπισης ή αντικατάστασης. Ένα στοιχείο ή ένωση αντικαθιστά ένα άλλο σε μια ένωση, απελευθερώνοντάς το.
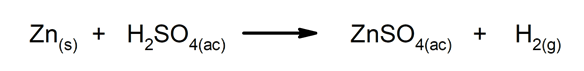
-
Αντιδράσεις διπλής υποκατάστασης. Δύο ενώσεις ανταλλάσσουν στοιχεία ή ενώσεις ταυτόχρονα.

-
Αντιδράσεις σύνθεσης ή προσθήκης. Δύο ουσίες συνδυάζονται για να σχηματίσουν μια νέα ουσία.
Οργανικές αντιδράσεις. Είναι αντιδράσεις στις οποίες παρεμβαίνουν οργανικές ενώσεις. Έχουν πολλές ταξινομήσεις με βάση τον τύπο της οργανικής ένωσης που αντιδρά και τον τύπο της αντίδρασης που υποβάλλεται. Μερικά παραδείγματα είναι:
-
Αλογόνωση αλκανίων. Ένα υδρογόνο αντικαθιστά το α αλκανίου από αλογόνο.
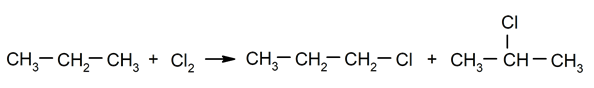
-
Καύση αλκανίων. Ένα αλκάνιο αντιδρά με οξυγόνο για να παράγει διοξείδιο του άνθρακα και νερό, εάν ολοκληρωθεί η καύση.
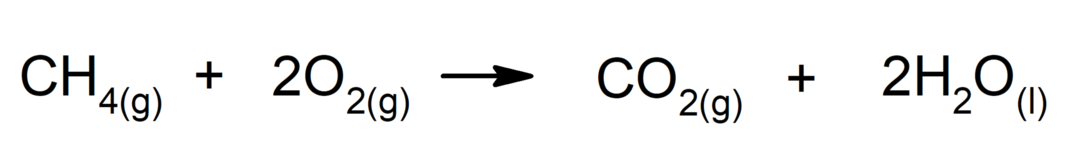
-
Αλογόνωση του αλκένια. Τα αλογόνα αντικαθιστούν ένα ή και τα δύο υδρογόνα των ανθράκων που εμπλέκονται στον διπλό δεσμό.
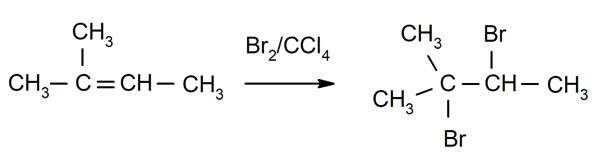
-
Υδρογόνωση αλκενίων. Τα υδρογόνα προστίθενται στους άνθρακες που εμπλέκονται στον διπλό δεσμό για να σχηματίσουν το αντίστοιχο αλκάνιο.
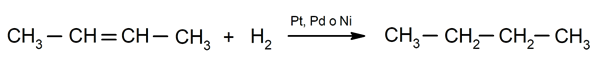
Σημασία των χημικών φαινομένων
Πολλά χημικά φαινόμενα διατηρήστε τη ζωή ζωντανών πραγμάτων, όπως πέψη σε ανθρώπους και των ζώων, φωτοσύνθεση στα φυτά και αναπνοή και στα δύο.
Μια άλλη πολύ σημαντική χημική διαδικασία, ειδικά στη ζωή του μικροοργανισμοί, είναι το ζύμωση, το οποίο χρησιμοποιείται συνήθως στην κατασκευή του τροφή όπως τυριά, γιαούρτια, κρασιά και μπύρες.
Ολα τα αυξάνουν και το ανάπτυξη του α ζωντανό ον Περιλαμβάνει χημικές αντιδράσεις που λαμβάνουν χώρα σε αυτό, μερικές φορές διεγείρονται από ορισμένες περιβαλλοντικές συνθήκες.
Παραδείγματα χημικών φαινομένων
Γύρω μας υπάρχουν πολλές περιπτώσεις χημικών φαινομένων ή διεργασιών που περιλαμβάνουν:
- Ξύλο σάπιο
- Καύση χαρτιού
- Αντοχή σε αντιβιοτικά βακτήρια
- Γάλα που γίνεται ξινό
- Απολύμανση μιας πληγής με αλκοόλ
- Χρησιμοποιώντας αλάτι φρούτων για την καταπολέμηση της καούρας
- Κάψιμο ενός κεριού
- Πήξης του αίματος
- Μυϊκή κόπωση μετά από έντονη άσκηση
- ΘΑΝΑΤΟΣ του έντομα από εντομοκτόνα
- Λήψη τυριού Roquefort
- Λήψη μηλίτη
- Λήψη γιαουρτιού
- Κομποστοποίηση
- Απασχόληση
- Λήψη βιοαιθανόλης από μελάσα
- Πρησμένα δοχεία κασσίτερου
- Χαλασμένο αυγό
- Σκουριά από σχάρα
- Λήψη βιοντίζελ από φοινικέλαιο
Χημικά φαινόμενα στη βιομηχανία
Ορισμένα χημικά φαινόμενα είναι επίσης βασικά στοβιομηχανία. Κατ 'αρχάς, η καύση του υδρογονάνθρακες (όπως βενζίνη, ντίζελ ή κηροζίνη) παράγει Ενέργεια να τρέξει τις μηχανές που χειρίζονται αμέτρητες βιομηχανικές διαδικασίες.
Από την άλλη πλευρά, το βιομηχανία χάλυβα, χαρτί, πλαστικά, δομικά υλικά, χρώματα, φάρμακα, προϊόντα για η αγρο, κ.λπ., βασίζεται σε διάφορα χημικά φαινόμενα όπως γαλβανισμός, ηλεκτρόλυση και πολλά άλλοι περισσότερο.
Η γενιά του νέες πηγές ενέργειας (όπως το βιοντίζελ και η βιοαιθανόλη) βασίζεται επίσης σε αυτό το είδος φαινομένου.
Ο μετασχηματισμός της ενέργειας
Σε χημικά φαινόμενα είναι κοινό να υπάρχει ενεργειακός μετασχηματισμός. Για παράδειγμα, όταν η χημική ενέργεια που περιέχεται στους δεσμούς ενός συγκεκριμένου μορίου μετατρέπεται σε ηλεκτρική ενέργεια ή απελευθερώνεται ως θερμότητα (αυτό συμβαίνει σε εξωθερμικά φαινόμενα, όπως όταν το υδροχλωρικό οξύ αναμιγνύεται με ψευδάργυρο), υπάρχει μετασχηματισμός Ενέργεια. Το ίδιο συμβαίνει όταν η ελαφριά ενέργεια συλλαμβάνεται και μετατρέπεται σε χημική ενέργεια.
Ορισμένες χημικές διεργασίες απαιτούν τη λειτουργία της θερμότητας και ονομάζονται «ενδοθερμική». Άλλοι απαιτούν την παρουσία καταλυτών ή συμπαράγοντων.
