Πώς σχηματίζονται τα υδροξείδια; (με παραδείγματα)
Miscellanea / / July 04, 2021
ο υδροξείδια αποτέλεσμα από το συνδυασμό ενός μεταλλικό οξείδιο (επίσης λέγεται βασικά οξείδια) Και το νερό. Με αυτόν τον τρόπο, η σύνθεση των υδροξειδίων δίνεται από τρία στοιχεία: οξυγόνο, υδρογόνο και το εν λόγω μέταλλο. Σε συνδυασμό, το μέταλλο πάντα να ενεργείς σαν κατιόν και η ομάδα υδροξειδίου (ΟΗ–) λειτουργεί ως ανιόν. Για παράδειγμα:
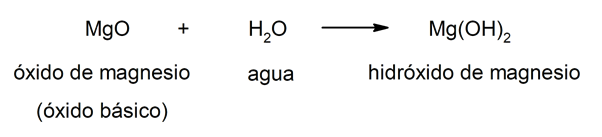
Γενικά, τα υδροξείδια, μοιράζονται ορισμένα χαρακτηριστικά, όπως παρουσιάζοντας μια πικρή γεύση και είναι καυστική. Επιπλέον, είναι συνήθως ολισθηρό στην αφή και διαβρωτικό. Από την άλλη πλευρά, έχουν κάποιες ιδιότητες απορρυπαντικών και σαπουνιών. Τα περισσότερα είναι διαλυτά στο νερό και αντιδρούν με οξέα για την παραγωγή βγες έξω.
Ορισμένα χαρακτηριστικά, από την άλλη πλευρά, είναι ειδικά για κάθε τύπο υδροξειδίου, όπως αυτό του νάτριο (NaOH), το οποίο απορροφά νερό, και αναμιγνύεται με quicklime (CaO) απορροφά γρήγορα το διοξείδιο του άνθρακα (CO2). Από την πλευρά του, υδροξείδιο του ασβεστίου (Ca (OH)2) λαμβάνεται στην αντίδραση οξειδίου του ασβεστίου με νερό και απορροφά επίσης CO
2. Ένα άλλο παράδειγμα είναι το υδροξείδιο του σιδήρου (II) (Fe (OH)2), η οποία είναι μια ζελατινώδης ένωση και είναι πρακτικά αδιάλυτη στο νερό.Τα υδροξείδια ονομάζονται επίσης βάσεις ή αλκάλια, αν και αυτοί οι όροι έχουν επεκταθεί και για άλλες ουσίες με αλκαλικό χαρακτήρα και που δεν είναι υδροξείδια.
Σε τι χρησιμοποιούνται τα υδροξείδια;
Οι εφαρμογές των υδροξειδίων ποικίλλουν επίσης μεταξύ των διαφόρων περιπτώσεων:
Ονοματολογίες
Εκτός από την ονομασία άλλων τύπων χημικές ενώσεις, υπάρχουν διαφορετικές ονοματολογίες για τα υδροξείδια:
Παραδείγματα υδροξειδίων
- Υδροξείδιο μολύβδου (II), Pb (OH)2, διυδροξείδιο του μολύβδου.
- Υδροξείδιο Platinum (IV), Pt (OH)4τετραϋδροξείδιο πλατίνας.
- Vanadic υδροξείδιο, V (OH)4, τετραϋδροξείδιο του βαναδίου.
- Υδροξείδιο του σιδήρου, Fe (OH)2, διυδροξείδιο του σιδήρου.
- Υδροξείδιο μολύβδου (IV), Pb (OH)4, τετραϋδροξείδιο μολύβδου.
- Υδροξείδιο αργύρου, AgOH, υδροξείδιο αργύρου.
- Υδροξείδιο κοβαλτίου, Co (OH)2, διυδροξείδιο του κοβαλτίου.
- Υδροξείδιο του μαγγανίου, Mn (OH)3, τριυδροξείδιο του μαγγανίου.
- Υδροξείδιο του σιδήρου, Fe (OH)3, τριϋδροξείδιο του σιδήρου.
- Υδροξείδιο του χαλκού, Cu (OH)2, διυδροξείδιο του χαλκού.
- Υδροξείδιο αργιλίου, Al (OH)3, τριϋδροξείδιο αργιλίου.
- Υδροξείδιο του νατρίου, NaOH, υδροξείδιο του νατρίου.
- Υδροξείδιο του στροντίου, Sr (OH)2, διϋδροξείδιο του στροντίου.
- Υδροξείδιο του μαγνησίου, Mg (OH)2, διυδροξείδιο του μαγνησίου.
- Υδροξείδιο αμμωνίου, NH4ΟΗ, υδροξείδιο του αμμωνίου.
- Υδροξείδιο του καδμίου, Cd (OH)2, διϋδροξείδιο του καδμίου.
- Vanadic υδροξείδιο, V (OH)3, τριϋδροξείδιο του βαναδίου.
- Υδροξείδιο του υδραργύρου, Hg (OH)2, διυδροξείδιο του υδραργύρου.
- Υδροξείδιο του χαλκού, CuOH, υδροξείδιο του χαλκού.
- Υδροξείδιο λιθίου, LiOH, υδροξείδιο λιθίου.
Μερικές φορές έχουν τα υδροξείδια κοινά ονόματα δεδομένης της πιο συμβατικής χρήσης του: το υδροξείδιο του νατρίου ονομάζεται επίσης καυστική σόδα, το υδροξείδιο του καλίου ονομάζεται καυστική ποτάσα, υδροξείδιο του ασβεστίου που ονομάζεται ασβέστης νερό ή ασβέστης και υδροξείδιο του μαγνησίου που ονομάζεται γάλα μαγνησία.
Ακολουθήστε με:

