Παράδειγμα δεσμού πεπτιδίου
Χημεία / / July 04, 2021
ο Πεπτιδικός δεσμός είναι αυτό στο οποίο δύο μόρια αμινοξέων ενώνονται με συμπύκνωση.
Για να κατανοήσουμε καλύτερα τους πεπτιδικούς δεσμούς, πρέπει πρώτα να οριστούν τα αμινοξέα:
ο Τα αμινοξέα είναι οργανικά μόρια σύντομο που περιέχει τουλάχιστον μια αμινομάδα (-ΝΗ2), αλκαλικό στη φύση, και μια καρβοξυλική ομάδα (-COOH), όξινο χαρακτήρα.
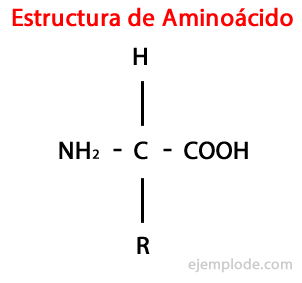
Αν και τα ζωντανά όντα συνθέτουν, για διαφορετικούς σκοπούς, πολύ διαφορετικούς τύπους αμινοξέων, τα πιο σημαντικά είναι αυτά που είναι μέρος πρωτεϊνών, όλα ανήκουν στην τάξη του α-αμινοξέα.
Τα α-αμινοξέα χαρακτηρίζονται από το ότι το οξύ και οι αμινομάδες συνδέονται στο ίδιο άτομο άνθρακα, που ονομάζεται α άνθρακας. Επιπλέον, αυτός ο α-άνθρακας δεσμεύει, ως τρίτος υποκαταστάτης, άτομο υδρογόνου και, ως τέταρτο υποκαταστάτη, μια πρόσθετη ομάδα διαφορετικού μεγέθους και χαρακτηριστικών, η οποία διαφοροποιεί κάθε αμινοξύ από οι υπολοιποι.
Ο τέταρτος υποκαταστάτης ονομάζεται Πλευρική αλυσίδα Το αμινοξύ και αντιπροσωπεύεται συχνά με απλοποιημένη μορφή με το γράμμα R.
Καθώς οι τέσσερις υποκαταστάτες του α-άνθρακα είναι διαφορετικοί και υιοθετούν μια τετραεδρική διάταξη γύρω από αυτό, τα α-αμινοξέα οπτικός ισομερισμός, που είναι όταν ένα μόριο έχει εναλλακτική μορφή που μοιάζει με εικόνα καθρέφτη του, το οποίο στο τέλος δεν είναι ίσο μόριο. Σε αυτές τις δύο ισομερείς μορφές του μορίου αποδίδονται τα γράμματα D ή L, ανάλογα με τον τρόπο που οι υποκαταστάτες είναι διατεταγμένοι στο διάστημα. Όλα τα αμινοξέα που βρίσκονται στις πρωτεΐνες είναι L.
Τα αμινοξέα ταξινομούνται σύμφωνα με τον χημικό τους χαρακτήρα στο Πολικός και απολικός. Τα Polars με τη σειρά τους χωρίζονται σε Ουδέτερο και φορτισμένο (που μπορεί να είναι όξινο ή βασικό). ο Το μη πολικό μπορεί να είναι αλειφατικό ή αρωματικό.
Πεπτίδια και ο δεσμός πεπτιδίου
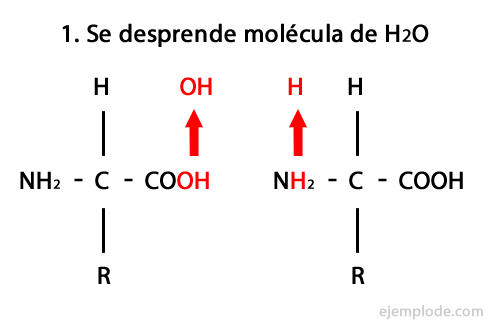
Τα πεπτίδια είναι το προϊόν της ομοιοπολικής ένωσης αμινοξέων μέσω Amide Bonds, σχηματίζοντας από συμπύκνωση του καρβοξυλικού άκρου του ενός και του αμινο άκρου του άλλου, απελευθερώνοντας ένα μόριο νερού στο αντίδραση. Αυτή η ένωση ονομάζεται Peptide Bond.
Ο μηχανισμός αυτής της αντίδρασης παρουσιάζεται παρακάτω, στον οποίο Ομάδες αμινο και καρβοξυλίου, και η συμπύκνωση των μορίων αμινοξέων συμβαίνει για να σχηματίσει το πεπτίδιο.
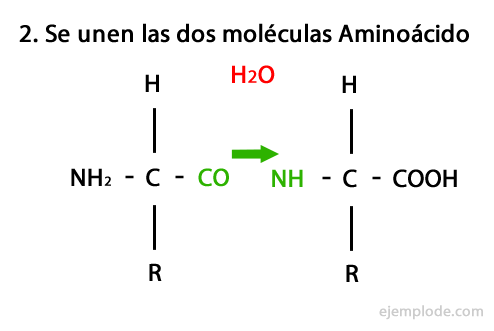

Πεπτίδια, όπως αμινοξέα και πρωτεΐνες, έχουν μια αμινομάδα και μια καρβοξυλική ομάδα στα άκρα τους χωρίς αντίδραση.
Για να προσδιορίσετε τον τύπο ενός απλού πεπτιδίου, και ακόμη και μιας πρωτεΐνης, αρκεί να απαριθμήσετε τα αμινοξέα που το συνθέτουν, ξεκινώντας με αυτό με μια δωρεάν ομάδα Amino, και τελειώνει με αυτό με τη δωρεάν ομάδα Carboxyl.
Μερικά πεπτίδια που βρίσκονται στο σώμα είναι τα Βασοπρεσίνη, η οποία αυξάνει την αρτηριακή πίεση και αυξάνει την απορρόφηση του νερού στα νεφρά. ο Εγκεφαλίνη, η οποία μειώνει την αίσθηση του πόνου. και το Οξυτοκίνη, που προκαλεί τη συστολή της μήτρας.
Χαρακτηριστικά πεπτιδικού δεσμού
Η συμπύκνωση της αμινομάδας ενός αμινοξέος με το καρβοξύλιο άλλου, λαμβάνει χώρα σε υδατικό διαλύτη, έτσι ώστε δεν είναι αυθόρμητο, και συνεπώς η σύνθεση πρωτεϊνών απαιτεί παροχή ενέργειας.
Ο δεσμός πεπτιδίου, όπως σε κάθε αμιδικό δεσμό, παρουσιάζει συντονισμό μεταξύ δύο ακραίων μορφών: η ουδέτερη μορφή, με έναν μόνο δεσμό που ενώνει τον καρβονύλιο άνθρακα του πρώτου αμινοξέος και το αμινο άζωτο του δεύτερου (C-N), και τη φόρμα με διαχωρισμό χρεώσεων στο οποίο τα δύο άτομα συνδέονται με διπλό δεσμό (C = N). Στην πραγματικότητα, ο πεπτιδικός δεσμός δεν υιοθετεί καμία από τις δύο ακραίες καταστάσεις, αλλά είναι ένα συντονισμένο υβρίδιο και των δύο.
Υπάρχει η κλήση Πεπτιδικό επίπεδο, που αποτελείται από όλα τα άτομα που εμπλέκονται στο πεπτιδικό δεσμό, τα οποία ενώνουν τα δύο αρχικά αμινοξέα. Αφενός, τα άτομα του αζώτου και του υδρογόνου, με τον αντίστοιχο άνθρακα α στο πρώτο αμινοξύ. Από την άλλη, ο άνθρακας α του άλλου αμινοξέος, με το οξυγόνο και τον άνθρακα της καρβονυλομάδας.
Διαφορές μεταξύ πεπτιδίων και πρωτεϊνών
ο τα πεπτίδια έχουν χαμηλό αριθμό αμινοξέων, η οποία κυμαίνεται από δύο έως μερικές δεκάδες από αυτές, και η διαμόρφωσή τους σε διάλυμα γίνεται ευέλικτη.
ο μικρές πρωτεΐνες, δομικά κοντά σε μεγάλα πεπτίδια, έχουν καθορισμένη διαμόρφωση και πολύ λιγότερο ευέλικτη.
Υπάρχουν πρωτεΐνες που, όπως τα πεπτίδια, έχουν διαταραγμένη και ευέλικτη διαμόρφωση, αλλά ταξινομούνται όταν αλληλεπιδρούν με άλλα μακρομόρια στο κύτταρο.
20 παραδείγματα αμινοξέων που συμμετέχουν στο Peptide Bonding
- Γλυκίνη
- Στο κορίτσι
- Βαλίν
- Λευκίνη
- Ισολευκίνη
- Προλίνη
- Μεθειονίνη
- Φαινυλαλανίνη
- Τυροσίνη
- Τρυπτοφάνη
- Σερίνη
- Θρεονίνη
- Κυστεΐνη
- Σπαράγγια
- Γλουταμίνη
- Ασπαρτικό οξύ
- Γλουταμινικό οξύ
- Λυσίνη
- Αργινίνη
- Ιστιδίνη


