Παράδειγμα ονοματολογίας οργανικών ενώσεων
Χημεία / / July 04, 2021
Οι οργανικές ενώσεις είναι μόρια των οποίων το χαρακτηριστικό είναι ότι σχηματίζονται από μια βάση μορίων άνθρακα και υδρογόνο, επίσης γνωστό ως σκελετός, και σε συνδυασμό με άλλα στοιχεία, κυρίως οξυγόνο, άζωτο και θείο.
ο IUPAC (Διεθνής Ένωση Καθαρής και Εφαρμοσμένης Χημείας, Διεθνής Ένωση Καθαρής και Εφαρμοσμένης Χημείας) έχει θεσπίσει γενικούς κανόνες για την ταξινόμηση και την ονοματολογία των οργανικών μορίων, από τους οποίους εξηγούμε τα πιο σημαντικά.
Υδρογονάνθρακες
Οι υδρογονάνθρακες είναι τα απλούστερα οργανικά μόρια, αποτελούμενα από σκελετό άνθρακα και άτομα υδρογόνου. Υπάρχουν τρεις τύποι υδρογονανθράκων:
Αλκάνια
Είναι τα πιο απλά, σχηματίζονται από άτομα άνθρακα που συνδέονται με απλούς ομοιοπολικούς δεσμούς με τα άτομα υδρογόνο, με το γενικό σκεύασμα H = 2n + 2, δηλαδή, τα άτομα υδρογόνου είναι διπλάσιο του αριθμού των ατόμων υδρογόνου. άνθρακας, συν 2. Η ονοματολογία του σχηματίζεται με τα αριθμητικά προθέματα met- για 1 άτομο άνθρακα, et- για 2, prop- για 3 και but- for 4; από 5 άτομα άνθρακα χρησιμοποιούνται τα κοινά προθέματα pent-, hex-, hept-, oct-, κλπ. Σε όλα τα αλκάνια προστίθεται το τέλος -ano.
Παράδειγμα: CH4: μεθάνιο; ντο2Η6: αιθάνιο; ντο4Η10: βουτάνιο; ντο6Η14: εξάνιο
Αλκένια
Σχηματίζονται από έναν σκελετό άνθρακα στον οποίο υπάρχει ένας διπλός δεσμός μεταξύ των ατόμων άνθρακα. Ο γενικός τύπος του είναι H = 2n, δηλαδή τα άτομα υδρογόνου του είναι διπλάσιο από τον αριθμό ατόμων άνθρακα. Όπως τα αλκάνια, χρησιμοποιούν προθέματα που δηλώνουν τον αριθμό των ατόμων άνθρακα και σε αυτήν την περίπτωση προστίθεται το τέλος -eno. Επιπλέον, σε μόρια με περισσότερα από τρία άτομα άνθρακα, το άνθρακα όπου βρίσκεται ο διπλός δεσμός, αρχίζοντας να μετράει από τον άνθρακα που βρίσκεται πλησιέστερα είναι.
Παραδείγματα: Γ2Η4: αιθένιο; ντο3Η6: προπένιο; ντο4Η8: βουτένιο, 2-βουτένιο; ντο6Η12: Εξένιο, 2-εξένιο (διπλός δεσμός στο άτομο 2), 3-εξένιο (διπλός δεσμός στο άτομο 3).
Αλκίνες
Τα αλκίνια περιέχουν τριπλό δεσμό στα άτομα άνθρακα. Ο γενικός τύπος του είναι H = 2n-2, υποδεικνύοντας ότι το μόριο θα περιέχει δύο άτομα υδρογόνου μικρότερο από το διπλάσιο του αριθμού των ατόμων άνθρακα. Στο πρόθεμα που υποδεικνύει τον αριθμό των άνθρακα, προστίθεται το τέλος -ino. Όπως στην περίπτωση των αλκενίων, αναφέρεται ο άνθρακας που περιέχει τον τριπλό δεσμό, μετρούμενος από το ακραίο πλησιέστερο σε αυτό.
Παραδείγματα: Γ2Η2: αιθίνη; ντο3Η4: υπόδειξη; ντο4Η6: butyne, 2-butyne; ντο6Η12: Hexino, 2-hexyne (τριπλός δεσμός στο άτομο 2), 3-hexyne (τριπλός δεσμός στο άτομο 3).
Λειτουργικές ομάδες
Οι λειτουργικές ομάδες είναι συνδυασμοί ατόμων που λειτουργούν ως ιόντα και αντικαθιστούν ένα άτομο υδρογόνου στον τύπο ενός αλκανίου.
Ριζοσπαστικά
Το αλκάνιο χωρίς το άτομο υδρογόνου ονομάζεται Radical, και για να το αναγνωρίσουμε προστίθεται το τέλος -ilo:
Παραδείγματα CH4: μεθάνιο - CH3+ μεθύλιο; ντο2Η6: αιθάνιο - C2Η5+ αιθύλιο; ντο4Η10: βουτάνιο - C4Η9+ βουτύλιο; ντο6Η14: εξάνιο - C6Η13+ εξύλιο.
Συνδυασμός υδρογονανθράκων
Μία από τις περιπτώσεις που μπορεί να συμβεί είναι ότι δύο ή περισσότεροι υδρογονάνθρακες συνδυάζονται σε ένα μόριο. Οι υδρογονάνθρακες με τους οποίους συνδυάζεται ονομάζονται arborescences. Σε αυτές τις περιπτώσεις, ο βασικός υδρογονάνθρακας θα είναι αυτός με τη μεγαλύτερη αλυσίδα και ο αριθμός άνθρακα όπου Βρίσκονται τα arborescences, ακολουθούμενο από το όνομα της ρίζας με το τέλος -il, και μετά το όνομα του υδρογονάνθρακα βάση. Ο αριθμός θα αναφέρεται τόσο πολλές φορές όσο τα δέντρα που συνδέονται με αυτό. Σε περίπτωση που οι αρβοσκέψεις είναι της ίδιας ρίζας σε διαφορετικά άτομα άνθρακα, θα αναφερθούν οι αριθμοί που διαχωρίζονται με κόμματα, ακολουθούμενο από παύλα, το όνομα της ρίζας, τότε οι αριθμοί των ατόμων όπου συνδέεται η άλλη ρίζα, εάν υπάρχει, μια παύλα, το όνομα της ρίζας και το όνομα του υδρογονάνθρακα βάση. Σε περίπτωση που υπάρχουν δύο ρίζες συνδεδεμένες στο ίδιο άτομο άνθρακα, ο αριθμός θα αναφέρεται δύο φορές. Εάν είναι διαφορετικές ρίζες, τότε θα αναφέρεται μία φορά πριν από το όνομα κάθε ρίζας. Αν οι ρίζες είναι ίσες, ο αριθμός θα αναφέρεται δύο φορές. Θα ξεκινήσουμε αναφέροντας πρώτα τους απλούστερους arborescences (αυτούς με τη λιγότερη ποσότητα άνθρακα) και μετά αυτούς με την υψηλότερη ποσότητα.
Παράδειγμα: Ένα μόριο πεντανίου, με δύο ρίζες αιθανίου, συνδεδεμένο στον άνθρακα 2 και 3:
2,3-αιθυλ πεντάνιο. Ένα μόριο οκτανίου, μια ρίζα προπανίου στον άνθρακα 6, ρίζες μεθανίου στους άνθρακες 4 και 5, και ρίζες αιθανίου, συνδεδεμένες στους άνθρακες 2, 3 και 4: 4,5-μεθυλ-2,3,4-αιθυλ-6-προπυλ -οκτάνιο.
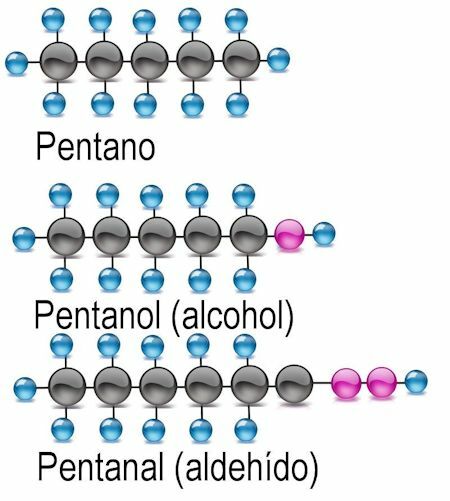
Λειτουργική ομάδα αλκοόλ
Η απλούστερη από τις λειτουργικές ομάδες είναι η αλκοόλη, στην οποία ένα άτομο υδρογόνου αντικαθίσταται από μια ομάδα υδροξυλίου (ΟΗ). Σε αυτές τις ενώσεις η τελική-αιθανόλη προστίθεται στο όνομα της ρίζας. Όπου ενδείκνυται, πρέπει να αναφέρεται το άτομο άνθρακα όπου βρίσκεται η λειτουργική ομάδα:
Παραδείγματα CH3ΟΗ: μεθανόλη: C2Η5ΟΗ αιθανόλη; ντο4Η9ΟΗ βουτανόλη ή 2-βουτανόλη; ντο6Η13ΟΗ εξανόλη, 2-εξανόλη (λειτουργική ομάδα στο άτομο 2), 3-εξανόλη (λειτουργική ομάδα στο άτομο 3).
Λειτουργική ομάδα αλδεϋδης
Στις αλδεϋδες, το άτομο υδρογόνου ανταλλάσσεται με τη λειτουργική ομάδα -CHO. Για την ταυτοποίησή τους, προστίθεται το τέλος-anal και αναφέρεται επίσης το άτομο άνθρακα όπου βρίσκεται η λειτουργική ομάδα:
Παραδείγματα CH3COH: μεθανάλη: C2Η5Ethanal COH; ντο4Η9COH βουταναλ ή 2-βουταναλη; ντο6Η13COH εξάνιο, 2-εξάνιο (λειτουργική ομάδα στο άτομο 2), 3-εξάνιο (λειτουργική ομάδα στο άτομο 3).
Οξύ λειτουργική ομάδα
Στα οργανικά οξέα, το άτομο υδρογόνου ανταλλάσσεται με τη λειτουργική ομάδα -COOH. Για την ταυτοποίησή τους, αναφέρεται η λέξη οξύ και προστίθεται το τέλος -anoic και αναφέρεται επίσης το άτομο άνθρακα όπου βρίσκεται η λειτουργική ομάδα:
Παραδείγματα CH3COOH: μεθανοϊκό οξύ: C2Η5COOH αιθανοϊκό οξύ; ντο4Η9COOH βουτανοϊκό οξύ ή 2-βουτανοϊκό οξύ. ντο6Η13COH εξανοϊκό οξύ, 2-εξανοϊκό οξύ (λειτουργική ομάδα στο άτομο 2), 3-εξανοϊκό οξύ (λειτουργική ομάδα στο άτομο 3).


