20 keemiliste nähtuste näited
Miscellanea / / July 04, 2021
The keemilised nähtused (või keemilised reaktsioonid) on need nähtused, kus aines toimuvad muutused, moodustuvad uued ained, mida nimetatakse "toodeteks", ja teised, mida nimetatakse "reagentideks", lagunevad. Näiteks: puidumädanik, paberi põletamine, kompostimine.
Keemilised reaktsioonid võivad olla spontaanne (reaktsioonid, mis toimuvad ilma energia või katalüsaatorite vajaduseta) või mitte spontaanne (reaktsioonid, mis vajavad energia panust, katalüsaatoreid või mõnda välist sekkumist). Mitu korda on reaktsiooni tekkimiseks vajalik, et reagentidel oleks a temperatuur spetsiifiline, a pH seatud rõhu väärtus jne.
Samuti võib olla oluline kontrollida kiirus millele tekivad keemilised reaktsioonid. The katalüsaatorid Need on ained, mis lisatakse keemilisele reaktsioonile selle kiiruse suurendamiseks, inhibiitorid aga ained, mis aeglustavad keemiliste reaktsioonide kiirust. Teised keemilise reaktsiooni kiirust mõjutavad tegurid on temperatuur, rõhk, reagentide kontsentratsioon ja reaktsiooni olemus.
See võib teile teenida:
Keemiliste nähtuste tüübid
Keemilised reaktsioonid võivad olla:
Anorgaanilised reaktsioonid. Vahele segama anorgaanilised ühendid ja neid saab liigitada järgmiselt:
- Tähendus, milles reaktsioon toimub.
-
Pöörduvad reaktsioonid. Neid esineb mõlemal viisil, nii et saadused võivad laguneda ja moodustavad reaktandid uuesti.
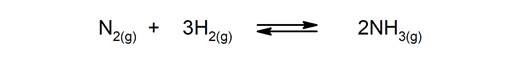
-
Pöördumatud reaktsioonid. Neid juhtub ainult ühel viisil.

-
Pöörduvad reaktsioonid. Neid esineb mõlemal viisil, nii et saadused võivad laguneda ja moodustavad reaktandid uuesti.
- Reageeriva osakese tüüp.
-
Happe-aluse reaktsioonid. Toimub H ioonide ülekanne+.

-
Oksüdatsiooni-redutseerimise reaktsioonid. Üks reaktantidest oksüdeerub (suurendab selle reaktiivi) oksüdeerumine), samas kui teine on redutseeritud (selle oksüdatsiooniarv väheneb). Nendes reaktsioonides toimub elektronide ülekanne.

-
Happe-aluse reaktsioonid. Toimub H ioonide ülekanne+.
- Reaktsioonikiirus.
-
Kiired reaktsioonid. Need tekivad väga lühikese aja jooksul.
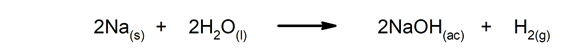
-
Aeglased reaktsioonid Nende täitmine võtab kaua aega.
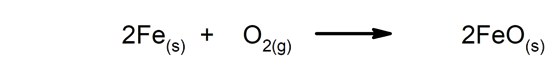
-
Kiired reaktsioonid. Need tekivad väga lühikese aja jooksul.
- Selle kiiratava või neelduva energia vorm.
-
Eksotermilised reaktsioonid. Tekkides eraldavad nad soojust.
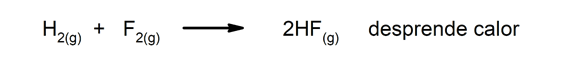
-
Endotermilised reaktsioonid. Nende tekkimisel neelavad nad soojust.

-
Eksolumiinsed reaktsioonid. Kui need tekivad, kiirgavad nad valgust.

-
Endoluminous reaktsioonid. Et juhtuda, vajavad nad valgust.

-
Eksotermilised reaktsioonid. Tekkides eraldavad nad soojust.
- Transformatsiooni tüüp.
-
Sünteesi- või liitumisreaktsioonid. Kaks ainet moodustavad uue aine.
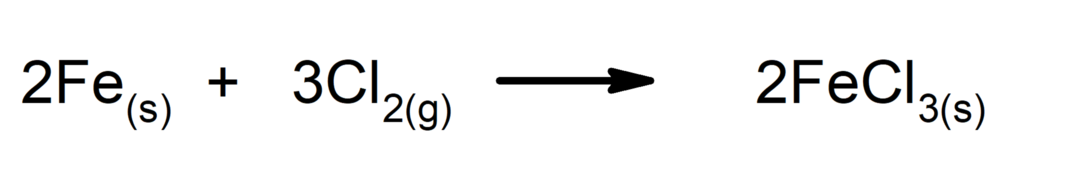
-
Lagunemisreaktsioonid. Üks või mitu ainet lagunevad kõige lihtsamateks koostisosadeks.
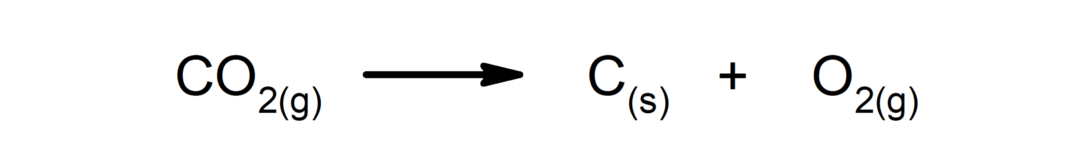
-
Nihutamis- või asendusreaktsioonid. Üks element või ühend asendab ühendis teise, vabastades selle.
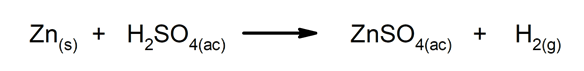
-
Topeltasendusreaktsioonid. Kaks ühendit vahetavad elemente või ühendeid korraga.

-
Sünteesi- või liitumisreaktsioonid. Kaks ainet moodustavad uue aine.
Orgaanilised reaktsioonid. Need on reaktsioonid, milles orgaanilised ühendid sekkuvad. Neil on palju klassifikatsioone, mis põhinevad reageeriva orgaanilise ühendi tüübil ja selle reaktsioonil. Mõned näited on:
-
Alkaanide halogeenimine. Vesinik on asendatud a alkaan halogeeniga.
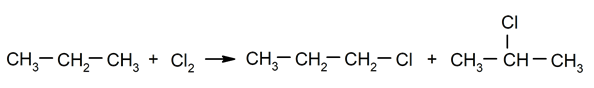
-
Alkaanide põletamine. Alkaan reageerib hapnikuga, tekitades süsinikdioksiidi ja vett, kui põlemine on täielik.
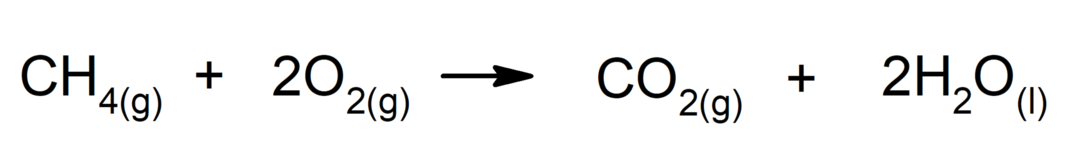
-
Halogeenimine alkeenid. Halogeenid on asendatud ühe või mõlema süsiniku vesinikuga, mis on seotud kaksiksidemega.
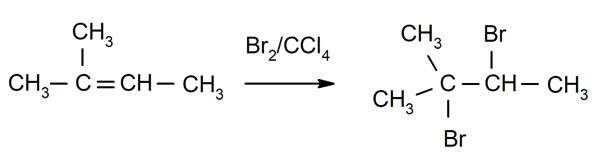
-
Alkaanide hüdrogeenimine. Kaksiksidemega seotud süsinikele lisatakse vastava alkaani moodustamiseks vesinikud.
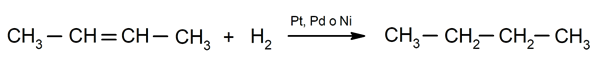
Keemiliste nähtuste tähtsus
Paljud keemilised nähtused säilitada elu elusolenditest, näiteks seedimine inimestel ja loomad, fotosüntees taimedes ja hingamine mõlemas.
Teine väga oluline keemiline protsess, eriti elus mikroorganismid, on käärimine, mida tavaliselt kasutatakse toit nagu juustud, jogurtid, veinid ja õlled.
Kõik suurendama ja kasvu aasta elusolend See hõlmab selles toimuvaid keemilisi reaktsioone, mida mõnikord stimuleerivad teatud keskkonnatingimused.
Keemiliste nähtuste näited
Meie ümber on arvukalt keemilisi nähtusi või protsesse, mis neid sisaldavad:
- Puidumädanik
- Põlemine paberist
- Vastupanu antibiootikumid bakterid
- Piim, mis muutub hapuks
- Haava desinfitseerimine alkohol
- Puuviljasoola kasutamine kõrvetiste vastu võitlemiseks
- Küünla põletamine
- Vere hüübimine
- Lihasväsimus pärast intensiivset treeningut
- Surm putukad putukamürkide abil
- Roqueforti juustu saamine
- Siidri hankimine
- Jogurti saamine
- Kompostimine
- Sileerimine
- Bioetanooli saamine melassist
- Paisunud plekkpurgid
- Mädamuna
- Resti roostetamine
- Biodiisli saamine palmiõlist
Keemilised nähtused tööstuses
Teatud keemilised nähtused on ka võtmetähtsusegatööstuses. Alustuseks põletamine süsivesinikud (näiteks bensiin, diisel või petrooleum) toodab Energia juhtida masinaid, mis tegelevad lugematute tööstusprotsessidega.
Teiselt poolt terasetööstus, paber, plast, ehitusmaterjalid, värvid, ravimid, tooted agro jne põhinevad erinevatel keemilistel nähtustel nagu galvaniseerimine, elektrolüüs ja paljud teised rohkem.
Põlvkond uusi energiaallikaid (nagu biodiisel ja bioetanool) põhineb samuti seda tüüpi nähtustel.
Energia muundumine
Keemiliste nähtuste korral on see tavaline energia muundamine. Näiteks kui teatud molekuli sidemetes sisalduv keemiline energia muundatakse elektrienergiaks või vabastatakse kuumus (seda esineb eksotermiliste nähtuste korral, näiteks kui vesinikkloriidhape segatakse tsingiga), toimub Energia. Sama juhtub siis, kui valgusenergia on hõivatud ja muundatud keemiliseks energiaks.
Mõned keemilised protsessid vajavad töötamiseks soojust ja neid nimetatakse "endotermilisteks". Teised nõuavad katalüsaatorite või kofaktorite olemasolu.