20 Näited hapetest
Miscellanea / / July 04, 2021
The happed moodustavad olulise rühma keemilised ühendid, väga lai. Happeid määratletakse tavaliselt kui ühendeid, mis võivad annetada ühe või mitu katioonid vesinik (H+) teiseks ühendiks, tuntud kui alus. Ehkki tegelikkuses on happed määratletud mitme teooria järgi:
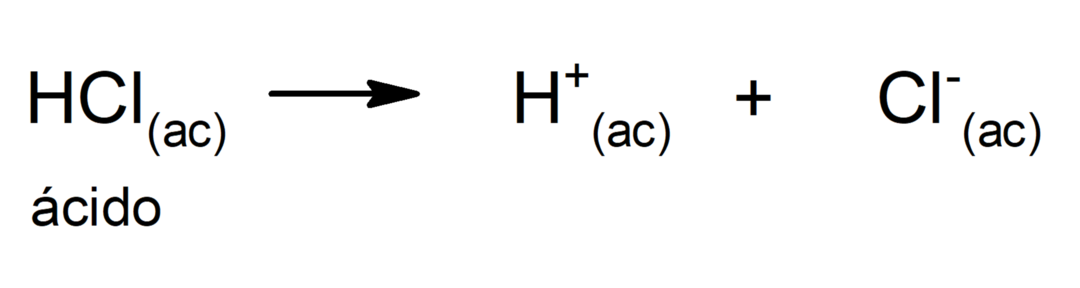 Selle teooria piirang on see, et happed on määratletud ainult vesilahuses.
Selle teooria piirang on see, et happed on määratletud ainult vesilahuses. 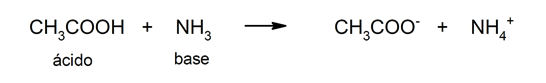

Vabastamise vara vesinikioonid on see, mis paneb happed tootma lahuseid pH vähem kui 7. Happed, mis võivad vabastada rohkem kui ühte prootonit (kasutades seda nime H+) nimetatakse polüprootilisteks või polüfunktsionaalseteks.
Happelised omadused
Nende kohta omadused, happeid võib esitada järgmiselt: vedelikud või nagu gaasid, harvemini kui tahke. Happemaitse, mille tunneme ära ja mis iseloomustab neid ühendeid, leiame näiteks tsitrusviljad, mis sisaldavad palju sidrunhapet või äädikat, mis on happe lahus äädikhape. Need on orgaanilised happed.
olemas orgaanilised ja anorgaanilised happed; kõige tugevamad on tavaliselt anorgaanilised. Paljud orgaanilised happed täidavad olulist bioloogilist rolli. Anorgaaniliste hulgast on vesinikkloriidhape, millel on seedimisprotsessis väga oluline roll. The
nukleiinhapped Need on olulised ka kogu elu jaoks, kuna need on organismi geneetilise materjali aluseks rakke ja sisaldavad võtme valk.Happe tugevuse määrab prootonite kaotamise tendents.
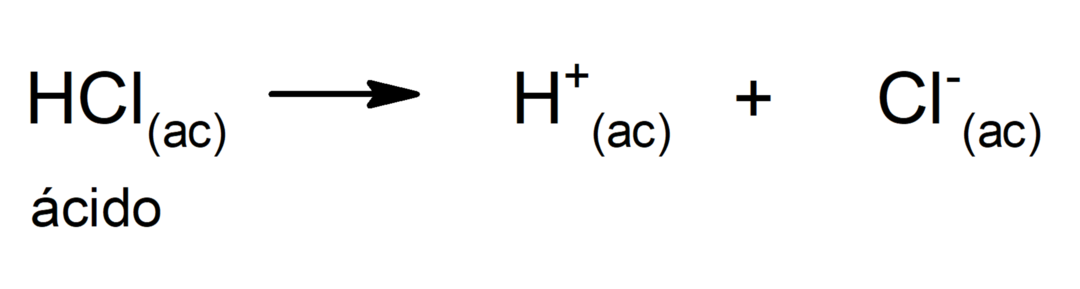
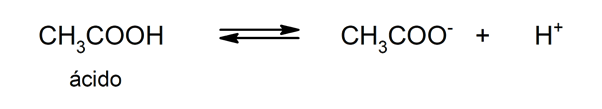
Hapete kasutamine
Hapetel on palju kasutusviise, nii tööstuses kui ka kodus. Neid kasutatakse sageli lisaainete ja säilitusainetena toit, kosmeetika, joogid jne. Mõningaid happelisi tahkeid aineid kasutatakse katalüsaatorid (keemiliste reaktsioonide kiirendid) naftakeemia- või paberitööstuses.
On ka happeid, mida kasutatakse desinfektsioonivahendid (karboolhape, salitsüülhape). Lisaks saab neid kasutada auto akudes elektrolüütidena, nagu väävelhappe puhul. Viimast tugevat hapet kasutatakse sageli ka mineraalid, näiteks kivimfosfaatidest väetiste tootmisel.
Tasub selgitada, et teatud aineid saab lahustada ainult happelises keskkonnas ja teatud reaktsioonid toimuvad ainult sellistes tingimustes. Lämmastikhape ja ammoniaak muudavad ammooniumnitraadi, mis on ka kultuuride jaoks oluline väetis.
Hapete näited
Allpool on näitena toodud kakskümmend hapet:
- Perkloorhape (HClO4). See on tugev happeline vedelik a temperatuur keskkond, väga oksüdeeriv.
- Lämmastikhape (HNO3). See on tugev ja intensiivselt oksüdeeruv hape, mida kasutatakse teatud lõhkeainete ja ka lämmastikväetiste valmistamiseks.
- Askorbiinhape (C6H8VÕI6). See on C-vitamiin, mis on tervisele nii vajalik. See on antioksüdatiivse toime tõttu kaitsev aine.
- Vesinikkloriidhape (HClac)). See on ainus tugev hape, mida inimkeha sünteesib, protsess, mis toimub spetsiifiliselt maos, et viia läbi toit seedeprotsessis.
- Viinhape (C4H6VÕI6). See on valge kristalne pulber, seda kasutatakse kihisevate jookide valmistamiseks, pagari-, veini- ja farmaatsiatööstuses. Mõnes retseptis sisalduv hambakreem on viinhape.
- Fluorhape (HFac)). Klaasi ründamise võime tõttu kasutatakse seda kristallide nikerdamisel ja graveerimisel.
- Väävelhape (H2SW4). See on tugev happe par excellence, seda on lugematuid rakendusi erinevates tööstusharudes ja sünteesiprotsessid.
- Trifluoroäädikhape (C2HF3VÕI2). See on hea lahusti paljudele orgaanilised ühendid.
- Fosforhape (H3PO4). Seda leidub (väikestes kontsentratsioonides) erinevates koolajookides. Seda peetakse tervisele kahjulikuks, kuna see soodustab katlakivi eemaldamist.
- Äädikhape (CH3COOH). See on äädika põhikomponent. Selle tekitatud happesus muudab selle laialdaselt kasutatavaks toidukaitsevahendiks.
- Fluoroantimonhape (SbHF6). See on tugevaim teadaolev ülihape, ületades puhta väävelhappe happesuse 10 võrra19.
- Kroomhape (H2CrO4). See on tumepunane pulber, see osaleb kroomimisprotsessis. Seda kasutatakse ka keraamika glasuurimiseks.
- Indoläädikhape (C10H9MITTE2). See on auksiinide peamine esindaja, mis on oluline taimed.
- Deoksüribonukleiinhape (DNA). See on see, mis hoiab elu võtit, sest see moodustab geenid, mis reguleerivad lugematute valkude sünteesi.
- Trikarboksüülhapped. Need sisaldavad karboksüülhapete rühma, millel on kolm karboksüülrühma (-COOH). Sidrunhape (C6H8VÕI7) See on üks neist.
- Sipelghape (CH2VÕI2). See on orgaaniliste hapete seas kõige lihtsam. Pikaajaline kokkupuude selle happega võib põhjustada hingamispuudulikkust ja surma.
- Glükoonhape (C6H12VÕI7). Selle happe soolasid kasutatakse laialdaselt klaasnõude puhastamisel.
- Piimhape (C3H6VÕI3). See on oluline osa biokeemilistest protsessidest.
- Bensoehape (C7H6VÕI2). See on iseloomuliku lõhnaga hape, mida kasutatakse laialdaselt toiduainete säilitamiseks, mis vajavad a pH hape.
- Õunhape (C4H6VÕI5). Ravimitööstuses kasutatakse seda lahtistite tootmiseks laialdaselt.
- Süsinikhape (H2CO3). Mõnes kohas on see osa koobaste moodustamise protsessist. Seda leidub gaseeritud jookides.



