Keemilise energia näide
Keemia / / July 04, 2021
The Keemiline energia on see, mis pärineb keemilistest reaktsioonidest. Keemiliste liikide vastastikune mõju põhjustab purunemist ja / või sidemete tekkimist, mis tähendab vastavalt energia eraldumist või neeldumist. Keemilist energiat nimetatakse vabanenud energiaks, mida saab kasutada näiteks soojusenergia ja elektrienergiana.
Energia keemilistes reaktsioonides
Keemilist energiat saab maksimaalses väljenduses kahest peamisest allikast: põlemis- ja elektrolüütilised lahused. Teiselt poolt on inimkeha tasandil võimalik saada energiat toidu keemilise lagunemise kaudu.
Põlemisenergia
Näiteks kui kütusemetaan CH4, kõige lihtsam süsivesinik, hakkab põlema hapniku oksüdeerija juuresolekul, see laguneb, moodustades süsinikdioksiidi CO tooteid.2 ja vesi H2VÕI. Lisaks vabastab vesinikuaatomite sidemed süsiniku aatomitega energia soojuse kujul.
CH4 (g) + 2O2 (g) → CO2 (g) + 2H2 O (l) ∆H = -212,8 Kcal / mol
Metaani põlemise võrrand. Selle reaktsiooni kuumust tähistab ΔH. Negatiivne märk näitab energia vabanemist. Reaktsioon on eksotermiline.
 Metaangaasi põletamine. Reaktsioon avaldub leegiga.
Metaangaasi põletamine. Reaktsioon avaldub leegiga.
Orgaaniliste ühendite põlemiskuumuse näited temperatuuril 25 ° C
Ühend |
Valem |
ΔH (Kcal / mol) |
Metaan (g) |
CH4 |
-212.80 |
Etaan (g) |
C2H6 |
-372.82 |
Propaan (g) |
C3H8 |
-530.60 |
n-butaan (g) |
C4H10 |
-687.98 |
n-pentaan (g) |
C5H12 |
-845.16 |
Etüleen (g) |
C2H4 |
-337.23 |
Atsetüleen (g) |
C2H2 |
-310.62 |
Benseen (g) |
C6H6 |
-787.20 |
Benseen (l) |
C6H6 |
-780.98 |
Tolueen (l) |
C7H8 |
-934.50 |
Naftaleen (id) |
C10H8 |
-1,228.18 |
Sahharoos (id) |
C12H22VÕI11 |
-1,348.90 |
Metanool (l) |
CH3Oh |
-173.67 |
Etanool (l) |
C2H5Oh |
-326.70 |
Äädikhape (l) |
CH3COOH |
-208.34 |
Bensoehape (d) |
C6H5COOH |
-771.20 |
Selleks, et kütus annaks kogu põlemissoojuse, mida see suudab, peab see olema gaasilises olekus. Nagu tabelist näha, annab vedel benseen põlemissoojuse, mis on 6,22 Kcal / mol väiksem kui gaasilise benseeni eraldatav. See tähendab, et vedeliku asemel gaasiks muutmiseks tuleb investeerida 6,22 Kcal / mol.
Klõpsake lisateabe saamiseks saidil Kütused.
Elektrolüütiliste lahuste energia
Elektrolüütide juht on keskkond, milles osaleb üks või mitu ioonset liiki, mis on hajutatud koos oma elektrilaenguga, võimaldades elektrivoolul selle läbi minna Põhiseadus. Elektrolüütilised lahendused on elektrolüütide juhid.
Elektrolüütide juhid hõlmavad lisaks elektrolüütide lahustele ka Sulatatud soolad ja ka mõned tahked soolad, näiteks naatriumkloriid NaCl ja hõbenitraat AgNO3.
Elektroniülekanne toimub ioonse migratsiooni abil, positiivse ja negatiivse suunas elektroodide suunas. See ränne hõlmab lisaks elektrienergia ülekandmisele ka aine transportimist juhi ühest osast teise.
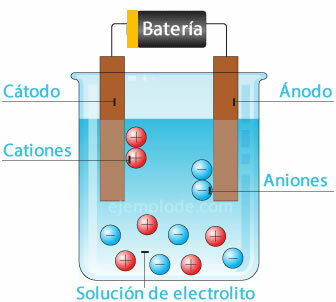 Elektrokeemiline element
Elektrokeemiline element
Potentsiaalallika ühendamine metallelektroodidega (katood ja anood) ja nende uputamine a Vesilahus, elektronid liiguvad läbi anoodi, et pääseda lahusest positiivsesse poolusesse purskkaev. Nii on see näiteks kloriidiooniga, mis vabaneb selle elektronist ja juba neutraalse laenguga liitub see teise kloori aatomiga, moodustades diatoomse molekuli. Kloorgaas väljub lahusest.
2Cl- = 2Cl + 2e-
Allika negatiivsest poolusest lahkuvad elektronid paigutatakse sukeldatud katoodi. Vesilahuses esinevad liigid (ioonid) võtavad elektronid katoodist. Näiteks võtsid vett moodustavad vesinikuioonid, olles olnud positiivses laengus elektron, mis neutraliseeritakse ja ühendatakse teise vesinikuaatomiga, moodustades molekuli diatoomiline. See pääseb lahusest vesinikgaasina.
2H+ + 2e- = 2H
2H = H2 g)
See elektronide vahetus võib toetada autoakude tööd, mis koosnevad väävelhappe H lahusesse sukeldatud plii Pb elektroodidest.2SW4.
See sama energia saadakse igat tüüpi patareides, mida käsitletakse kodusel tasandil: 9V, AA, AAA, D, kui tuua mõned näited.
Toiduenergia
Inimesed omastavad energia, mis vabaneb, lagundades meie kehas söödavat toitu. See energia on see, mida meie keha kasutab teadvustamata funktsioonide (seedimine, südamelöögid, raku funktsioonid) ja nende jaoks, mida me täidame.
Kuni teil pole intensiivset füüsilist koormust ja ainevahetus on aeglane, on soovitatav tarbida regulaarselt kaloreid, sest kõrge Kompleksseid lipiide ja süsivesikuid, millel on väga suured struktuurid, on raskem lagundada, mille tulemuseks on Energia. Sel juhul oleks mõju hetkeliselt vastupidine.
Puuvilju on soovitatav tarbida siis, kui peate töötama öösel, sest puuviljad sisaldavad fruktoosi, lihtne süsivesik, mida on lihtne lagundada ja millel on energia pärast teie tarbimine.
Keemiline energia ja selle teisendused
Termoelektrijaamad
Raskekütuseid kasutatakse termoelektrijaamades kõrge ja pikaajalise kütteväärtusega. Üldiselt on see kütteõli (kütteõli). Põlemine, mis on protsessi keemiline etapp, toimib katla kütteainena, mis tekitab küllastunud auru. See aur väljub auru jaotusvõrgu kaudu rõhu all ja hakkab generaatoriturbiinid liikuma. Need seadmed toodavad vastava elanikkonna varustamiseks elektrienergiat.
Keemiline energia → Mehaaniline energia → Elektrienergia
Autotööstus
Autod sõltuvad toiteallikast, milleks on Aku. Patareis on juba teada elektrolüütiline juhtivus, mis toidab süütesüsteemi, kriipsutarvikuid ja lisatoiteallikaid. Tänu sellele olemasolevale elektrile saab auto liikuda, et viia juht soovitud asukohta.
Keemiline energia → Elektrienergia → Mehaaniline energia
