Perioodilise seaduse mõiste
Miscellanea / / July 04, 2021
Florencia Ucha poolt, juuli. 2012
 The seadus perioodiline kas ta on asutamine perioodilisustabel elementidest, nagu skeem universaalne, mis korrastab, klassifitseerib ja jaotab olemasolevaid erinevaid keemilisi elemente nende omaduste ja omaduste suhtes.
The seadus perioodiline kas ta on asutamine perioodilisustabel elementidest, nagu skeem universaalne, mis korrastab, klassifitseerib ja jaotab olemasolevaid erinevaid keemilisi elemente nende omaduste ja omaduste suhtes.
Alus, millel paikneb elementide perioodiline tabel
Vahepeal näeb perioodiline seadus ette, et eespool nimetatud elementide füüsikalised ja keemilised omadused on kaldunud süstemaatilisele kordamisele, kui elementide aatomite arv suureneb.
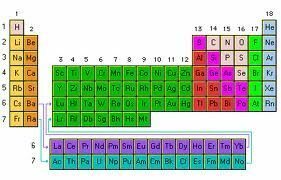
Perioodiline tabel: keemiliste elementide korraldus kasvavas järjekorras vastavalt nende aatomite arvule
Nii kuulus elementide tabel, mida uurime koolFüüsika ja keemia õppeainetes on see skeem, mis käsitleb keemiliste elementide järjestamist vastavalt nende aatomite arvu kasvavale järjekorrale.
Tabeli vertikaalseid veerge nimetatakse rühmadeks ja need sisaldavad sama aatomvalentsiga elemente ning seetõttu on neil sarnased omadused, kui horisontaalsetes ridades, mida nimetatakse perioodideks, on rühmitatud elemendid, millel on erinevad omadused, kuid millel on sarnane mass.
Kuidas neid teadmisi arendati: konkreetsed ja järkjärgulised sündmused
Tuleb märkida, et kõik need füüsikale ja keemiale omased mõisted töötati välja XIX sajandi jooksul järk-järgult.
Peame ütlema, et mõned elemendid nagu hõbe (Ag), kuld (Au), vask (Cu), plii (Pb) ja elavhõbe (Hg) olid juba iidsetest aegadest täiuslikud teadmised, Esimene elemendi teaduslik avastus leidis aset 17. sajandil, kui alkeemik Henning Brand tuvastas esmakordselt fosfori (P).
Järgmisel sajandil, see tähendab 18. sajandil, hakati tundma uusi elemente, millest kõige olulisemad olid gaasid, tänu pneumaatilise keemia arengule, sealhulgas hapnik (O), lämmastik (N) ja vesinik (H).
Umbes sel ajal kirjutas prantsuse keemik Antoine Lavoisier nimekirja lihtsatest ainetest, milles oli juba 33 elementi.
XIX sajandi alguses käivitas elektriaku leiutamine keemiliste nähtuste uurimise uus ja see lõpuks avastas rohkem elemente, nagu leelismetallid ja leeliseline-mullane.
Aastaks 1830 oli 55 elementi juba tuvastatud.
Üheksateistkümnenda sajandi keskel leiti seadme, nimega spektroskoop, leiutamisel rohkem elemente, eriti need, mis on seotud nende spektrijoone esitanud värviga, sealhulgas tseesium, tallium ja rubiidium nimetage mõnda.
Spektroskoop on instrument, mida kasutatakse a spekter, kuna see on kiirguste, helide või lainete nähtuste seeria hajumise tulemus.
Teatud elementide sarnasus keemiliste ja füüsikaliste omaduste osas viis mõneni tollased teadlased otsustasid neid süstemaatiliselt tellida, teatud järgi rühmitada kriteeriumid.
The eelkäija Kõige kaugem, mis meil seadusest on, on tuntud Oktaavide seadus, mille on välja töötanud inglise keemik John Alexander Newlands, kes tegi ettepaneku äratada suur uudsus, et iga kaheksa elemendi puhul leiame end sarnaste omaduste ees.
See oli tema jaoks käivitus oma perioodilise tabeli koostamiseks, mis ametlikult avaldati 1863. aastal.
Nagu oleksite a võistlus postitustest võttis kinda selles mõttes kätte teine keemik, antud juhul Sakslane Julius Lothar Meyer, kes kasutas lähtepunktina Newlandsi tulemusi, määras aastal 1870 elementide aatomimahud.
Kui ta oli arvutanud aatommassid ja joonistanud need välja, oli ta võimeline maailmale demonstreerima teadus kinnitab, et aatommass tähendab omaduste suurenemist füüsiline.
Ja peaaegu samaaegselt Meyeri teostega, Venemaal sündinud keemik Dimitri Mendelejev avaldab esimene perioodiline tabel, pekses Meyerit, kes teeks seda aasta hiljem ja seetõttu on tema see, kes on jäänud selle loojana teenimise juurde.
Mendelejev sordiks elemendid kasvavas järjekorras aatommass mida nad esitlevadVahepeal paigutas ta samasse veergu need, kellel olid mingid omadused.
Tasub mainida, et selleks ajaks oli teada juba 63 elementi olemasolevast 90-st.
Laud valmis 19. sajandi lõpus koos teise rühmaga, mida nimetati nulliks ja mis koosnes väärisgaasidest.
Perioodilise õiguse teemad


