20 Esimerkkejä kemiallisista ilmiöistä
Sekalaista / / July 04, 2021
kemialliset ilmiöt (tai kemialliset reaktiot) ovat niitä ilmiöitä, joissa aineessa tapahtuu muutoksia, ja muodostuu uusia "tuotteiksi" kutsuttuja aineita ja muut "reagoivat aineet" hajoavat. Esimerkiksi: puun laho, paperin polttaminen, kompostointi.
Kemialliset reaktiot voivat olla spontaani (reaktiot, jotka tapahtuvat ilman energian tai katalyyttien tarvetta) tai ei spontaani (reaktiot, jotka tarvitsevat energian, katalyyttien tai jonkin ulkoisen puuttumisen). Monta kertaa reaktion tapahtumiseksi on välttämätöntä, että reagensseilla on a lämpötila erityinen, a pH asetettu paine-arvo jne.
Voi myös olla välttämätöntä hallita nopeus johon kemialliset reaktiot tapahtuvat. katalyytit Ne ovat aineita, jotka lisätään kemialliseen reaktioon sen nopeuden lisäämiseksi, kun taas estäjät ovat aineita, jotka hidastavat kemiallisten reaktioiden nopeutta. Muita kemiallisen reaktion nopeuteen vaikuttavia tekijöitä ovat lämpötila, paine, reagenssien pitoisuus ja itse reaktion luonne.
Se voi palvella sinua:
Kemiallisten ilmiöiden tyypit
Kemialliset reaktiot voivat olla:
Epäorgaaniset reaktiot. Puuttua asiaan epäorgaaniset yhdisteet ja voidaan luokitella seuraavasti:
- Merkitys, jossa reaktio tapahtuu.
-
Palautuvat reaktiot. Ne esiintyvät molemmilla tavoilla, joten tuotteet voivat hajota ja muodostaa reaktantit uudelleen.
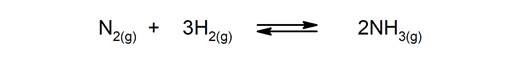
-
Palauttamattomat reaktiot. Ne tapahtuvat vain yhdellä tavalla.

-
Palautuvat reaktiot. Ne esiintyvät molemmilla tavoilla, joten tuotteet voivat hajota ja muodostaa reaktantit uudelleen.
- Reagoivan hiukkasen tyyppi.
-
Happo-emäs-reaktiot. H-ioninsiirto tapahtuu+.

-
Hapettumista vähentävät reaktiot. Yksi reagoivista aineista hapettuu (lisää sen määrää) hapettuminen), kun taas toinen on vähentynyt (sen hapetusluku pienenee). Näissä reaktioissa tapahtuu elektroninsiirto.

-
Happo-emäs-reaktiot. H-ioninsiirto tapahtuu+.
- Reaktionopeus.
-
Nopeat reaktiot. Ne tapahtuvat hyvin lyhyessä ajassa.
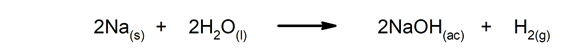
-
Hitaat reaktiot Niiden valmistuminen kestää kauan.
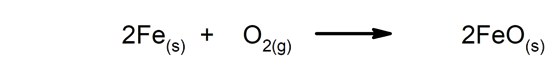
-
Nopeat reaktiot. Ne tapahtuvat hyvin lyhyessä ajassa.
- Sen lähettämän tai absorboiman energian muoto.
-
Eksotermiset reaktiot. Niiden tapahtuessa ne vapauttavat lämpöä.
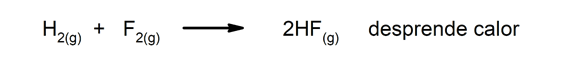
-
Endotermiset reaktiot. Kun ne tapahtuvat, ne imevät lämpöä.

-
Eksolumiiniset reaktiot. Kun ne tapahtuvat, ne lähettävät valoa.

-
Endoluminous reaktiot. Tapahtumaan he tarvitsevat valoa.

-
Eksotermiset reaktiot. Niiden tapahtuessa ne vapauttavat lämpöä.
- Transformaation tyyppi.
-
Synteesi- tai lisäysreaktiot. Kaksi ainetta muodostaa uuden aineen.
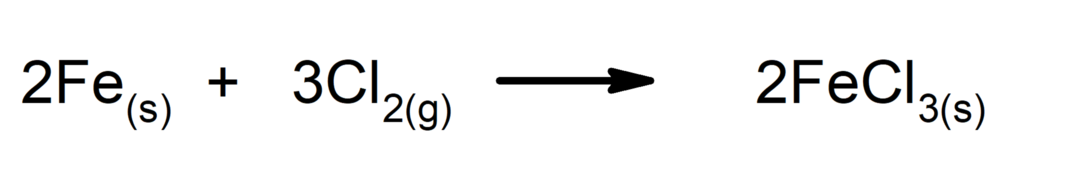
-
Hajoamisreaktiot. Yksi tai useampi aine hajoaa yksinkertaisimpiin ainesosiinsa.
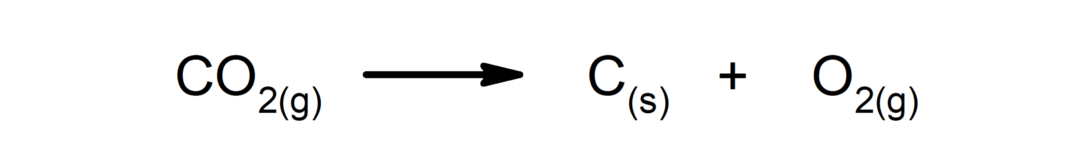
-
Siirtymä- tai korvausreaktiot. Yksi elementti tai yhdiste korvaa toisen yhdisteessä vapauttaen sen.
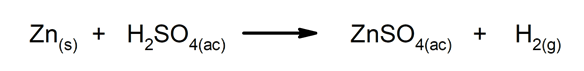
-
Kaksoiskorvausreaktiot. Kaksi yhdistettä vaihtaa elementtejä tai yhdisteitä samanaikaisesti.

-
Synteesi- tai lisäysreaktiot. Kaksi ainetta muodostaa uuden aineen.
Orgaaniset reaktiot. Ne ovat reaktioita, joihin orgaaniset yhdisteet puuttuvat. Heillä on monia luokituksia reagoivan orgaanisen yhdisteen tyypin ja sen läpi tapahtuvan reaktion tyypin perusteella. Joitakin esimerkkejä ovat:
-
Alkaanien halogenointi. A: n vety alkaani halogeenilla.
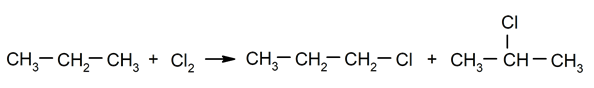
-
Alkaanien polttaminen. Alkaani reagoi hapen kanssa muodostaen hiilidioksidia ja vettä, jos palaminen on valmis.
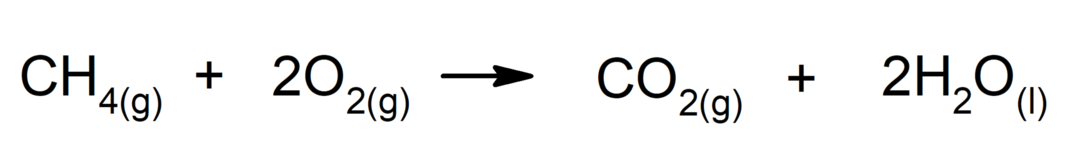
-
Halogenointi alkeenit. Yksi tai molemmat kaksoissidokseen osallistuvien hiilien vedyt korvataan halogeeneilla.
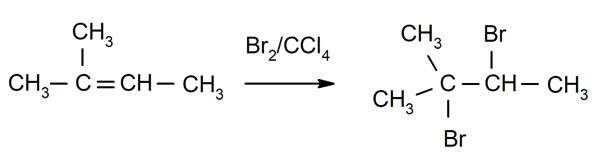
-
Alkaanien hydraus. Vetyjä lisätään kaksoissidoksen mukana oleviin hiileihin vastaavan alkaanin muodostamiseksi.
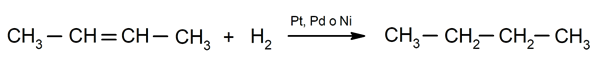
Kemiallisten ilmiöiden merkitys
Monet kemialliset ilmiöt ylläpitää elämää elävien olentojen, kuten ihmisen ruoansulatuksen ja eläimet, fotosynteesi kasveissa ja hengitys molemmissa.
Toinen erittäin tärkeä kemiallinen prosessi, erityisesti mikro-organismit, on käyminen, jota yleensä käytetään ruokaa kuten juustot, jogurtit, viinit ja oluet.
Kaikki lisääntyä ja kasvu a elävä olento Siihen liittyy kemiallisia reaktioita, joita siinä tapahtuu, joskus tietyt ympäristöolosuhteet stimuloivat.
Esimerkkejä kemiallisista ilmiöistä
Ympärillämme on lukuisia kemiallisia ilmiöitä tai prosesseja, jotka sisältävät niitä:
- Puun mätää
- Palaminen paperia
- Vastus antibiootit bakteerit
- Maito, joka muuttuu hapan
- Desinfioi haava alkoholia
- Hedelmäsuolan käyttö närästyksen torjunnassa
- Kynttilän polttaminen
- Veren hyytymistä
- Lihasten väsymys intensiivisen liikunnan jälkeen
- Kuolema ötökät hyönteismyrkkyillä
- Roquefort-juuston hankkiminen
- Siiderin hankkiminen
- Jogurtin saaminen
- Kompostointi
- Ensilage
- Bioetanolin saaminen melassista
- Turvotetut tölkit
- Mätä muna
- Arinan ruostuminen
- Biodieselin saaminen palmuöljystä
Kemialliset ilmiöt teollisuudessa
Tietyt kemialliset ilmiöt ovat myös avainasemassaala. Ensinnäkin polttaminen hiilivedyt (kuten bensiini, diesel tai kerosiini) tuottaa Energia käyttää koneita, jotka käsittelevät lukemattomia teollisia prosesseja.
Toisaalta terästeollisuus, paperi, muovit, rakennusmateriaalit, maalit, lääkkeet, tuotteet agro jne. perustuvat erilaisiin kemiallisiin ilmiöihin, kuten galvanointi, elektrolyysi ja monet toiset enemmän.
Sukupolvi uusia energialähteitä (kuten biodieseli ja bioetanoli) perustuu myös tämän tyyppiseen ilmiöön.
Energian muutos
Kemiallisissa ilmiöissä on yleistä energian muutos. Esimerkiksi kun tietyn molekyylin sidoksiin sisältyvä kemiallinen energia muunnetaan sähköenergiaksi tai vapautetaan lämpö (tämä tapahtuu eksotermisissä ilmiöissä, kuten esimerkiksi kloorivetyhapon sekoittuessa sinkkiin), Energia. Sama tapahtuu, kun valoenergia siepataan ja muunnetaan kemialliseksi energiaksi.
Jotkut kemialliset prosessit vaativat lämpöä toimiakseen ja niitä kutsutaan "endotermisiksi". Toiset vaativat katalyyttien tai kofaktorien läsnäoloa.

