30 Esimerkkejä alkoholeista
Esimerkkejä / / November 06, 2023
The alkoholit ovat orgaaniset kemialliset yhdisteet jotka sisältävät rakenteessa funktionaalisen hydroksyyliryhmän (-OH) kiinnittyneenä hiileen (-C). Ryhmää (-C – OH) kutsutaan "karbinoliksi". Joitakin esimerkkejä alkoholeista ovat: metanoli, etanoli ja 1-propanoli.
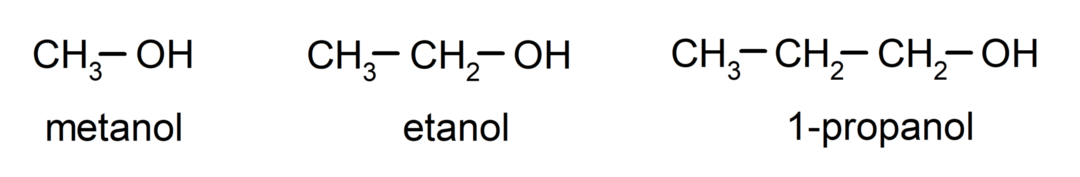
Alkoholit ovat kemiallisia yhdisteitä, joilla on erilaisia käyttötarkoituksia jokapäiväisessä elämässä, koska niillä on antibakteerisia ja antiseptisiä ominaisuuksia. Toisaalta ne voivat olla vaarallisia ihmisten terveydelle hallitsemattomasti nautittuna.
Samoin ihmiset eivät voi niellä kaikkia alkoholeja.
- Katso myös: Amiinit ja ketonit
Alkoholien tyypit
Riippuen hiiliatomien lukumäärästä, johon hiiliatomi, johon hydroksyyliryhmä on kiinnittynyt, on kiinnittynyt, alkoholi voi olla:
- Ensisijainen alkoholi. Hiiliatomi, johon hydroksyyliryhmä on kiinnittynyt, on myös kiinnittynyt yhteen hiiliatomiin. Esimerkiksi:
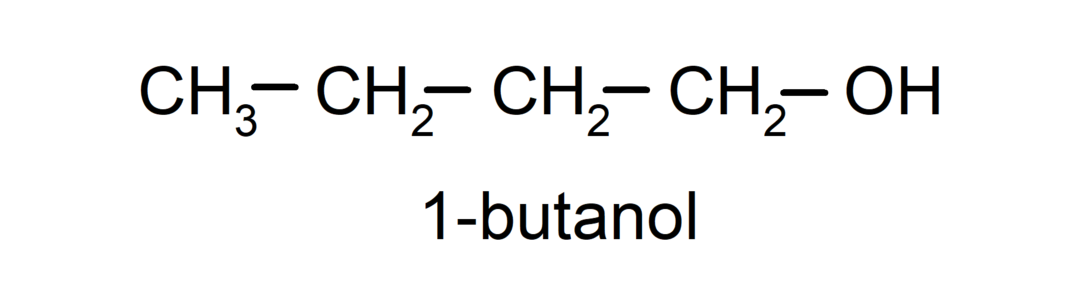
- Toissijainen alkoholi. Hiiliatomi, johon hydroksyyliryhmä on kiinnittynyt, on myös sitoutunut kahteen muuhun hiiliatomiin. Esimerkiksi:
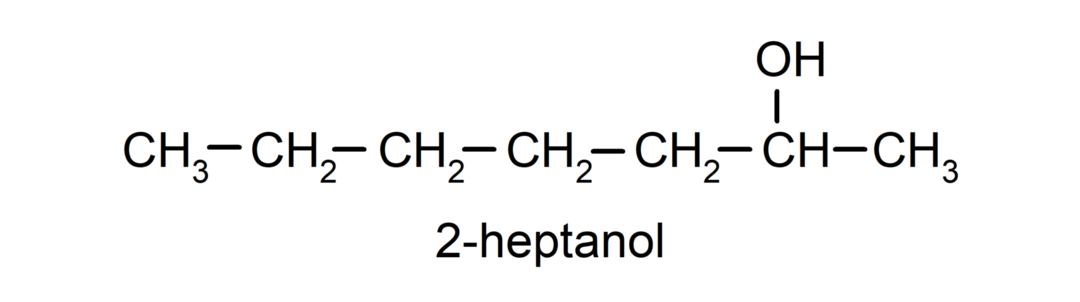
- Tertiäärinen alkoholi. Hiiliatomi, johon hydroksyyliryhmä on kiinnittynyt, on myös kiinnittynyt kolmeen hiiliatomiin. Esimerkiksi:
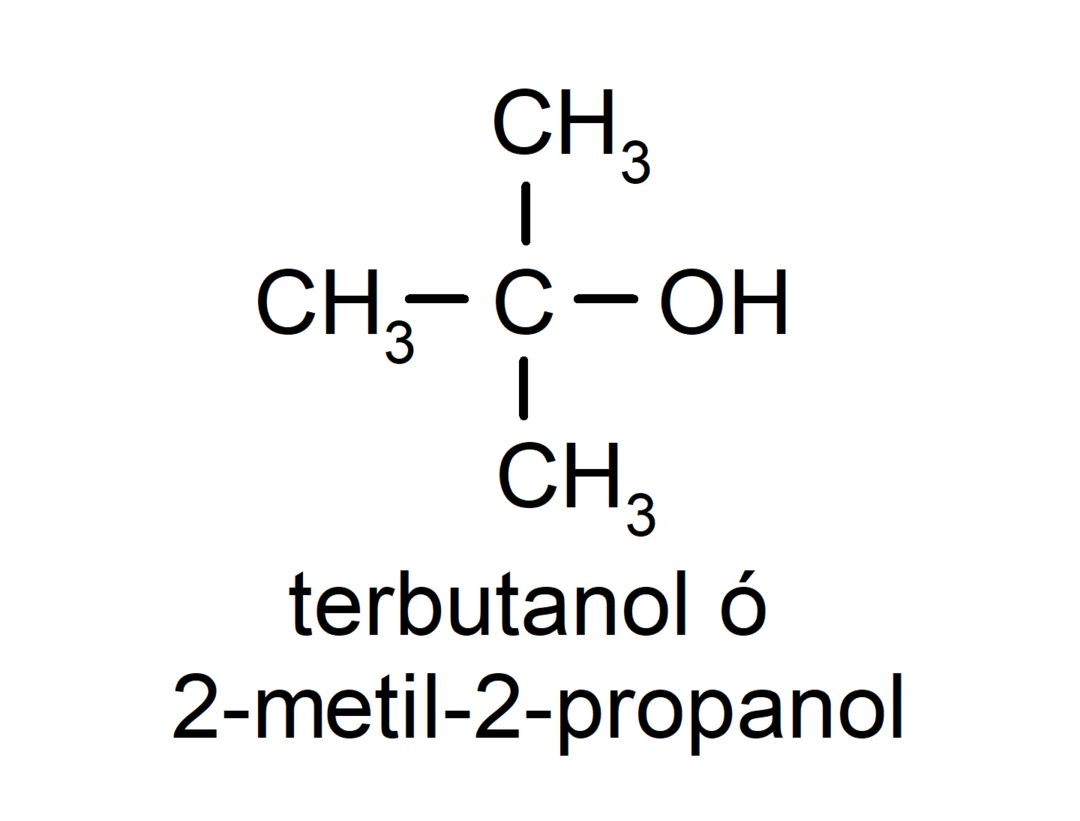
Riippuen siinä olevien hydroksyyliryhmien lukumäärästä alkoholi voi olla:
- Diol. Sen rakenteessa on kaksi hydroksyyliryhmää. Esimerkiksi:
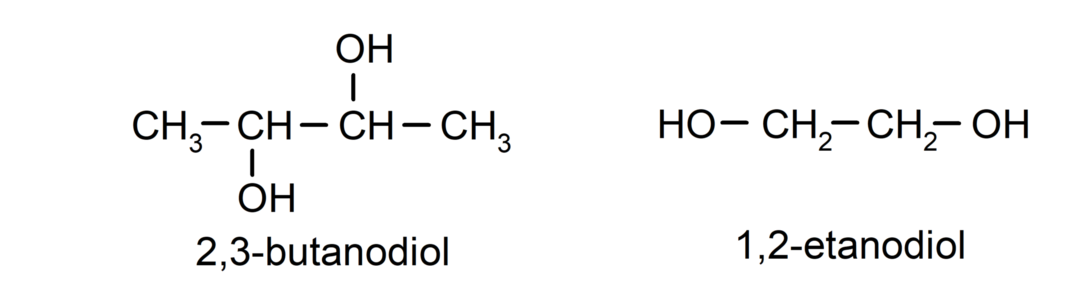
- Triol. Sen rakenteessa on kolme hydroksyyliryhmää. Esimerkiksi:
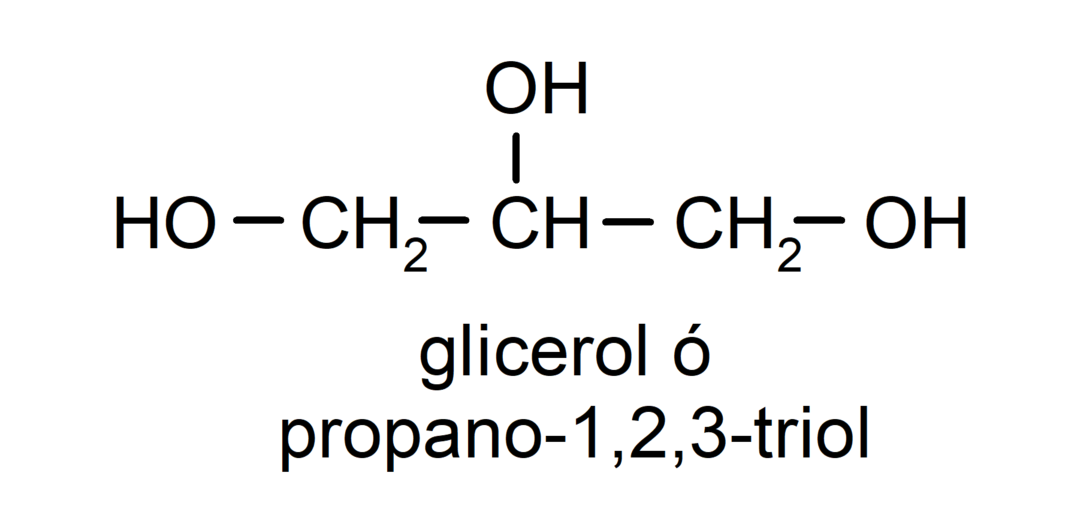
- polyalkoholi. Sen rakenteessa on monia hydroksyyliryhmiä. Esimerkiksi:
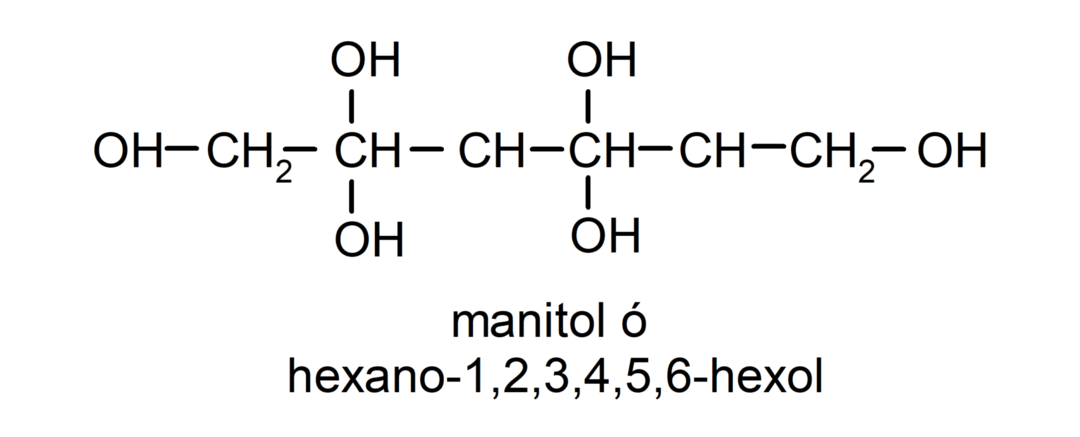
Alkoholien fysikaaliset ominaisuudet
Jotkut alkoholien fysikaalisista ominaisuuksista ovat:
- Kiehumispiste. Alkoholien kiehumispiste on melko korkea johtuen hydroksyyliryhmän läsnäolosta, mikä mahdollistaa vetysidosten muodostumisen. Lisäksi mitä enemmän hydroksyylifunktionaalisia ryhmiä on hiiliketjussa, sitä korkeampi on Kiehumispiste alkoholeista.
- Vastakkaisuus. Alkoholit ovat melko polaarisia yhdisteitä.
- Liukoisuus. Pienen molekyylipainon alkoholit liukenevat veteen. Toisaalta mitä suurempi alkoholien hiiliketju on, sitä pienempi on niiden liukoisuus veteen. Lisäksi mitä enemmän hydroksyyliryhmiä alkoholeissa on, sitä suurempi on niiden vesiliukoisuus.
- Kokoamistila. Useimmat alkoholit ovat nestemäisiä huoneenlämpötilassa (25 ºC) ja niillä on ominaista hajua.
Alkoholien kemialliset ominaisuudet
Jotkut alkoholien kemiallisista ominaisuuksista ovat:
- Alkoholit käyttäytyvät kuten hapot ja emäkset.. Niiden käyttäytyminen happoina voidaan nähdä reaktioissa aktiivisten metallien kanssa vetykaasun vapauttamiseksi ja alkoksidejen muodostamiseksi.

Niiden käyttäytyminen emäksinä voidaan nähdä reaktioissa, kuten metanolin reaktio bromivedyn kanssa metyylioksoniumbromidin muodostamiseksi.
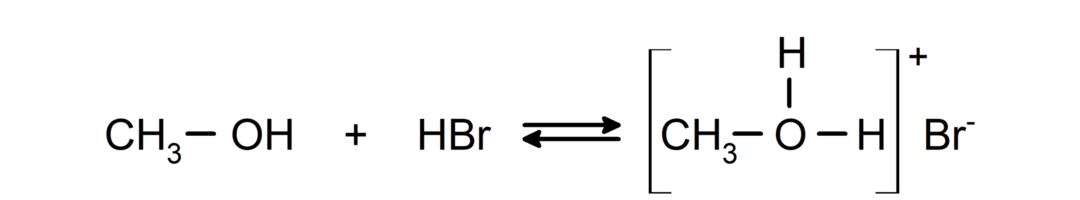
- Alkoholit käyvät läpi halogenointireaktioita. Ne reagoivat vetyhalogenidien kanssa muodostaen alkyylihalogenideja.
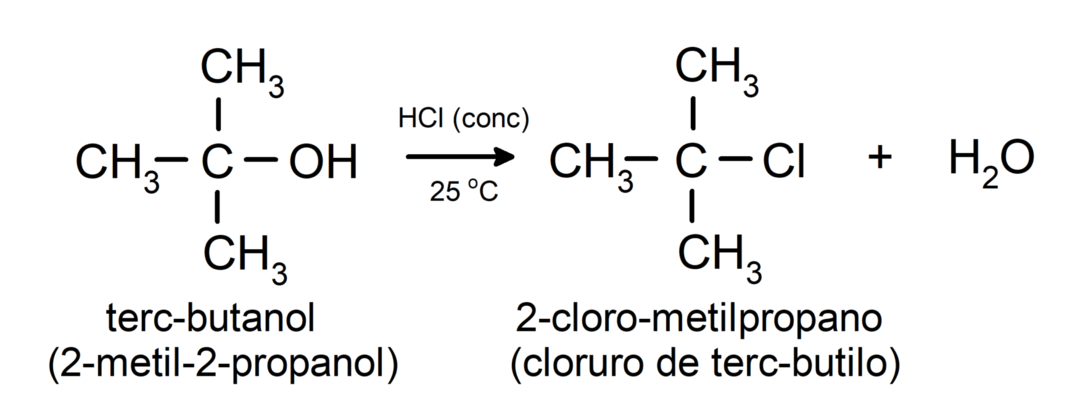
-
Alkoholit käyvät läpi hapettumisreaktioita kun ne reagoivat tiettyjen hapettavien yhdisteiden kanssa. Hapettumisreaktioiden tuotteet riippuvat reagoivan alkoholin tyypistä, eli onko se primääristä, sekundaarista vai tertiääristä.
Primaarisen alkoholin hapetus aldehydiksi tai karboksyylihapoksi.
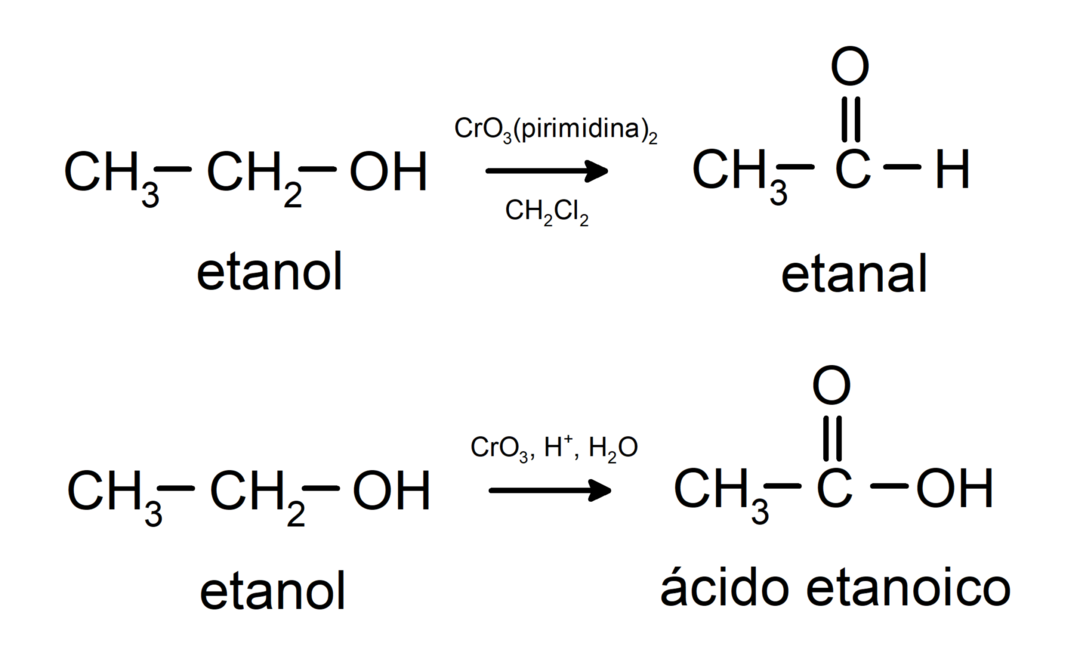
Sekundaarisen alkoholin hapettuminen ketoniksi.
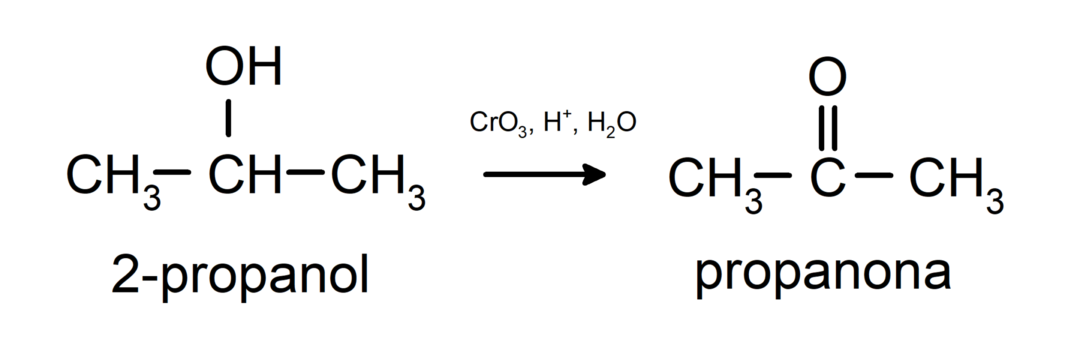
Tertiääriset alkoholit eivät hapetu tavallisten hapettimien kanssa. Erittäin vahvoilla hapettimilla ne voidaan muuttaa alkeeneiksi, jotka voidaan sitten hapettaa.
Alkoholit, joissa on kaksi hydroksyyliryhmää vierekkäisissä hiileissä, hapetetaan lyijytetra-asetaatilla kahden ketonin muodostamiseksi.
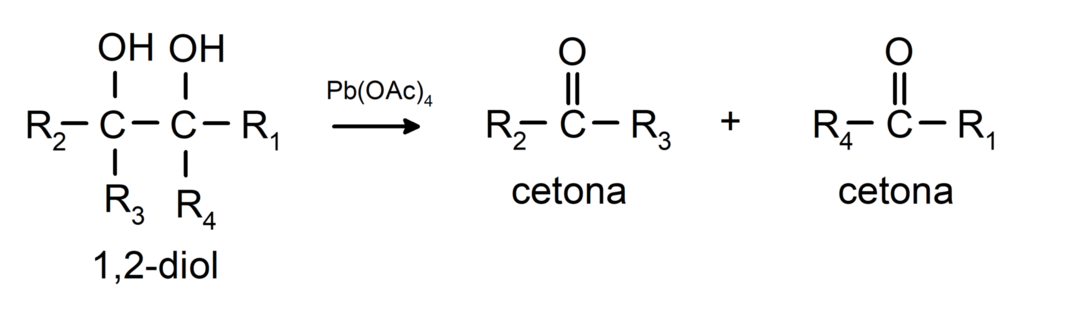
- Alkoholit käyvät läpi dehydrausreaktioita. Nämä reaktiot tapahtuvat vain primääristen ja sekundaaristen alkoholien kanssa, jotka joutuessaan alttiiksi korkeille lämpötiloille katalyyttien läsnä ollessa vapauttavat vetyä.
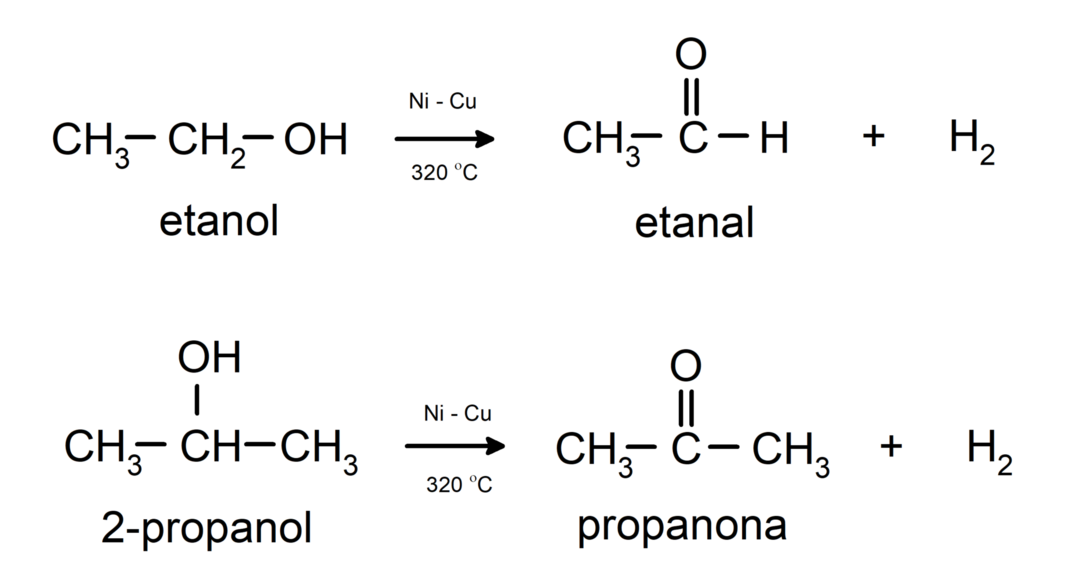
- Alkoholit käyvät läpi kuivumisreaktioita. Alkoholit dehydratoituvat muodostaen vastaavia alkeeneja. Tämä reaktio tapahtuu hapon ja välilämpötilojen läsnä ollessa.
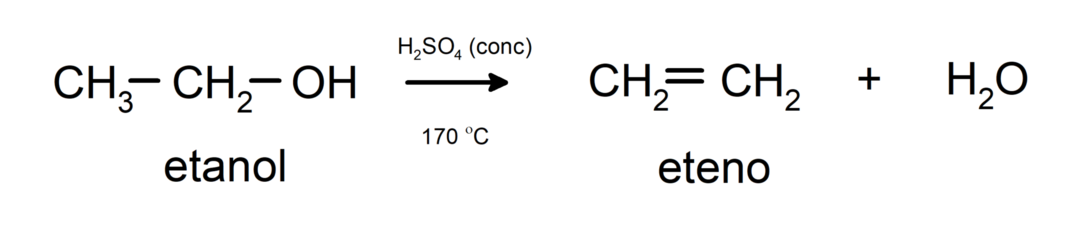
Alkoholin nimikkeistö
IUPAC: n (International Union of Pure and Applied Chemistry) laatiman nimikkeistön mukaan alkoholit nimetään seuraavien sääntöjen mukaisesti:
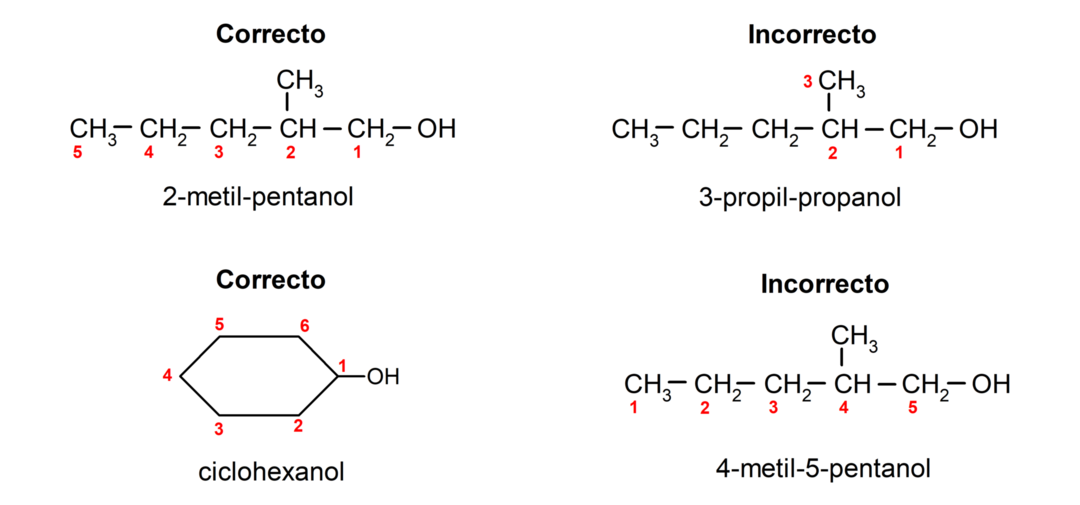
- Hydroksyyliryhmän asema valitaan ottaen huomioon, että se on pienin mahdollinen määrä hiiliketjussa. Jos alkoholin rakenne on syklinen, otetaan huomioon se 1-asema hiilessä, johon hydroksyyliryhmä on kiinnittynyt, ja sen nimeämiseen käytetään etuliitettä syklo-.
- Alkoholin nimi kirjoitetaan etuliitteillä, jotka osoittavat atomien lukumäärän hiiliketjussa, ja lisäksi sijoitetaan jälkiliite -ol.
- Jos alkoholin rakenteessa on haaroja, päähiiliketjuksi valitaan pisin ketju, joka sisältää myös hydroksyyliryhmän.
Perinteisen nimikkeistön mukaan alkoholit nimetään kirjoittamalla sana "alkoholi" ja kirjoittamalla sitten alkoholin nimi. alkaani, joka vastaa hiiliketjua, mutta alkaanin -aanipäätteen käyttämisen sijaan pääte -yllistä.
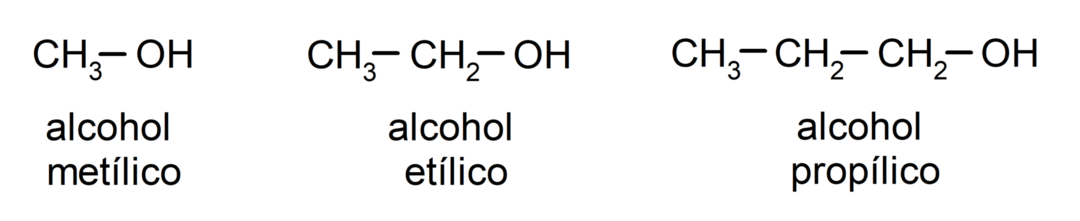
Esimerkkejä alkoholeista
- metanoli
- etanoli
- 1-propanoli
- 2-propanoli
- 1-butanoli
- 3-etyyliheksan-2-oli
- glyseroli
- fenoli
- 2-metyyli-2-butanoli
- 1,2-etaanidioli
- 1,5-heptadien-3-oli
- 3-metyyli-2-butanoli
- bentsyylimetanoli
- 3-pentanoli
- 2-metyylifenoli
- 1,2-dihydroksifenoli
- sykloheaxnol
- 1-fenyylietanoli


Alkoholien käyttö
Alkoholien yleisimmät käyttötarkoitukset ovat:
- Niitä käytetään desinfiointiaineina ja antiseptisinä aineina, koska ne estävät joidenkin kasvun mikro-organismeja tai tuhota ne. Etanolia ja isopropyylialkoholia käytetään eniten tähän tarkoitukseen.
- Niitä käytetään synteesissä eri kemialliset yhdisteet. Metanolia käytetään esimerkiksi metanolin (formaldehydin) saamiseksi.
- Niitä käytetään pakkasnesteen valmistukseen. Metanoli on yksi eniten käytettyjä tähän tarkoitukseen.
- Niitä käytetään liuottimina lääketeollisuudessa. Etanoli on yksi eniten käytetyistä tässä mielessä.
- Niitä käytetään lakkojen, väriaineiden ja musteiden liuottimina. Metanolia käytetään laajalti tähän tarkoitukseen.
- Niitä käytetään polttoaineena ja on tärkeä taipumus korvata käyttö osittain fossiiliset polttoaineet käyttämällä bioetanolipolttoainetta.
- Niitä käytetään hartsien valmistukseen. Fenolia käytetään tässä mielessä.
Alkoholin käytön vaarat
Vaikka alkoholin käyttö on nykyään yhteiskunnallisesti hyväksyttyä, sen väärinkäyttö aiheuttaa riippuvuutta ja riippuvuutta.
Etanoli on alkoholijuomissa oleva alkoholi, joka liiallinen nauttiminen vaikuttaa kognitiivisia kykyjä ja voi aiheuttaa sydän- ja verisuonisairauksia, maksakirroosia ja syöpä.
Lisäksi alkoholimyrkytysasteen eli humalatilan saavuttaessa, jos alkoholin annos liian korkea alkoholipitoisuus voi ilmaantua alkoholikooma, joka voi johtaa hengityshalvaukseen ja jopa kuolemaan. kuolema.
Viitteet
- T. TO. Geissman. (1974) "Orgaanisen kemian periaatteet" Toinen painos. Pääkirjoitus Reverté, S.A. ISBN: 8429171800
- Ahumada-Cortez, J. G., Gámez-Medina, M. E. ja Valdez-Montero, C. (2017). Alkoholin kulutus kansanterveysongelmana. Ra Ximhai, 13(2), 13-24.
- Morrison, R. T. ja Boyd, R. N. (1998). Orgaaninen kemia. Pearson koulutus.
- Weininger, S. J. & Stermitz, F. R. (1988). Orgaaninen kemia. minä käänsin.
Seuraa:
- Etyylialkoholi
- Polttoaineet
- orgaaninen kemia


