Esimerkki peptidisidoksesta
Kemia / / July 04, 2021
Peptidisidos on se, jossa kaksi aminohappomolekyyliä liitetään kondensaatiolla.
Peptidisidosten ymmärtämiseksi paremmin aminohapot on ensin määriteltävä:
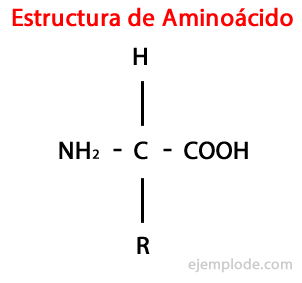
Aminohapot ovat orgaanisia molekyylejä lyhyt sisältää vähintään aminoryhmä (-NH2), emäksinen, ja karboksyyliryhmä (-COOH), hapan luonteeltaan.
Vaikka elävät olennot syntetisoivat eri tarkoituksiin hyvin erilaisia aminohappotyyppejä, tärkeimmät ovat ne ovat osa proteiineja, kaikki kuuluvat luokkaan a-aminohapot.
A-aminohapoille on tunnusomaista se, että happo- ja aminoryhmät ovat kiinnittyneet samaan hiiliatomiin, jota kutsutaan a-hiileksi. Lisäksi tämä a-hiili sitoutuu kolmantena substituenttina vetyatomiksi ja neljänneksi substituentti, erikokoinen ja -ominaisuuksiltaan ylimääräinen ryhmä, joka erottaa jokaisen aminohapon toiset.
Neljää substituenttia kutsutaan Sivuketju Aminohappo ja sitä edustaa usein yksinkertaistetussa muodossa R-kirjain.
Koska a-hiilen neljä substituenttia ovat erilaiset ja hyväksyvät sen ympärille tetraedrisen järjestelyn, läsnä olevat a-aminohapot
optinen isomeria, jolloin molekyylillä on a vaihtoehtoinen muoto joka näyttää a peilikuva hänen, joka ei lopulta ole samanlainen molekyyli. Näille kahdelle molekyylin isomeeriselle muodolle on annettu kirjaimet D tai L riippuen siitä, miten substituentit on järjestetty avaruuteen. Kaikki proteiineissa olevat aminohapot ovat L.Aminohapot luokitellaan niiden kemiallisten ominaisuuksien mukaan Polar ja Apolar. Polarit puolestaan jaetaan Neutraali ja ladattu (joka voi olla hapan tai emäksinen). Ei-polaarinen voi olla alifaattinen tai aromaattinen.
Peptidit ja peptidisidos
Peptidit ovat aminohappojen kovalenttisen yhdistymisen amidisidosten kautta muodostamia yhden ja toisen aminopään karboksyylipään kondensaatio vapauttamalla vesimolekyyli reaktio. Tätä yhdistystä kutsutaan peptidisidokseksi.
Tämän reaktion mekanismi on esitetty alla, jossa Amino- ja karboksyyliryhmät ja aminohappomolekyylien kondensaatio tapahtuu peptidin muodostamiseksi.
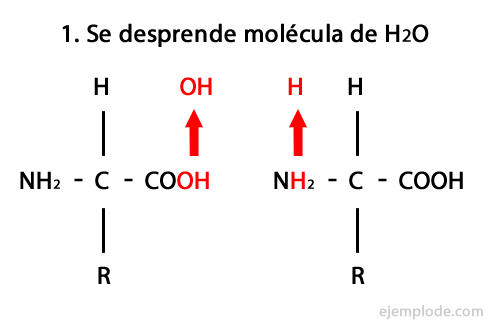
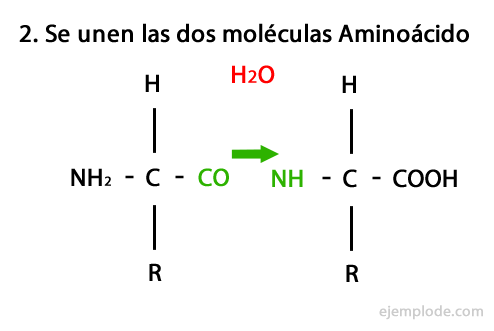

Peptidit, kuten aminohapot ja proteiinit, niiden päissä on aminoryhmä ja karboksyyliryhmä reagoimatta.
Yksinkertaisen peptidin ja jopa proteiinin kaavan määrittämiseksi riittää, että luetellaan sen muodostavat aminohapot, alkaen siitä, jolla on ilmainen Amino-ryhmä, ja päättyen siihen, jolla on vapaa karboksyyliryhmä.
Jotkut kehossa löydetyt peptidit ovat Vasopressiini, joka nostaa verenpainetta ja lisää veden imeytymistä munuaisissa; Enkefaliini, joka vähentää kipua; ja Oksitosiini, joka aiheuttaa kohdun supistumisen.
Peptidisidoksen ominaisuudet
Yhden aminohapon aminoryhmän kondensaatio toisen karboksyylin kanssa, tapahtuu vesipitoisessa liuottimessa, jotta se ei ole spontaaniaja siksi proteiinisynteesi vaatii energian saannin.
Peptidisidos, kuten missä tahansa amidisidoksessa, esittää resonanssia kahden ääripään välillä: neutraali muoto, jolloin yksittäinen sidos yhdistää ensimmäisen aminohapon karbonyylihiilen ja toisen (C-N) aminotyypin, ja lomake erottamalla maksut jossa kaksi atomia on kytketty kaksoissidoksella (C = N). Todellisuudessa peptidisidos ei hyväksy kumpaakaan näistä äärimmäisistä tilanteista, mutta se on kummankin resonanssihybridi.
Puhelu on Peptiditaso, joka koostuu kaikki peptidisidoksessa olevat atomit, jotka liittyvät kahteen alkuperäiseen aminohappoon. Toisaalta typen ja vedyn atomit vastaavan hiiliatomin kanssa ensimmäisessä aminohapossa. Toisaalta toisen aminohapon hiili a, karbonyyliryhmän hapen ja hiilen kanssa.
Peptidien ja proteiinien erot
peptideillä on pieni määrä aminohappoja, joka vaihtelee kahdesta muutamaan kymmeneen niistä, ja niiden konformaatio liuoksessa muuttuu joustavaksi.
pienet proteiinit, rakenteellisesti lähellä suuria peptidejä, on a määritelty muoto ja paljon vähemmän joustava.
On proteiineja, joilla on peptidien tapaan häiriintynyt ja joustava konformaatio, mutta järjestys, kun ne ovat vuorovaikutuksessa solun muiden makromolekyylien kanssa.
20 esimerkkiä aminohapoista, jotka osallistuvat peptidisidontaan
- Wisteria
- Tytölle
- Valine
- Leusiini
- Isoleusiini
- Proline
- Metioniini
- Fenyylialaniini
- Tyrosiini
- Tryptofaani
- Serine
- Treoniini
- Kysteiini
- Asparagiini
- Glutamiini
- Asparagiinihappo
- Glutamiinihappo
- Lysiini
- Arginiini
- Histidiini



