Esimerkki reaktiivisista materiaaleista
Kemia / / July 04, 2021
Reaktiiviset materiaalit ovat aineita, jotka joutuessaan kosketuksiin muiden kanssa yleensä aloita kemiallinen reaktio. Tämän reaktion lopussa on seurauksena tietty määrä erilaisia aineita.
Reaktiivisuus aineissa
Reaktiivisuus on aineiden kapasiteetti olla vuorovaikutuksessa muiden kanssa kemiallisessa reaktiossa. Kaikkia tämän reaktion osallistujia kutsutaan reaktiivisiksi. Kun kemiallinen ilmiö päättyy, erilaisia aineita kutsutaan Tuotteet.
Teollisuusympäristössä reaktiivisuutta käytetään milloin haluat tuottaa määrän tuotetta halusi. Teollisuuslaitoksissa tehdään valitsemaan raaka-aine, jonka koostumuksessa on sopivat reagenssit, ja sijoita se - reaktorin nimisessä säiliössä kemiallisen reaktion suorittamiseksi ja varmista, että siinä on taloudellinen prosessi ja tehokas.
On aikoja, jolloin reaktio se tulee olemaan spontaania, ja se suoritetaan vaivattomasti vain saattamalla reagenssit kosketuksiin. Riittää, että reagensseja ravistetaan niiden sisällyttämisen edistämiseksi.
Muissa tilanteissa reagenssien yksinkertainen kontakti ei riitä, mutta
ehtoja on tarpeen muuttaa prosessin, joko lisäämällä reaktoriin lisää sekoitusta, tai lisäämällä kuumennusta tai jopa jäähdytystä siten, että reaktio alkaa ja etenee nopeammin ja nopeammin.Reagenssit alkavat osallistua Tuotteiden luomiseen, mutta tekevät osuuden mukaan joka osoittaa reaktion ilmaisevan yhtälön, kuten seuraavassa:
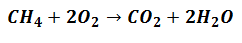
Se tarkoittaa, että metaanireagenssit (CH4) ja happea (O2) sekoitetaan suhteessa 1 - 2 molekyyliyksikköä vastaavien tuotteiden muodostamiseksi.
Jos jokin reagensseista lisätään pienin määrä johon vaaditaan laskettuna, kutsutaan Reagenssin rajoittaminen, koska kun kaikki on kulutettu, reaktio loppuu.
Toista reagenssia, joka reaktion lopussa on ylijäämä, kutsutaan Reaktiivinen ylimäärässä, ja tietysti se tulee yhdessä Tuotteiden kanssa.
Aineiden reaktiivisuutta voidaan käyttää monissa kemiallisissa ilmiöissä, kuten Hapetukset, kaliumpermanganaatin tapauksessa; Katalyysi, kuten platinametallissa hienon silmän muodossa; alkuainevaihto, kuten sinkkimetallin tapauksessa, joka korvaa vedyn hapoissa.
Reaktiivisuus vaarallisten materiaalien ominaisuutena
Reaktiivisuus edustaa a riskialtista omaisuutta kun reaktiivinen materiaali on jo jätettä ilman käyttöä, se kaadetaan ensin astiaan, joka varmistaa, että se pysyy eristettynä ihmiskontaktista. Kun jäte on kiinteää tai nestemäistä, se on yleensä paksua muoviastiaa, jossa on pakollisena tarra "reagenssimateriaalin" piktogrammi, joka on kuva, jossa on oranssi tausta ja vastaava symbologia mustalla. Seuraava kuva näyttää erilaisten reaktiivisuuden signaalien erilaisuuden.

Reaktiivisuus on yksi ominaisuuksista CRETIB vaarallisista jätteistä: Syövyttävä, reaktiivinen, räjähtävä, myrkyllinen, syttyvä ja biologisesti tarttuva. Itse asiassa se on edustavin, koska kaikki muut ominaisuudet liittyvät reaktiivisuuteen.
Hyvin yleinen tapaus, jossa näiden materiaalien vaara altistuu, on silloin, kun tapahtuu niiden vuoto. Esimerkiksi kun rikkihappovuoto tapahtuu ja sitä vuotaa hyvin suurelle alueelle, henkilöstö, jolla ei ole koulutusta tilanteen hallitsemiseksi, on poistettava. Tähän koulutettujen ihmisten on puututtava asiaan.
Menettely vaarallisen tilanteen poistamiseksi alkaa siirtymällä paikalle sopivilla henkilökohtaisilla suojavarusteilla. Reaktiivisen materiaalin vuotoalue tunnistetaan ja eristetään, ja sen reaktiivisuus alkaa toimia toisen kemiallisesti vastakkaisen lajin kanssa. Tässä tapauksessa rikkihappo toimii happona. Tämä reaktiivisuus voidaan sammuttaa vain sellaisilla lajeilla kuin natriumhydroksidi, joka on yksi tehokkaimmista emäksistä.
Hapon ja emäksen välistä reaktiota kutsutaan neutraloinniksi. Tämän ilmiön avulla rikkihapon reaktiivisuus vuodossa ohjataan kohti natriumhydroksidin aktiivisuutta.
Tulee aika, jolloin natriumhydroksidi, myös reaktiivinen materiaali, lopettaa rikkihapon vaarallisuuden. Kun reaktio on ohi, kyse on vain tuotteiden laimentamisesta runsaalla vesivirralla.

Esimerkkejä reaktiivisista materiaaleista
- Natriumhydroksidia
- Kalsiumhydroksidi
- Magnesiumhydroksidi
- Rikkihappo
- Suolahappo
- Typpihappo
- Rikkivety
- Kaliumnitraatti
- Natriumbikarbonaatti
- Hiilidioksidi
- Rikkidioksidi
- Rikkitrioksidi
- Vetykaasu
- Kaasumainen happi
- Kloorikaasu
- Kaasumainen bromi
- Metallinen litium
- Metallinen natrium
- Metallinen cesium
- Metallinen magnesium
- Ammoniumnitraatti
- Natriumkloridia
- Kaliumkloridi
- Kalsiumkloridi
- Kaliumpermanganaattia
- Natriumpermanganaatti
- Metallinen platina
- Metallinen sinkki
- Kalsiumkarbidi
- Asetyleeni
- Metaani
- Etaani
- Propaani
- Butaani


