Orgaanisen kemian esimerkki
Kemia / / July 04, 2021
Orgaaninen kemia Se on yleisen kemian osa, joka vastaa tutkimuksesta ja kemiallisten yhdisteiden toiminnallisesta luokittelusta, jonka rakenteellinen elementti on Hiili, läsnä runsaasti elävää ainetta; Tämä luo hyvin erilaistuneen epäorgaanisen kemian universumin, joka on omistettu mineraaleiksi luokitelluille kemiallisille yhdisteille.
Hiiliatomissa on neljä elektronia elektronisen kokoonpanonsa viimeisessä kuoressa. Tämä ominaisuus yhdessä sen atomisäteen kanssa mahdollistaa sen liittämisen kovalenttisilla sidoksilla muihin saman alkuaineen atomit lukuisissa ketjuissa muodostaen suuren määrän kemiallisia yhdisteitä vakaa.
Voit tarkistaa Kovalenttiset sidokset.
Sellaiset kemialliset yhdisteet, niiden hiiliatomien lisäksi, jotka antavat niille alkuperäisen rakenteensa, sisältävät vetyatomeja hiilivalsenssin pääkomplementtina. Lisäksi tässä yhdisteiden monimuotoisuudessa on sellaisia, joissa on happiatomeja, Typpi, halogeenit, rikki ja jopa fosfori, emäksiset ja maa - alkalimetallit sekä metallien metallit siirtyminen. Riippuen siitä, kuka molekyylissä on mukana, se on lopullisen aineen fysikaaliset ja kemialliset ominaisuudet.
orgaaniset yhdisteet ovat läsnä kaikkialla elävää ainetta; edistää ja ylläpitää kaikkia biologiset toiminnottoisin kuin epäorgaaniset tai kivennäisaineet, joita ihmiset ovat käyttäneet kaupallisiin tarkoituksiin, kokeiluihin tai tiettyjen kotitaloustehtävien hoitamiseen.
Orgaanisen kemian historia
Ennen vuotta 1828 orgaanisen kemian ja epäorgaanisen kemian välillä tehtiin jo ero. Orgaaninen aine liittyi luomiseen a "elintärkeä voima"ja epäorgaaniseen elottomien, mineraalien kanssa. Näiden käsitysten perusteella ei voida odottaa saavan orgaanisia yhdisteitä epäorgaanisista materiaaleista laboratoriossa.
Kuitenkin, vuonna 1828 Friedrich Wöhler (1800-1882) onnistui valmistamaan orgaanisen aineen, Urea CO (NH2)2, tärkeä eläinten aineenvaihdunnan tuote, epäorgaanisista yhdisteistä. Hoito Lyijysyanaatti Pb (CNO)2 kanssa Ammoniakki NH3 saada Ammoniumsyanaatti NH4CNO; Tämä yhdiste todellakin muodostui, mutta kun liuos keitettiin ammoniumsyanaatin kiteyttämiseksi, se muutettiin ureaksi.
Tämä kemiallinen muutos on esimerkki Sisäinen uudelleenryhmittely, jossa molekyylin atomien lukumäärä tai luokka ei muutu, vaan vain niiden järjestys siinä. Tämäntyyppiset muunnokset ovat hyvin yleisiä orgaanisessa kemiassa.
Wöhlerin löytö aloitti myöhemmin elämänvoimateorian hylkäämisen - hävitetään kokonaan seuraamalla monien muiden orgaanisten yhdisteiden valmistamista laboratorio. Tästä huolimatta epäorgaanisten ja orgaanisten ominaisuuksien määritelmät pysyvät voimassa, koska epäorgaaniset yhdisteet liittyvät mineraalituotteisiin ja orgaaniset yhdisteet, jotka ovat itse asiassa hiili- ja vetyyhdisteitä ja niiden johdannaisia, ovat elävien organismien tuottamia.
Vaikka yleisen kemian lait koskevat yhtä lailla molempia yhdisteitä, erilaiset syyt oikeuttavat ja tekevät tämän jaon tarpeelliseksi. Siten orgaaniset ja epäorgaaniset yhdisteet eroavat erilaisista ominaisuuksista, kuten: niiden Liukoisuus edullinen orgaanisissa liuottimissa (eetteri, alkoholi, kloroformi jne.) ja vastaavasti vedessä Vakaus (orgaaniset yhdisteet hajoavat suhteellisen matalissa lämpötiloissa), ja Reaktioiden luonne; epäorgaanisten yhdisteiden osalta ne ovat ionisia, yksinkertaisia ja käytännöllisiä ja orgaanisten yhdisteiden osalta kovalenttisia, monimutkaisia ja hitaita.
Orgaaniset yhdisteet
Tunnetaan hiiliyhdisteet, joissa on jopa yhdeksänkymmenen atomin ketjuja. ketjut Hiiliatomeja voi olla lineaarinen ja haarautunut ja joilla on yksittäisiä kovalenttisia sidoksia tai kaksois- tai kolmoissidoksia. Yli 2500 yhdisteen tiedetään sisältävän vain hiiltä ja vetyä (Hiilivedyt).
Orgaanisten yhdisteiden isomerismi
Epäorgaanisissa yhdisteissä kaava edustaa yleensä yhtä yhdistettä; siten on vain yksi kaavan H mukainen aine2SW4. Rikkihappomolekyyli sisältää kaksi vetyatomia, yhden rikkiä ja neljä happea, erityisessä ja ainutlaatuisessa järjestelyssä. Orgaanisissa yhdisteissä se on harvinaista, että näin tapahtuu. Siten on esimerkiksi kaksi yhdistettä, jotka reagoivat kaavaan C2H6Tai etyylialkoholi tai etanoli ja dimetyylieetteri.

Mitä monimutkaisempi molekyyli on, sitä suurempi on hiiliatomien määrä, sitä suurempi on mahdollisten isomeerien määrä.
Orgaanisten yhdisteiden analyysi
Orgaanisen yhdisteen analyysi käsittää kvalitatiivinen analyysi, kvantitatiivinen analyysi ja Toiminnallinen analyysi. Oletetaan, että yhdiste on epäpuhtaassa tilassa, se puhdistetaan aiemmin Kiteytys, Tislaus, Sublimaatio, Uuttaminen, jne. Puhtauskriteeri voidaan arvioida sen fysikaalisten vakioiden perusteella, kuten sulamispiste, kiehumispiste, tiheys, liukoisuus, kiteinen muoto, taitekerroin jne.
kvalitatiivinen analyysi Se varmistetaan tutkimalla yhdisteen muodostavien alkuaineiden, erityisesti hiili, vety ja typpi, ja joskus halogeenit, rikki ja fosfori, läsnäoloa.
kvantitatiivinen analyysi Se suoritetaan perustana kvalitatiivisessa analyysissä käytetyistä menetelmistä. Lähtökohtana on tietty määrä ainetta, joka palaa, ja hiilidioksidi kerätään ja punnitaan. muodostunut hiili - ja vesihöyry hiilen ja vedyn prosenttiosuuden laskemiseksi yhdiste. Kvantitatiivisen analyysin tulokset helpottavat standardin laskemista empiirinen kaava, vaikka molekyylikaava löytyy vasta aineen molekyylipainon määrittämisen jälkeen. Mutta ongelmaa ei ole vielä ratkaistu, koska sama molekyylikaava voi vastata erilaisia isomeerejä.
Orgaanisten yhdisteiden luokitus
Rakenteensa mukaan orgaaniset yhdisteet on jaettu yhdisteisiin alifaattinen, aromaattinen Y heterosyklinen. Alifaattiset yhdisteet ovat sukua metaani CH: lle4, ovat avointa ketjua, paitsi sykloparafiinit, ja nimensä velkaa se, että eläin- ja kasvirasvat kuuluvat tähän ryhmään.
aromaattiset yhdisteet, suljettu ketju, läheinen sukulaisuus bentseeniin, C6H6, ja he ovat velkaa nimensä siitä, että monilla heistä on tuoksuvia, miellyttäviä tuoksuja.
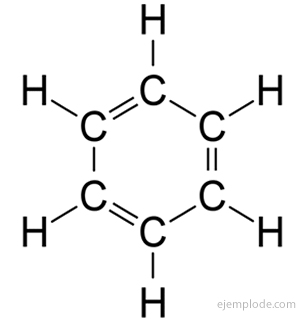
Bentseenirengas
heterosykliset yhdisteet Ne ovat suljetun ketjun yhdisteitä, joissa renkaassa on muuta alkuaine kuin hiili.
Perustuslain mukaan he ovat:
Hiilivedyt, joka puolestaan luokitellaan linkkien tyypin vuoksi Alkaanit, Alkeenit Y Alkynes. Lisäksi sykloalkaanit, bentseeni ja niiden johdannaiset, jotka koostuvat vain hiilestä ja vedystä, kuuluvat tähän luokkaan.
Heterosykliset yhdisteet
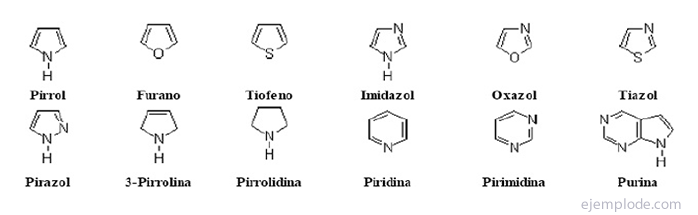
Halogenoidut johdannaiset:R-X
Nitroyhdisteet:R-NO2
Sulfonihapot:R-SO3H
Nitriilit (OR-alkyylisyanidit) ja isonitriilit:R-CN ja R-NC. Ne eroavat toisistaan siinä, miten typpiatomi sitoutuu molekyyliin.
Alkoholit:R-OH
Fenolit: Yhdisteet, jotka perustuvat runkoon, joka koostuu bentseenirenkaasta, johon on lisätty hydroksyyliryhmä.

Eetterit:R-O-R
Merkaptaanit: R-SH
Tioeetterit:R-S-R
Tioihapot:R-COSH
Aldehydit:R-CHO
Ketonit:R-CO-R
Karboksyylihapot:R-COOH
Menet ulos:R-COOM (M metallille)
Esterit: R-COO-R
Anhydridit: R-CO-O-OC-R
Aminot:R-NH2, R-NH-R, 2R-N-R
Aldosa-tyyppiset hiilihydraatit:-CHOH-CHOH-CHO
Ketoosityyppiset hiilihydraatit:-CHOH-CO-CH2vai niin
Organometalliset yhdisteet:R-M-R
Metalli-alkyylihalogenidit:R-MX (tunnetaan myös nimellä Grignard Reagents)
