Lantanidin ominaisuudet
Kemia / / July 04, 2021
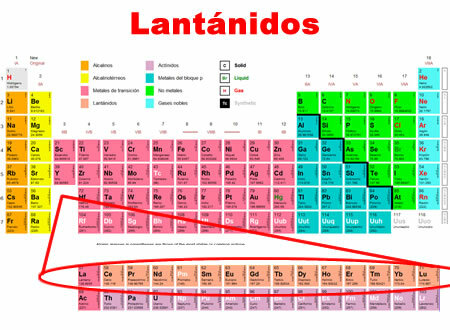
Lanthanidit ovat kemiallisia alkuaineita, jotka vaihtelevat Lanthanumista Lutetiumiin. Niillä on yhteisiä piirteitä, joiden vuoksi ne on luokiteltu erityisryhmään jaksollisen taulukon alaosassa.
Lantanidien pääominaisuudet:
- Ne sijaitsevat jaksollisen taulukon jaksossa 6.
- Ne kattavat 15 elementtiä, 57-71.
- Ne jakavat Lanthanumin rakenteen, johon lisätään energiataso f, joka on vähemmän kemiallisesti reaktiivinen.
- Niitä kutsuttiin harvinaisiksi maametalleiksi, koska luonnollisessa tilassa ne yhdistetään aina oksidien muodostamiseksi.
- Jotkut niistä ovat suhteellisen runsaita.
- Vaikka heillä on vaihtelevat valenssit, useimmilla on valenssit +3.
- Kun sen atomiluku kasvaa, sen säde pienenee.
- Niillä kaikilla on kiiltävä metallinen ilme.
Lantanidien yksilölliset ominaisuudet:
Lantaani (La).
- Atomiluku 57
- Atomipaino: 139
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 920 ° C
- Kiehumispiste: 3457 ° C
Se löydettiin vuonna 1839. Teollisuudessa sitä käytetään seoksissa muiden lantanidien kanssa kevyempien kivien valmistamiseksi; optiikassa sitä käytetään optisiin laskeihin. Sitä käytetään myös vetysiineihin, joita käytetään kaasujen pitämiseen. Lääketieteessä sitä käytetään lantaanikarbonaatin muodossa munuaisten vajaatoiminnan hoitoon, koska sillä on affiniteetti sekoittua fosfaattien kanssa, mikä vähentää hyperfosfemiaa.
Serium (Ce)
- Atomiluku 58
- Atomipaino: 140
- Tila: Pehmeä kiinteä
- Ulkonäkö: Metallinen, hopeanharmaa, rautamainen
- Valencias: +3, +4
- Sulamispiste: 798 ° C
- Kiehumispiste: 3426 ° C
Se löydettiin vuonna 1803. Se on runsain lantanidi. Sitä käytetään katalyyttien valmistamiseen, pääasiassa autoille (katalysaattorit) ja öljyn krakkaamiseen. Oksidimuodossa sitä käytetään lasien ja linssien kiillottamiseen. Vaikka sillä ei ole tunnettuja biologisia toimintoja, sitä käytetään lääketieteessä palovoiteissa.
Praseodyymi (Pr)
- Atomiluku 59
- Atomipaino: 144
- Tila: Pehmeä kiinteä
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 931 ° C
- Kiehumispiste: 3520 ° C
Se löydettiin vuonna 1841 ja eristettiin vuonna 1885. Teollisuudessa sitä käytetään magnesiumseoksissa lentokoneiden moottoreiden valmistamiseen; Sitä käytetään antamaan lasille ja emalille keltainen väri. Nikkeliseoksilla on magneettisia ominaisuuksia. Reagoi halogeenien kanssa muodostaen fluorideja, klorideja, bromideja ja jodideja.
Neodyymi (Nd)
- Atomiluku 60
- Atomipaino: 139
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 1024 ° C
- Kiehumispiste: 3100 ° C
Se löydettiin vuonna 1885, kun praseodyymi eristettiin; neodyymi eristettiin vuoteen 1925 saakka. Se on yksi reaktiivisimmista lantanideista. Teollisuudessa sitä käytetään lasin ja emalien värjäämiseen. Koska se kykenee absorboimaan valoa, sitä käytetään tähtitieteessä kiteiden luomiseen, joilla infrapunaspektrometrit ja suodattimet kalibroidaan. Yksi sen tärkeimmistä käyttötarkoituksista on valmistaa magneettisesti voimakkaita magneetteja. Näitä magneetteja käytetään tarkkuusinstrumentteihin, kuten tietokoneen kiintolevyihin, sekä joihinkin ohuissa kaiuttimissa.
Prometium (Pm)
- Atomiluku 61
- Atomipaino: 145
- Kiinteä tila
- Ulkomuoto: ?
- Valencias: +3
- Sulamispiste: 1100 ° C
- Kiehumispiste: 3000 ° C
Sen olemassaolo ennustettiin vuonna 1902, mutta se pystyttiin todistamaan vasta vuonna 1944. Tätä lantanidia ei löydy luonnosta, sillä se on sen uraanin hankkimisen ja tutkimuksen lähde. Kun uraanifissio ydinreaktorissa, yksi atomista, joka syntyy tästä atomierotuksesta, on prometium. Sillä on radioaktiivisia ominaisuuksia, jotka antavat sille fosforesenssin, ja sitä käytetään avaruusaluksissa käytettäviin kalibraattoreihin ja ydinparistoihin.
Samarium (Sm)
- Atomiluku 62
- Atomipaino: 150
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 1072 ° C
- Kiehumispiste: 1803 ° C
Se löydettiin vuonna 1853 ja eristettiin vuonna 1879. Siinä on useita isotooppeja, ja ainakin kaksi niistä on radioaktiivisia. Teollisuudessa sitä käytetään optiikassa infrapunavaloa absorboivien kiteiden valmistamiseen. Sitä käytetään myös katalysaattorina alkoholin saamiseksi ja osana joissakin loistelampuissa ja televisioissa. Terveyden kannalta se voi hengitysteitse (kuten kiteiden kiillottamiseen käytettävä oksidi) aiheuttaa keuhkoemboliaa tai vaikuttaa maksaan. Radioaktiivisia isotooppeja käytetään terminaalisesti sairaiden potilaiden sädehoidossa.
Europium (Eu)
- Atomiluku 63
- Atomipaino: 152
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +2, +3
- Sulamispiste: 826 ° C
- Kiehumispiste: 1527 ° C
Se löydettiin vuonna 1890. Se on reaktiivisin lantanideista. Sitä on käytetty loisteputkissa ja televisioissa, mutta se aiheuttaa keuhkoemboliaa, jos se on hengitettynä tai vahingoittaa maksaa, jos sitä kertyy ihmiskehoon, sillä ei ole melkein mitään teollista käyttöä. Atomisessa tutkimuksessa sitä käytetään, koska se absorboi neutroneja.
Gadolinium (Gd)
- Atomiluku 64
- Atomipaino: 157
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 1312 ° C
- Kiehumispiste: 3250 ° C
Gadoliniumilla on vain vähän käyttökohteita, joista suurin on magneettinen teollisuusjäähdytys, koska se lisää magneettisia ominaisuuksia alhaisissa lämpötiloissa; mutta koska tämän tyyppiset jäähdyttimet vaativat arseenin käyttöä, niitä ei käytetä kotitalouksien jäähdytykseen. Lääketieteessä sitä käytetään varjoaineena magneettisen ydinresonanssin suhteen.
Terbium (Tb)
- Atomiluku 65
- Atomipaino: 159
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +4
- Sulamispiste: 1356 ° C
- Kiehumispiste: 3230 ° C
Se löydettiin vuonna 1843 ja eristettiin vuonna 1905. Se on erittäin tärkeä elektroniikkateollisuudessa, koska se on yksi puolijohteiden valmistuksessa käytetyistä elementeistä. Muita käyttötarkoituksia ovat loisteputkien ja kuvaputkien valmistus. Sitä käytetään myös katalysaattorina polttokennoissa. Vaikka sillä ei ole biologisia toimintoja, sen hengittämisellä tai pääsyllä ihmiskehoon on myrkyllisiä vaikutuksia, jotka vaikuttavat pääasiassa maksaan.
Dysprosium (Dy)
- Atomiluku 66
- Atomipaino: 162,5
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +2, +3
- Sulamispiste: 1407 ° C
- Kiehumispiste: 2567 ° C
Se löydettiin vuonna 1843 ja eristettiin vuonna 1905. Se on erittäin tärkeä elektroniikkateollisuudessa, koska se on yksi puolijohteiden valmistuksessa käytetyistä elementeistä. Muita käyttötarkoituksia ovat loisteputkien ja kuvaputkien valmistus. Sitä käytetään myös katalysaattorina polttokennoissa. Vaikka sillä ei ole biologisia toimintoja, sen hengittämisellä tai pääsyllä ihmiskehoon on myrkyllisiä vaikutuksia, jotka vaikuttavat pääasiassa maksaan.
Holmium (Ho)
- Atomiluku 67
- Atomipaino: 166
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 1474 ° C
- Kiehumispiste: 2700 ° C
Se löydettiin vuonna 1878 ja sen nimi on peräisin löytökaupungista Tukholma, latinaksi, Holmia. Sillä ei ole melkein mitään käytännön käyttöä; sitä käytetään kuitenkin joillakin teollisuudenaloilla katalysaattorina kemiallisille reaktioille sekä joillekin elektronisille komponenteille. Sitä käytetään myös lasersäteen taajuuden ja voimakkuuden muuttamiseen.
Erbium (Er)
- Atomiluku 68
- Atomipaino: 167
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 1795 ° C
- Kiehumispiste: 2863 ° C
Se löydettiin vuonna 1843. Sitä käytetään ydinteollisuudessa neutronipuskurina. Oksidimuodossa se on kiteiden väriaine, joka antaa heille vaaleanpunaisen sävyn; Näitä kiteitä käytetään optiikassa ja koruissa. Sitä käytetään myös kuituoptiikan valmistamiseen.
Thulium (Tm)
- Atomiluku 69
- Atomipaino: 167
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 1545 ° C
- Kiehumispiste: 1947 ° C
Se löydettiin vuonna 1879. Alhaisesta saatavuudesta huolimatta sen pääasiallinen käyttö on radioaktiivisten ominaisuuksiensa takia röntgenlähde kannettavissa laitteissa ja puolijohdelasereissa.
Yterterium (Yb)
- Atomiluku 70
- Atomipaino: 173
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 824 ° C
- Kiehumispiste: 1194 ° C
Se löydettiin vuonna 1878 ja eristettiin vuonna 1907. Radioaktiivisia isotooppeja käytetään kannettavissa röntgenlaitteissa, jotka toimivat ilman sähköä. Sitä käytetään myös parantamaan terässeoksia ja parantamaan niiden kestävyyttä, ominaisuutta, jota käytetään hammaslääketieteessä, teräksen mekaanisten ominaisuuksien parantumisen vuoksi. Sitä on käsiteltävä varoen, koska se voi aiheuttaa ärsytystä ja palovammoja. Lisäksi reagoidessaan ilman kanssa se voi aiheuttaa räjähdyksen tai tulipalon.
Lutetium (Lu)
- Atomiluku 71
- Atomipaino: 175
- Kiinteä tila
- Ulkonäkö: Metallinen, hopeanvalkoinen
- Valencias: +3
- Sulamispiste: 1652 ° C
- Kiehumispiste: 3402 ° C
Se löydettiin vuonna 1907. Se on vähäisin kemiallinen alkuaine maankuoressa. Alhaisesta saatavuudesta huolimatta sitä käytetään öljynjalostuksessa ja katalysaattorina orgaanisen kemian reaktioissa. Joitakin radioaktiivisia isotooppeja on testattu myös sädehoitohoidoissa.
