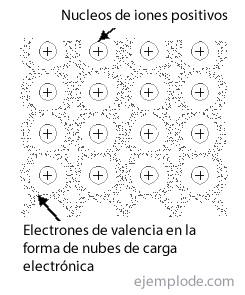
Metallinen joukkovelkakirjalainaesimerkki
Kemia / / July 04, 2021
Metallinen linkki on tapa, jolla metallin atomit onnistuvat kohtaamaan a kristallirakenne, vakaa, käyttämällä sen elektronien pilvetja riippumatta ionisten tai kovalenttisten sidosten yksinoikeudesta ilmestyä puhtaina aineina. On nimeltään Netto metallilinkkien ryhmään tai järjestelyyn.
Useimmat metallit kiteytyvät kolmen tyyppisissä järjestelyissä: Kehokeskeiset kuutioverkot, Kasvokeskeiset kuutioverkot Y Kompaktit kuusikulmaiset verkot.
Vuonna runko keskitetty, jokaista metallin atomia ympäröi 14 naapuria ja muut kaksi jäljellä mennessä 12. Jos yrität puuttua tällaisten rakenteiden sitoutumiseen, löydät heti elektronien vajaatoiminnan ongelman. Näin ollen litiumissa, jossa on yksi valenssielektroni ja 14 läheistä naapuria, on selitettävä, kuinka tämä elementti on ympäröi niin suuri määrä atomeja, ja silti se tuottaa riittävän stabiilin kiteen sulamispisteen ollessa 186 ° C. Sama tapahtuu muiden metallien kanssa.
Sveitsiläinen fyysikko Felix bloch vuonna 1928 hän ehdotti kvanttimekaanista teoriaa atomien sitoutumisen selittämiseksi metallikiteissä. Tässä
Bändin teoria kaikki elektronit, jotka ovat atomissa täysin täytetyillä energiatasoilla, otetaan huomioon olennaisesti sijaitseeeli sidottu atomeihin, joihin ne liittyvät. Toisaalta valenssielektroneja otetaan huomioon täyttämättömillä energiatasoilla vapaaja ne liikkuvat potentiaalisessa kentässä, joka ulottuu kaikkiin kristallissa oleviin atomeihin.atomien kiertoradat näistä vapaista elektroneista atomikannussa päällekkäin muiden kanssa delokalisoidut molekyyliradat jotka tuottavat sidoksen kaikkien läsnä olevien atomien välillä ja jotka tunnetaan nimellä Johtamisen kiertoradat.
energian tasot elektronien eristetyissä atomissa ovat hienotunteinen ja yleensä hyvin sijoitettu. Mutta muiden atomien läsnäolo kiteessä vaikuttaa näihin tasoihin muuttamalla jokaisen tason a-tasoksi tason nauha joiden lukumäärä on yhtä suuri kuin rakenteellisessa kokonaisuudessa olevien atomien lukumäärä. Jos tämä luku on suuri, kukin eristetty taso muodostaa käytännössä a jatkuva kaista. Lisäksi, kun alkuperäisten tasojen ja metallin atomien välinen tila on suuri, niin varhaisista elektronisista tasoista peräisin olevat bändit erotetaan toisistaan varten energiavajeet huomattava. Kun tasot ja etäisyydet ovat pienet, nauhat ovat ristissä ja päällekkäin kukin.
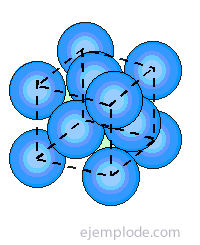
Tämä teoria antaa seuraavan kuvauksen tietyn metallin elektronisesta rakenteesta. A kiinteä metalli katsotaan olevan elektronikaistat erotettu toisistaan energiavajeet. Lisäksi nämä nauhat on joskus täysin täytetty paikallisilla elektroneilla tai ne on osittain täytetty vapailla elektroneilla, joiden molekyyliradat ulottuvat kaikkiin kristallin atomeihin.