15 exemples de diffusion et d'osmose
Divers / / July 04, 2021
La diffusion et osmose ce sont des processus de transport passif (ils ne nécessitent pas d'énergie supplémentaire pour se produire, contrairement au transport actif) de particules d'un ou plusieurs substances trouvé dans différentes concentrations de soluté et ils sont mis en contact les uns avec les autres, soit par une membrane semi-perméable (cas particulier de l'osmose), soit par d'autres moyens.
Qu'est-ce que la diffusion ?
La diffusion est un processus physique qui est basé sur le flux de particules d'une substance à partir d'une zone de forte concentration de soluté vers une faible concentration, jusqu'à ce que la concentration soit approximativement la même dans les deux zones. Le mouvement des particules est basé sur leur énergie cinétiqueEn d'autres termes, il n'y a pas d'apport d'énergie externe pour que la diffusion se produise. Par exemple: le passage de l'oxygène dans les alvéoles pulmonaires.
Ce mouvement se produit dans l'un des états d'agrégation de la la matière, mais elle s'observe plus facilement dans le cas des liquides et des gaz. La tendance du mouvement est à la formation d'un
mélanger uniforme des deux types de particules.Le scientifique Adolf baise établit en 1855 des lois qui portent son nom, et décrivent divers cas de diffusion de la matière dans un milieu dans lequel initialement il n'y a pas d'équilibre. Ces lois concernent la densité du débit des particules avec la différence de concentration entre les deux milieux séparés, son coefficient diffusion et perméabilité de la membrane (dans le cas où le milieu de séparation est une membrane semi-perméable).
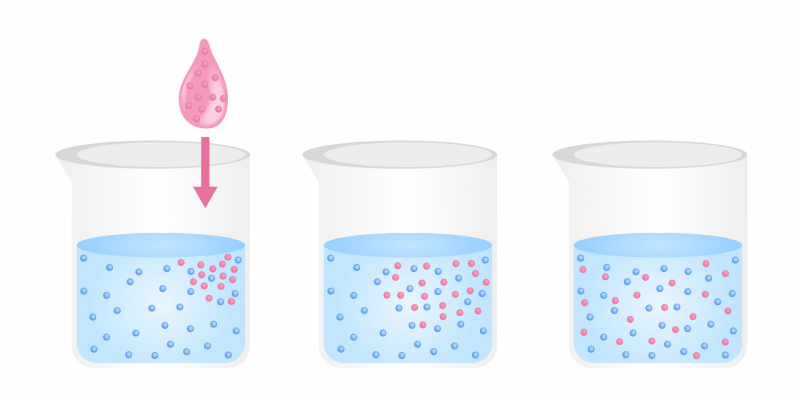
Exemples de diffusion
- Le passage de l'oxygène dans les alvéoles pulmonaires.
- Les impulsions nerveuses, qui impliquent ions sodium et potassium à travers la membrane des axones.
- Si vous prenez une paire de diffuseurs composée de deux métaux mis en contact par leurs faces, ils sont chauffés au-dessus du point de la fusion puis en refroidissant, on vérifiera que la composition a changé: diffusion d'atomes de nickel vers le cuivre et inversement s'est produite.
- Le réchauffement et le changement de couleur d'une tasse de café lorsqu'une bonne proportion de lait froid est ajoutée.
- L'entrée du glucose dans les globules rouges, en provenance de l'intestin.
- Dans un estuaire, il y a une diffusion moins dense de l'eau de rivière qui s'écoule sur l'eau de mer.
- Si vous mettez une cuillère à soupe de sucre dans un verre d'eau, le molécules de saccharose diffuse dans l'eau.
- La diffusion de gaz peut être observée lorsqu'une personne parfumée pénètre dans un endroit fermé et tout le monde sent immédiatement l'odeur. La même chose se produit lorsque quelqu'un fume à l'intérieur.
Qu'est-ce que l'osmose ?
L'osmose constitue un type de diffusion, mais avec deux caractéristiques particulières :
De cette façon, on observe que le solvant a tendance à traverser la membrane dans le sens de la dissolution dont la concentration est plus élevée, ce qui finit par produire une augmentation de la quantité de solvant dans la partie la plus concentrée (en soluté) et une diminution de la partie la moins concentrée (en soluté), c'est-à-dire que le solvant se déplace de la zone avec la concentration la plus faible en soluté vers la zone avec la concentration la plus élevée en soluté. C'est un processus qui est répété jusqu'à ce que la concentration (à la fois de soluté et de solvant) de la solution soit égale des deux côtés de la membrane.
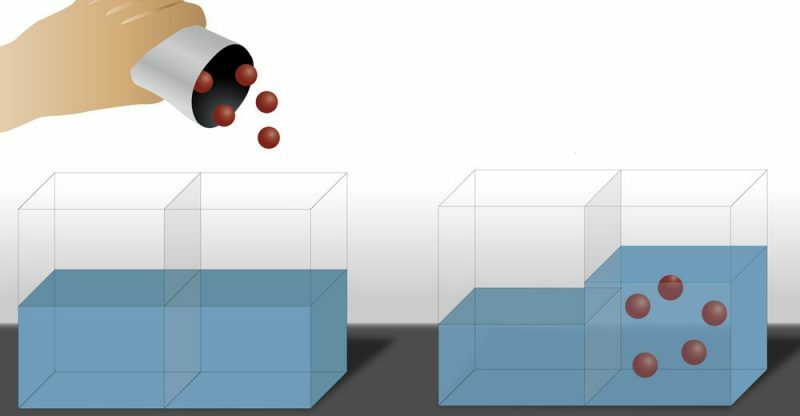
Il y a aussi le osmose inversée, où le passage du solvant s'effectue dans le sens inverse de l'osmose classique, c'est-à-dire que le solvant passe de la solution la plus concentrée en soluté à la moins concentrée en soluté. Pour y parvenir, une pression est appliquée sur la solution la plus concentrée en soluté.
Parce que c'est important?
La solubilité du soluté dans le solvant et la nature de la membrane semi-perméable à utiliser sont les facteurs fondamentaux qui déterminent l'efficacité du processus osmotique: l'un des facteurs qui influence la soi-disant « solubilité » sont les interactions entre les composants de la dissolution.
le processus osmotique Il est essentiel dans les processus biologiques où l'eau est le solvant, en particulier dans les processus visant à maintenir l'équilibre hydrique et électrolytique dans le êtres vivants, régulant les niveaux d'eau dans la cellule ou dans le corps en général: sans ce processus, il ne pourrait y avoir de régulation de liquides et l'absorption de nutriments.
Exemples de processus d'osmose
- Les êtres vivants unicellulaire vivant dans l'eau douce pénètrent dans de grandes quantités d'eau.
- L'absorption d'eau par les racines dans les organismes végétaux, ce qui permet la croissance.
- Obtention de l'eau des cellules épithéliales par le gros intestin.
- Fendre une pomme de terre en plaçant un peu de sucre avec de l'eau à une extrémité et une assiette avec de l'eau de l'autre. La pomme de terre agit comme une membrane, et après un certain temps, on verra que la solution qui contient du sucre a maintenant plus de liquide.
- L'hormone ADH qui permet la réabsorption de l'eau par le canal collecteur dans les reins.
- L'élimination de l'urine très diluée par laquelle le poisson expulse le maximum de liquide avec le minimum de perte de vous sortez.
- L'élimination de l'eau par la sueur chez les personnes.
- Les filtres pour purifier l'eau fonctionnent par osmose inverse, car ils sont fabriqués avec un Matériel qui permet le passage de l'eau, mais pas de molécules plus grosses.
Suivre avec:



