Définition du diagramme de phase
Divers / / December 22, 2021
Définition conceptuelle
Le diagramme de phase est la représentation visuelle de la dépendance à la température et à la pression d'une substance pure dans un système fermé. Expliquer les changements dans les états d'agrégation de la matière en fonction de la pression et de la température auxquelles la substance est soumise.

Ingénierie chimique
Auparavant, il est conseillé de comprendre ce que nous entendons par changements dans l'état d'agrégation. Ce sont précisément des changements d'état ou de phase. Lorsqu'une substance est simple, comme les fluides moléculaires, elle a des points de fusion et d'ébullition bien définis. Alors que, lorsque les masses molaires augmentent, ces températures deviennent des plages ou plutôt des intervalles, entre lesquels se produit le changement de phase.
Même dans de nombreux cas, certaines températures de changement de phase ne sont pas atteintes, car les substances sont préalablement décomposées. Nous définissons les changements de phase suivants qui seront localisés dans les diagrammes :
- Évaporation: du liquide au gaz.
- Condensation: du gaz au liquide.
- Sublimation: du solide au gaz.
- Sublimation inversée: du gaz au solide.
- Solidification: du liquide au solide.
- Fusion: du solide au liquide.
En général, ce sont des procédés thermiques, ils nécessitent la absorption ou la livraison de énergie de sorte qu'ils se produisent, de sorte que, au fur et à mesure que l'énergie est ajoutée ou retirée, nous nous déplacerons le long de la diagramme pour voir dans quel état d'agrégation la substance se trouvera.
Comme nous le savons bien, chaque substance est unique, donc chaque substance aura son propre diagramme de phase unique. Par conséquent, dans chaque diagramme un point triple sera présenté, où la pression et la Température auquel coexistent les trois phases (solide, liquide et gazeuse) Équilibre. De même, un point est présenté critiqueÀ l'extrémité supérieure de la courbe de vapeur ou de gaz, ce point indique qu'à des températures plus élevées, il ne peut pas être amené à un état liquide au-delà de continuer à augmenter la pression du gaz.
En général, les diagrammes de phases sont représentés comme suit :
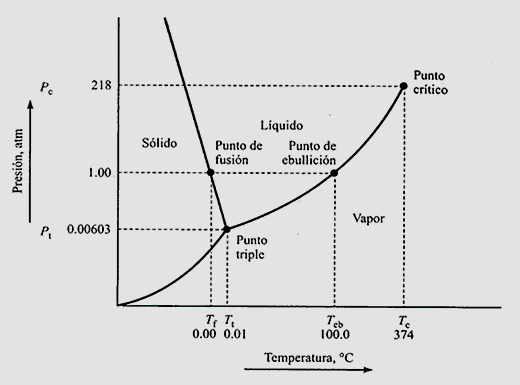
On observe ici, une schème où la pression est située sur l'axe des ordonnées et la température sur l'axe des abscisses. En général, les zones peuvent également être colorées pour une meilleure visualisation. À gauche de graphique la matière est à l'état solide et, à mesure que la température augmente (c'est-à-dire que la augmente l'énergie délivrée au système) un changement de phase est observé en liquide puis, de liquide en fumer. Tant que, nous nous déplaçons au-dessus du point triple. En dessous du point triple, le changement de phase est direct de solide à vapeur ou vice versa en fonction de l'apport ou de l'évacuation d'énergie.
Chacune des courbes représentées sont les courbes d'équilibre. Par exemple, la courbe du point triple au point critique est la courbe d'équilibre liquide - vapeur, tandis que la courbe de gauche est la courbe d'équilibre liquide-solide. Ci-dessous se trouve l'équilibre solide-vapeur, car à basse température et pression, la pression de vapeur du solide est représentée. Chacune de ces courbes d'équilibre représente les changements de phase qui ont été nommés ci-dessus.
Le diagramme de phase représenté est précisément le diagramme de phase de l'eau, en notant qu'à une pression de 1 atm, le point d'ébullition est de 100 ºC (point d'ébullition normal) et la température de fusion est de 0 ºC (point de fusion Ordinaire). Le point critique est observé avec une température critique de 374°C et une pression critique de 218 atm tandis que le point triple, où coexistent les trois équilibres, est de 0,00603 atm et 0,01°C.
De plus, on peut observer que, si l'on augmente la pression, le point de fusion diminue tandis que le température d'ébullition augmente, ceci est dû aux pentes de chacune des courbes de Équilibre.
Comme nous l'avons mentionné précédemment, chaque substance a son propre diagramme de phase, par conséquent, la tendance mentionné peut ne pas être reproduit dans toutes les études de cas puisque les pentes des courbes de l'équilibre varie.
Rubriques du diagramme de phases
