Définition de la structure atomique
Divers / / January 13, 2022
définition du concept
C'est la façon dont un atome est constitué. Lorsque nous parlons d'atomes, nous nous référons aux plus petites particules qui peuvent conserver les propriétés d'un certain élément.

Ingénierie chimique
Selon la Table périodique, il existe environ 118 types d'atomes différents qui, lorsqu'ils sont regroupés, forment des molécules. La structure de l'atome a été étudiée par différents scientifiques jusqu'à atteindre ce que nous prenons maintenant comme critère. général, qui est qu'un atome est composé de deux zones bien différenciées: la zone nucléaire et la zone extra nucléaire.
La zone nucléaire est formée par la charge positive (protons) et les charges neutres (neutrons), c'est pourquoi elle constitue près de 99,99 % de la masse atomique malgré une taille réduite de 10-12 cm. Les particules à l'intérieur sont maintenues ensemble par des forces nucléaires, des forces très fortes qui donnent lieu à Énergie nucléaire.
Bien qu'elle ait la masse atomique la plus faible, la zone extranucléaire occupe 99,99 % de la
le volume de l'atome, et il est chargé négativement étant la zone d'accueil pour les électrons, qui sont en continu mouvement indéfiniment.Lorsque l'atome est neutre, le nombre d'électrons et de protons est dit égal. Or, lorsqu'un atome perd ou gagne des électrons, restant chargés positivement ou négativement, des espèces ioniques appelées cations et anions se forment. Selon le nombre d'électrons gagnés ou perdus, on leur attribue un nom, par exemple, dans le cas de l'aluminium, qui est un métal qui forme un ion positif, puisqu'il perd trois électrons, on l'appelle un cation trivalent.
Si nous regardons les masses des particules subatomiques, nous verrions qu'elles sont similaires dans l'ordre des protons et neutrons tandis que les électrons ont une masse plus faible, tous définis dans le tableau périodique en la Unité de "uma". « uma » signifie « unité de masse atomique » et se définit comme un douzième de la masse atomique du carbone, pour établir une grandeur de référence. À son tour, il est défini comme l'équivalence suivante :
1 uma = 1,66 x 10-24 grammes
Si on regarde les ordres de grandeur, ils se rendent compte que c'est une valeur infime et imperceptible à la vision humaine. Ainsi, lors de la lecture de la masse atomique d'un élément, par exemple, dans le cas de l'hélium, nous voyons qu'il s'agit de 4,002602 amu ou, ce qui revient au même, de 6,64x10-24 grammes.
Lors de la définition de la structure atomique d'un élément, nous nous référons à deux nombres connus qui nous permettent d'identifier rapidement l'atome que nous nommons. Ces nombres sont: le numéro atomique et le nombre de masse.
Le numéro atomique ou "Z" représente le nombre de protons que l'atome a dans son noyau. Comme nous l'avons dit précédemment, si l'atome est neutre, "Z" correspond également au nombre d'électrons dans la zone extra-nucléaire. Grâce à son numéro "Z", nous pouvons le localiser dans le tableau périodique, ce qui lui donnera une série de certaines propriétés. Quant au nombre de masse ou "A", il fait référence au nombre de protons et de neutrons que l'atome a dans son noyau. En général, les deux nombres sont exprimés comme suit :
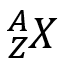
Où X représente le symbole du élément chimique.
Bien que pour un certain « X », « Z » soit unique, « A » peut varier en raison de l'existence d'isotopes.
Les isotopes sont des atomes d'un même élément qui diffèrent par le nombre de neutrons. Ils peuvent donc avoir le même "Z", c'est-à-dire le même nombre de protons, mais pas le même "A" puisque les neutrons varient de l'un à l'autre.
Il existe de nombreux exemples d'isotopes dans la nature, les plus répandus sont les isotopes du Carbone. Il existe les structures atomiques suivantes pour le même élément :
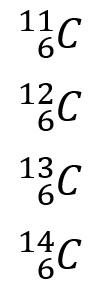
Comme on peut le voir, dans chacun d'eux, le nombre de neutrons varie. Toutes les espèces conservent 6 protons alors que la première a 5 neutrons, la seconde 6, la troisième 7 et la dernière 8. C'est en fonction de l'isotope que l'utilisation est déterminée. Par exemple, l'isotope Carbone-13 est le moins disponible dans la nature malgré sa stabilité physique. Le carbone 14 est un isotope radioactif avec des applications dans ce domaine et le graphite est l'un des isotopes les plus utiles aujourd'hui.
Sujets en structure atomique