Exemple d'énergie chimique
Chimie / / July 04, 2021
La L'énergie chimique est celle qui provient des réactions chimiques. L'interaction entre espèces chimiques engendre la rupture et/ou la génération de liaisons, ce qui implique respectivement une libération ou une absorption d'Énergie. L'énergie chimique est appelée énergie libérée, qui peut être utilisée comme énergie thermique et énergie électrique, par exemple.
L'énergie dans les réactions chimiques
L'énergie chimique peut être obtenue dans son expression maximale à partir de deux sources principales: la combustion et les solutions électrolytiques. D'autre part, au niveau du corps humain, il est possible d'obtenir de l'énergie grâce à la désintégration chimique des aliments.
Énergie de combustion
Par exemple, lorsque le Fuel Methane CH4, l'hydrocarbure le plus simple, commence à brûler en présence de l'Oxydizer, il se désintégrera pour former des produits de dioxyde de carbone CO.2 et eau H2OU ALORS. De plus, la rupture des liaisons des atomes d'hydrogène avec les atomes de carbone libérera de l'énergie sous forme de chaleur.
CH4 (g) + 2O2 (g) → CO2 (g) + 2H2 O (l) H = -212,8 Kcal / mol
Équation de la combustion du méthane. La chaleur de cette réaction est représentée par ΔH. Le signe négatif indique la libération d'énergie. La réaction est exothermique.
 Combustion du gaz méthane. La réaction se manifeste par une flamme.
Combustion du gaz méthane. La réaction se manifeste par une flamme.
Exemples de Chaleurs de Combustion de composés organiques à 25°C.
Composé |
Formule |
H (Kcal/mol) |
Méthane (g) |
CH4 |
-212.80 |
Éthane (g) |
C2H6 |
-372.82 |
Propane (g) |
C3H8 |
-530.60 |
n-butane (g) |
C4H10 |
-687.98 |
n-Pentane (g) |
C5H12 |
-845.16 |
Éthylène (g) |
C2H4 |
-337.23 |
Acétylène (g) |
C2H2 |
-310.62 |
Benzène (g) |
C6H6 |
-787.20 |
Benzène (l) |
C6H6 |
-780.98 |
Toluène (l) |
C7H8 |
-934.50 |
Naphtalène(s) |
C10H8 |
-1,228.18 |
Saccharose(s) |
C12H22OU ALORS11 |
-1,348.90 |
Méthanol (l) |
CH3Oh |
-173.67 |
Éthanol (l) |
C2H5Oh |
-326.70 |
Acide acétique (l) |
CH3COOH |
-208.34 |
Acide benzoïque (s) |
C6H5COOH |
-771.20 |
Pour qu'un Combustible fournisse toute la Chaleur de Combustion dont il est capable, il doit être à l'état gazeux. Comme indiqué dans le tableau, le benzène liquide fournit une chaleur de combustion inférieure de 6,22 Kcal/mol à celle dégagée par le benzène gazeux. Cela signifie que 6,22 Kcal/mol doivent être investis pour effectuer le passage du liquide au gaz.
Cliquez pour plus d'informations sur le Carburants.
Solutions électrolytiques Énergie
Un conducteur électrolytique est un milieu dans lequel est impliquée une ou plusieurs espèces ioniques, qui est dispersé avec sa charge électrique, permettant le passage d'un courant électrique à travers son Constitution. Les solutions électrolytiques sont des conducteurs électrolytiques.
Les conducteurs électrolytiques comprennent, en plus des solutions électrolytiques, Sels fondus, ainsi que certains sels solides, tels que le chlorure de sodium NaCl et le nitrate d'argent AgNO3.
Le transfert d'électrons se fait par migration ionique, positive et négative, vers les électrodes. Cette migration implique non seulement un transfert d'électricité, mais aussi le transport de matière d'une partie du conducteur à une autre.
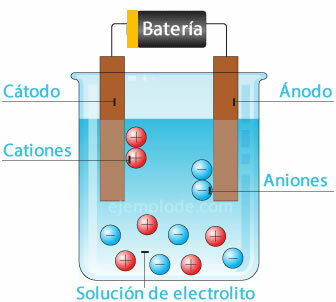 Cellule électrochimique
Cellule électrochimique
Connecter une source de potentiel aux électrodes métalliques (Cathode et Anode), et les plonger dans un Solution aqueuse, les électrons vont voyager à travers l'anode, pour s'échapper de la solution vers le pôle positif de la Fontaine. C'est le cas, par exemple, d'un ion Chlorure, qui se libère de son électron, et déjà avec une charge neutre, il rejoint un autre atome de Chlore, pour former la molécule diatomique. Le chlore gazeux s'échappera de la solution.
2Cl- = 2Cl + 2e-
Les électrons sortant du pôle négatif de la source seront logés dans la cathode immergée. Les espèces présentes dans la solution aqueuse (ions) vont prendre les électrons de la cathode. Par exemple, les ions Hydrogène qui composent l'eau, ayant été dans une charge positive, ont pris un électron à neutraliser, et joint à un autre atome d'hydrogène pour former la molécule diatomique. Il s'échappera sous forme d'hydrogène gazeux de la solution.
2H+ + 2e- = 2H
2H = H2 (g)
Cet échange d'électrons peut soutenir le fonctionnement des batteries de voiture, qui sont constituées d'électrodes de plomb Pb immergées dans une solution d'acide sulfurique H2SW4.
Cette même énergie est obtenue dans tous les types de piles qui sont manipulées au niveau domestique: 9V, AA, AAA, D, pour ne citer que quelques exemples.
Énergie alimentaire
Les êtres humains assimilent l'énergie qui est libérée en désintégrant la nourriture que nous mangeons dans notre corps. Cette énergie est ce que notre corps utilise pour les fonctions non conscientes (digestion, rythme cardiaque, fonctions cellulaires) et celles que nous réalisons.
Tant que vous n'avez pas d'activité physique intense et que votre métabolisme est lent, il est conseillé d'avoir un apport calorique régulier, car les aliments riches en Les lipides et les glucides complexes, qui ont de très grandes structures, sont plus difficiles à décomposer, ce qui entraîne une inversion de énergie. Dans ce cas, l'effet serait momentanément opposé.
Il est conseillé de consommer des fruits lorsque vous devez travailler la nuit, car le fruit contient du fructose, un glucide simple qui est facile à décomposer et qui aura de l'énergie à notre disposition après votre consommation.
L'énergie chimique et ses transformations
Centrales thermoélectriques
Les combustibles lourds sont utilisés dans les centrales thermoélectriques pour avoir un pouvoir calorifique élevé et durable. Généralement, il s'agit de mazout (fuel-oil). La combustion, qui est l'étape chimique du procédé, servira d'agent de chauffage pour une chaudière, qui générera de la vapeur saturée. Cette vapeur sortira sous pression par le réseau de distribution de vapeur et commencera à faire bouger les turbines du générateur. Ces appareils produiront de l'énergie électrique pour alimenter la population correspondante.
Énergie chimique → Énergie mécanique → Énergie électrique
Opération automobile
Les voitures dépendent d'une source d'énergie, qui est la batterie. Dans la batterie, la conduction électrolytique est déjà connue, ce qui alimente le système d'allumage, les accessoires du tableau de bord et les prises de courant auxiliaires. Grâce à cette électricité disponible, la voiture pourra se déplacer pour emmener le conducteur à l'endroit souhaité.
Énergie chimique → Énergie électrique → Énergie mécanique