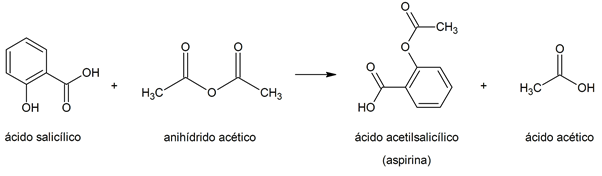रासायनिक प्रतिक्रियाओं के 20 उदाहरण
अनेक वस्तुओं का संग्रह / / July 04, 2021
यह कहा जाता है रासायनिक प्रतिक्रिया उस प्रक्रिया के लिए जिसके द्वारा एक या अधिक रासायनिक पदार्थ (जिन्हें "अभिकारक" कहा जाता है) रूपांतरित हो जाते हैं और दूसरों को जन्म देते हैं (जिन्हें "उत्पाद" कहा जाता है)। इस प्रकार, अभिकारकों के लिए एक रासायनिक प्रतिक्रिया के माध्यम से उत्पाद उत्पन्न करने के लिए, की एक पुनर्व्यवस्था परमाणुओं यू अणुओं जिसमें ऊर्जा विनिमय होता है। उदाहरण के लिए: दहन, ऑक्सीकरण, अम्ल-क्षार प्रतिक्रियाएं।
रासायनिक यौगिक है रासायनिक ऊर्जा परमाणुओं के बीच के बंधनों में जो उन्हें बनाते हैं। रासायनिक प्रतिक्रियाओं को आमतौर पर समीकरणों के माध्यम से व्यक्त किया जाता है, जहां अभिकारकों को बाईं ओर और उत्पादों को दाईं ओर इंगित किया जाता है, यदि प्रतिक्रिया उत्क्रमणीय है या प्रतिक्रिया है तो आगे और पीछे तीर दोनों भागों को एक दाहिने तीर से जोड़ना arrow प्रतिवर्ती।
जब मात्रा या अनुपात जिसमें अभिकारक प्रतिक्रिया करते हैं और उत्पाद प्राप्त होते हैं, तो हम स्टोइकोमेट्रिक प्रतिक्रियाओं की बात करते हैं।
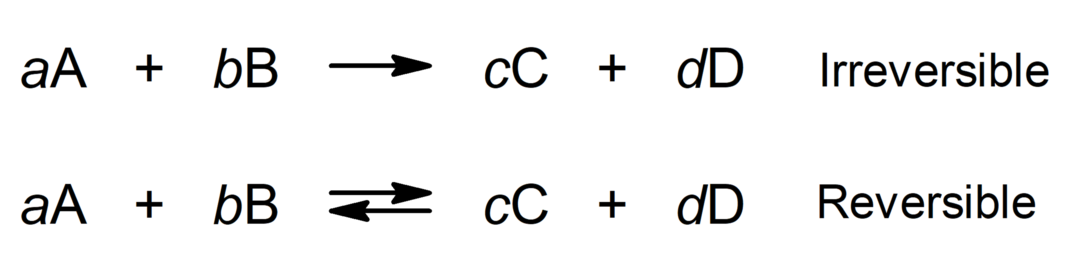
कहा पे:
- A और B अभिकारक हैं।
- सी और डी उत्पाद हैं।
- ए, बी, सी, डी स्टोइकोमेट्रिक गुणांक हैं (एक निश्चित प्रकार के अणुओं या परमाणुओं की संख्या जो एक रासायनिक समीकरण में भाग लेते हैं)।
रसायनिक प्रतिक्रिया वर्गीकृत किया जा सकता है ऊर्जा के प्रकार के अनुसार वे छोड़ते या अवशोषित करते हैं। इस अर्थ में, वे एक्ज़ोथिर्मिक या एंडोथर्मिक हो सकते हैं (यदि वे रिलीज या अवशोषित करते हैं) गरम), एक्सोल्यूमिनस या एंडोल्यूमिनस (यदि वे प्रकाश को छोड़ते या अवशोषित करते हैं), एक्सोइलेक्ट्रिक या एंडोइलेक्ट्रिक (यदि वे उत्पादन करते हैं या आवश्यकता होती है) बिजली).
रासायनिक प्रतिक्रियाओं के नियम
रासायनिक प्रतिक्रियाओं में कानून पूरे होते हैं। सबसे महत्वपूर्ण है द्रव्यमान के संरक्षण का नियम या कानून ळवोइसिएर, इस रसायनज्ञ द्वारा 1774 में तैयार किया गया था, जो यह मानता है कि प्रत्येक रासायनिक प्रतिक्रिया में अभिकारकों का द्रव्यमान उत्पादों के द्रव्यमान के बराबर होता है।
ये था डाल्टन जिन्होंने इस कानून की व्याख्या कुछ साल बाद पूरी की, यह इंगित करते हुए कि रासायनिक प्रतिक्रिया में. की संख्या उत्पादों के साथ अभिकारकों की तुलना करते समय परमाणु भिन्न नहीं होते हैं, केवल उनका संगठन बदलता है, इसलिए सी. का द्रव्यमान संरक्षित करता है।
रासायनिक अभिक्रियाओं में एक अन्य महत्वपूर्ण पैरामीटर उनका है प्रतिक्रिया की गति चूंकि सभी को उत्पादन करने में समान समय नहीं लगता है। प्रतिक्रिया दर को उत्पाद की मात्रा के रूप में परिभाषित किया जाता है जो प्रति इकाई समय या अभिकर्मक की मात्रा के रूप में प्रकट होता है जो प्रति इकाई समय में गायब हो जाता है।
यद्यपि प्रत्येक प्रतिक्रिया की एक अलग गति होती है, कुछ कारक इसके बढ़ने की प्रवृत्ति पैदा कर सकते हैं या कमी: प्रतिक्रियाशील कणों और तापमान के बीच संपर्क सतह कुछ हैं वे।
उत्प्रेरक वे पदार्थ हैं जो इसकी संरचना को संशोधित किए बिना, प्रतिक्रिया की गति को बढ़ाते हैं। अक्सर यह भूमिका कुछ लोगों द्वारा पूरी की जाती है धातुओं.
रासायनिक प्रतिक्रियाओं के उदाहरण
रासायनिक प्रतिक्रियाएं प्रकृति में, मानव शरीर में, कारखानों में, अपशिष्ट उपचार संयंत्रों आदि में लगातार होती रहती हैं। कुछ उदाहरण निम्न हैं:
-
दहन
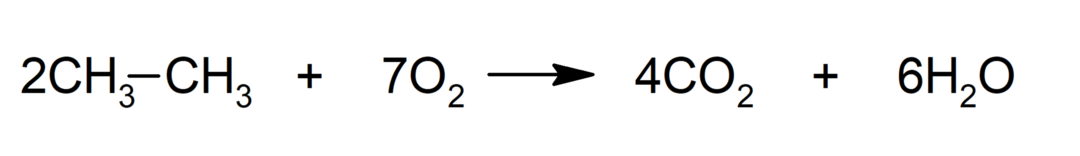
-
प्रतिस्थापन
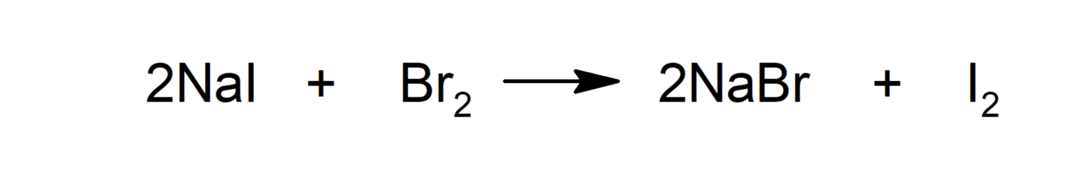
-
इसके अलावा
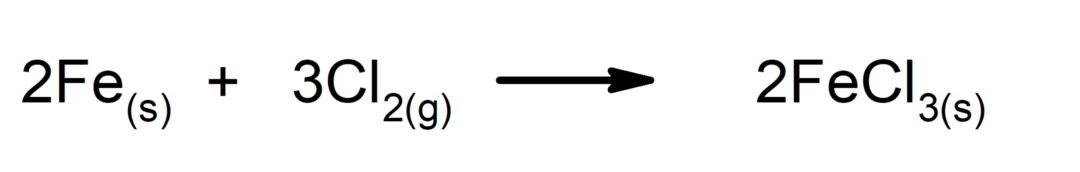
-
निकाल देना
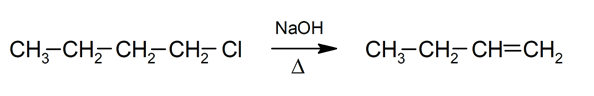
-
ऑक्सीकरण
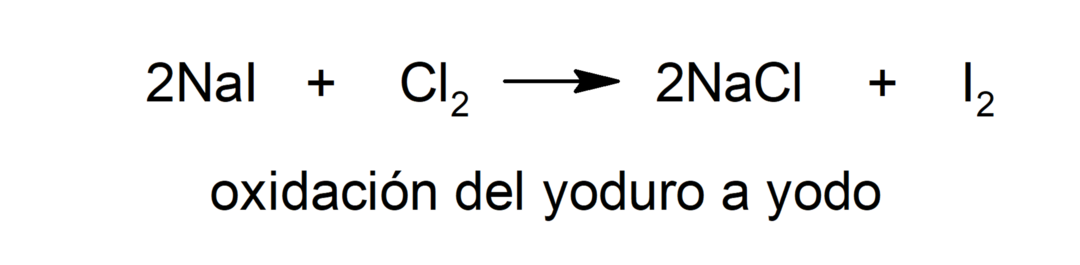
-
कमी
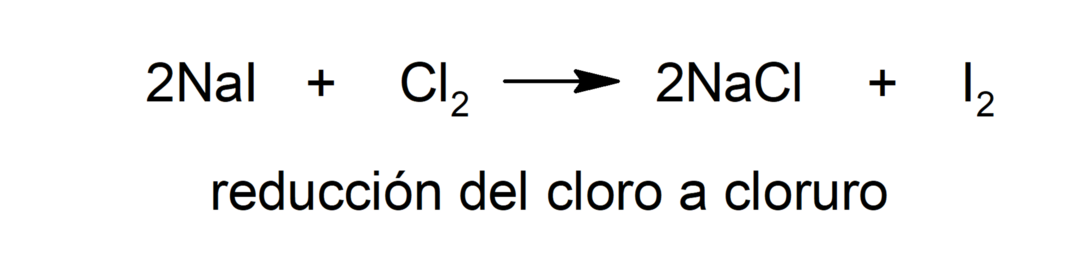
-
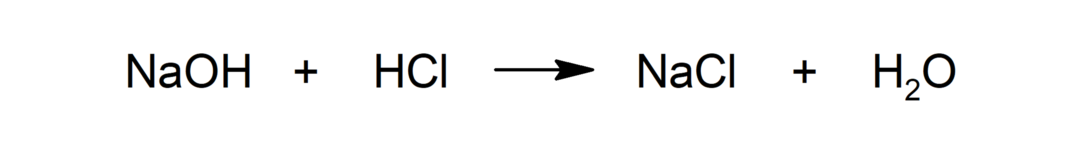
अम्ल-क्षार प्रतिक्रियाएं
-
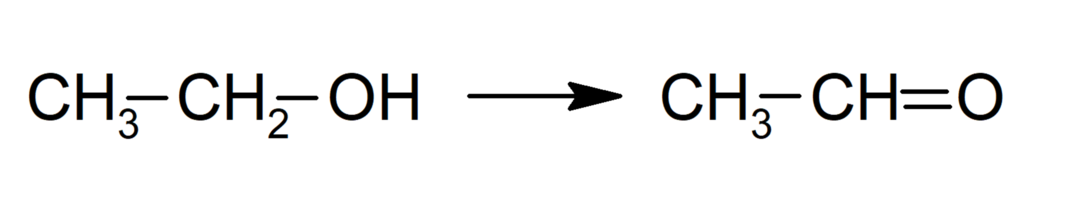
ऑक्सीजनेशन
-
ट्रांसएमिनेशन

-
क्लोरीनीकरण
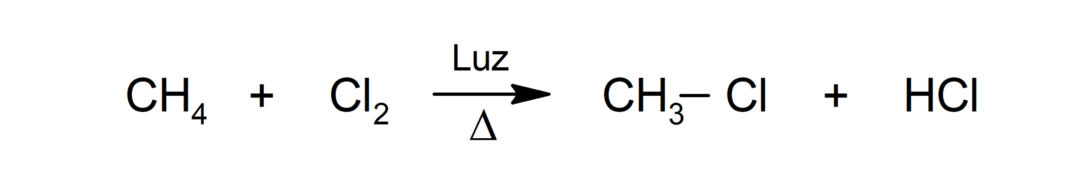
-
कार्बोनाइलीकरण

-
नाइट्रोसिलेशन. यह एक प्रतिक्रिया है जहां राइबोसोम द्वारा संश्लेषित होने के बाद नाइट्रोसिल समूह एक प्रोटीन से जुड़ा होता है।

-
पेरोक्साइडेशन
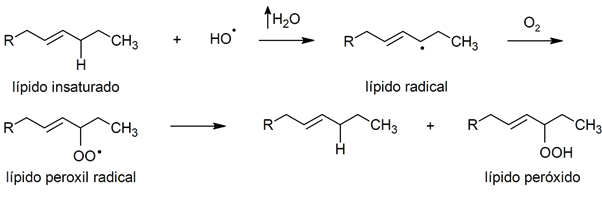
-
पानी का फोटोलिसिस
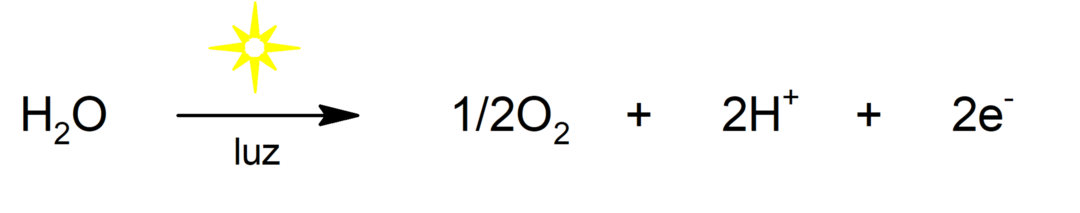
-
सल्फेशन
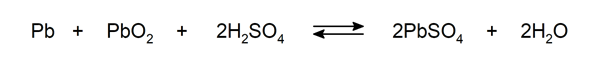
-
कार्बोनेशन
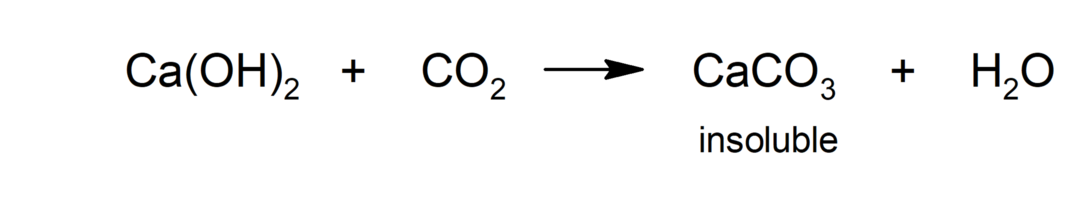
- ओजोनेशन. यह पानी को शुद्ध करने के लिए क्लोरीनीकरण की एक वैकल्पिक प्रतिक्रिया है।
-
एस्टरीफिकेशन
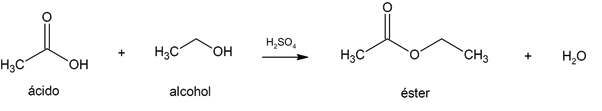
-
एल्कीनेस का हाइड्रोजनीकरण
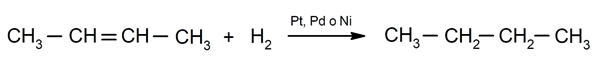
-
एसिटिलीकरण