रासायनिक तत्वों के १०० उदाहरण
अनेक वस्तुओं का संग्रह / / November 13, 2021
रासायनिक तत्व एक प्रकार का मामला है कि किसी भी प्रक्रिया से या रासायनिक प्रतिक्रिया उन्हें अन्य सरल तत्वों में कम या विघटित किया जा सकता है। इस कारण से यह कहा जा सकता है कि एक तत्व ही सब कुछ है मामला द्वारा निर्मित परमाणुओं एक ही और अद्वितीय वर्ग के, अर्थात्, परमाणु जिनकी परमाणु संख्या समान होती है (प्रोटॉन की समान संख्या), हालाँकि उनके परमाणु द्रव्यमान भिन्न होते हैं। उदाहरण के लिए: सल्फर, बोरॉन, क्रोमियम, टिन।
रासायनिक तत्व की पहली परिभाषा किसके द्वारा प्रस्तुत की गई थी? ळवोइसिएर में ट्रैटे एलेमेंटेयर डी चिमिआ, 1789 में। 18 वीं शताब्दी में वापस, लैवोज़ियर ने साधारण पदार्थों को चार समूहों में विभाजित किया:
समय समय पर तत्वो की तालिका
आज वे एक दूसरे को जानते हैं ११८ रासायनिक तत्व. वे सभी तत्वों की आवर्त सारणी के रूप में जानी जाने वाली ग्राफिक योजना में उनकी कई संपत्तियों के अनुसार एकत्रित, वर्गीकृत और व्यवस्थित हैं, जो मूल रूप से रूसी रसायनज्ञ द्वारा बनाई गई थी। दिमित्री मेंडेलीव १८६९ में। आवर्त सारणी 18 समूहों (स्तंभों) और 7 आवर्तों (पंक्तियों) से बनी है, जिसमें रासायनिक तत्व स्थित हैं।
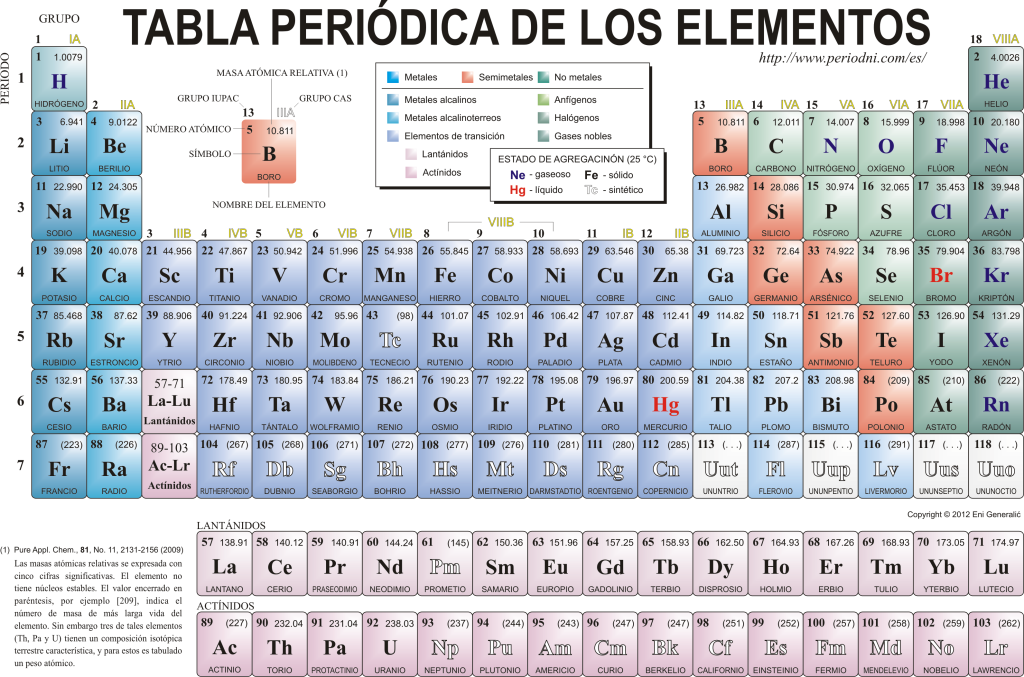
मुख्य समूह जो इस तालिका में पाया जा सकता है:
क्षार धातु (समूह 1), क्षारीय पृथ्वी धातु (समूह 2), स्कैंडियम परिवार, जिसमें पृथ्वी और एक्टिनाइड्स (समूह 3), टाइटेनियम परिवार शामिल हैं (समूह ४), वैनेडियम परिवार (समूह ५), क्रोमियम परिवार (समूह ६), मैंगनीज परिवार (समूह ७), लौह परिवार (समूह ८), कोबाल्ट परिवार (समूह) 9), निकेल परिवार (समूह 10), तांबा परिवार (समूह 11), जस्ता परिवार (समूह 12), पृथ्वी तत्व (समूह 13), कार्बोनिड तत्व, इस समूह में हैं कार्बन, जो पृथ्वी पर जीवन का आधार है (समूह 14), नाइट्रोजन बनाने वाले तत्व (समूह 15), एम्फीजेनेटिक तत्व, ऑक्सीजन शामिल है, जो कि एक मौलिक तत्व है साँस लेने का की जीवित प्राणियों (समूह १६), हैलोजन तत्व (समूह १७) और उत्कृष्ट गैसें (समूह १८)।
इनमें से कई तत्वों में स्थिर या रेडियोधर्मी समस्थानिक, अर्थात्, एक ही रासायनिक तत्व, उदाहरण के लिए, हाइड्रोजन (H), में कई समस्थानिक हो सकते हैं (1एच, 2एच, 3एच)। इसका मतलब यह है कि प्रत्येक आइसोटोप परमाणु में समान संख्या में प्रोटॉन होते हैं (जिसका अर्थ है कि यह एक ही रासायनिक तत्व से संबंधित है) और न्यूट्रॉन की एक अलग संख्या है।
कुछ समस्थानिक स्थिर (रेडियोधर्मी) नहीं होते हैं, अर्थात्, बिखर एक निश्चित समय में, कुछ कण (न्यूट्रॉन, फोटॉन, अल्फा कण, दूसरों के बीच) का उत्सर्जन करते हैं और अन्य स्थिर या रेडियोधर्मी समस्थानिक उत्पन्न करते हैं। रासायनिक तत्वों में बिंदु जैसे गुण होते हैं उबलना और वह विलय, विद्युत ऋणात्मकता, घनत्व और आयनिक त्रिज्या, दूसरों के बीच में। ये गुण महत्वपूर्ण हैं क्योंकि वे हमें इसके व्यवहार, प्रतिक्रियाशीलता आदि की भविष्यवाणी करने की अनुमति देते हैं।
आवर्त सारणी में तत्वों को कैसे प्रस्तुत किया जाता है?
प्रत्येक रासायनिक तत्व की विशेषता है आवर्त सारणी कुछ सिम्बोलॉजी का उपयोग करना। सबसे पहले, प्रत्येक वर्ग के केंद्र में इसका सार्वभौमिक प्रतीक होता है, जिसमें एक या दो. होते हैं पत्र (सम्मेलन के अनुसार, यदि दो अक्षर हैं, तो पहला अपरकेस में और अगला लोअरकेस में लिखा जाता है)।
ऊपर और बाईं ओर छोटे टाइपफेस में दिखाई देता है su परमाणु क्रमांक, जो वह है जो इस तत्व के प्रोटॉन की मात्रा को इंगित करता है। तत्व चिन्ह के नीचे उसका नाम और ऊपर बाईं ओर उसका नाम दिखाई देता है। परमाणु भार रिश्तेदार। इसके अलावा, जिस रंग में तत्व प्रतीक का प्रतिनिधित्व किया जाता है, वह उसके एकत्रीकरण की स्थिति को दर्शाता है (प्रत्येक आवर्त सारणी में प्रयुक्त प्रतिनिधित्व के अनुसार)।
मौजूद विभिन्न तत्व परमाणु त्रिज्या चर और, जैसे-जैसे नाभिक में प्रोटॉन की संख्या बढ़ती है, नाभिक जितना अधिक आकर्षण इलेक्ट्रॉनों पर लगाता है, इसलिए परमाणु त्रिज्या कम हो जाती है। जब परमाणु त्रिज्या छोटा होता है, तो बादल के सबसे बाहरी स्तर पर इलेक्ट्रॉन नाभिक की ओर बहुत आकर्षित होते हैं, इसलिए वे आसानी से हार नहीं मानते हैं। उच्च परमाणु त्रिज्या वाले तत्वों के साथ विपरीत होता है: वे अपने बाहरी इलेक्ट्रॉनों को आसानी से छोड़ देते हैं।
इस प्रकार, जब हम आवर्त सारणी के समूहों से गुजरते हैं तो परमाणु त्रिज्या ऊपर से नीचे तक बढ़ जाती है और जैसे-जैसे हम उनके आवर्त में जाते हैं, बाएं से दाएं घटते जाते हैं।
रासायनिक तत्वों के उदाहरण
| रासायनिक तत्व | प्रतीक |
| जंगी | एसी |
| अल्युमीनियम | तक |
| रेडियोऐक्टिव | बजे |
| सुरमा | एसबी |
| आर्गन | एआर |
| हरताल | ऐस |
| अस्त्ता | पर |
| गंधक | रों |
| बेरियम | बी 0 ए |
| फीरोज़ा | होना |
| बर्कीलियम | बीके |
| विस्मुट | द्वि |
| बोहरियो | बिहार |
| बोरान | ख |
| ब्रोमिन | बीआर |
| कैडमियम | सीडी |
| कैल्शियम | एसी |
| कलिफ़ोरनियम | सीएफ़ |
| कार्बन | सी |
| सैरियम | चुनाव आयोग |
| सीज़ियम | सी |
| क्लोरीन | क्लोरीन |
| कोबाल्ट | सीओ |
| तांबा | घन |
| क्रोम | सीआर |
| क्यूरियम | से। मी |
| डार्मस्टेडियो | डी एस |
| डिस्प्रोसियम | डीवाई |
| dubnium | डाटाबेस |
| आइंस्टिनियम | यह है |
| एर्बियम | एर |
| स्कैंडियम | अनुसूचित जाति |
| टिन | एस.एन. |
| स्ट्रोंटियम | श्री ग |
| युरोपियम | यूरोपीय संघ |
| फेर्मियम | एफएम |
| एक अधातु तत्त्व | एफ |
| मैच | पी |
| फ़्रांसिअस | फादर |
| गैडोलीनियम | गोलों का अंतर |
| गैलियम | गा |
| जर्मेनियम | जीई |
| हेफ़नियम | एचएफ |
| हसियो | एच |
| हीलियम | मेरे पास है |
| हाइड्रोजन | एच |
| लोहा | आस्था |
| होल्मियम | हो |
| भारतीय | में |
| आयोडीन | मैं |
| इरिडियम | जाना |
| यटरबियम | वाई बी |
| yttrium | यू |
| क्रीप्टोण | कृ |
| लेण्टेनियुम | |
| लॉरेंसियो | एलआर |
| लिथियम | ली |
| ल्यूटेशियम | सोमवार |
| मैगनीशियम | मिलीग्राम |
| मैंगनीज | एम.एन. |
| मिटनेरियस | मीट्रिक टन |
| मेण्डेलीवियम | मोहम्मद |
| बुध | एचजी |
| मोलिब्डेनम | एमओ |
| Neodymium | ना |
| नीयन | Ne |
| नैप्टुनियम | एनपी |
| नाइओबियम | नायब |
| निकल | न |
| नाइट्रोजन | नहीं |
| नोबेलियो | नहीं |
| सोना | औ |
| आज़मियम | आप |
| ऑक्सीजन | या |
| दुर्ग | पीएस |
| चांदी | एजी |
| प्लैटिनम | पीटी |
| लीड | पंजाब |
| प्लूटोनियम | पीयू |
| एक विशेष तत्त्व जिस का प्रभाव रेडियो पर पड़ता है | पीओ |
| पोटैशियम | क |
| प्रेसियोडीमियम | पीआर |
| वादा | सायं |
| एक प्रकार का रसायनिक मूलतत्त्व | देहात |
| रेडियो | आरए |
| रेडोन | आर एन |
| रेनीयाम | पुन |
| रोडियाम | राहु |
| रूबिडीयाम | आरबी |
| दयाता | आरयू |
| रदरफोर्डियो | आरएफ |
| सैमरियम | तु |
| सीबोर्गियो | एसजी |
| सेलेनियम | मैं जनता |
| सिलिकॉन | हाँ |
| सोडियम | ना |
| थालियम | टी एल |
| टैंटलम | टा |
| टेक्नेटियम | टीसी |
| टेल्यूरियम | चाय |
| टर्बियम | टीबी |
| टाइटेनियम | आप |
| थोरियम | वें |
| थ्यूलियम | टीएम |
| कोपरनिकस | सीएन |
| लिवरमोरियो | ल्वी |
| रोएंटजेनियो | आरजी |
| युनुनोक्टियम | उउओ |
| अनपेंशियम | उउप |
| फ्लेरोवियो | फ्लोरिडा |
| अनसेप्टियो | नया |
| अनन्ट्रियम | यूटा |
| यूरेनियम | या |
| वैनेडियम | वी |
| टंगस्टन | वू |
| क्सीनन | ज़ी |
| जस्ता | Zn |
| zirconium | Zr |

साथ में पीछा करना:
