परिभाषा एबीसी. में अवधारणा
अनेक वस्तुओं का संग्रह / / December 09, 2021
वैचारिक परिभाषा
हाइड्रोलिसिस को किसी पदार्थ के साथ पानी की किसी भी प्रतिक्रिया के रूप में समझा जाता है जो पानी के आयनीकरण संतुलन के विस्थापन का उत्पादन करता है।

रासायनिक इंजीनियर
घटना तब होती है, उदाहरण के लिए, जब नमक घुल जाता है पानीजहां नमक, जो एक इलेक्ट्रोलाइट है, पूरी तरह से आयनित होता है और पानी के साथ प्रतिक्रिया करने पर हाइड्रॉक्सिल या हाइड्रोनियम बना सकता है। लवण के वियोजन से a. का pH मान विघटन यह जानते हुए कि चरित्र जितना ऊंचा होगा अम्ल या यौगिक का मूल, हाइड्रोलिसिस प्रभाव जितना कम होगा।
मजबूत और कमजोर एसिड
आइए एचसीएल जैसे विशिष्ट उदाहरण पर विचार करें, यह एक मजबूत एसिड है जो आयनित होने पर निम्नानुसार व्यवहार करता है:
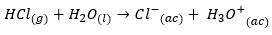
हाइड्रोलिसिस के प्रभाव का अध्ययन करने के लिए हम संयुग्म आधार पर ध्यान केंद्रित करते हैं: सी {एल ^ -} {(एसी)}, यह आयन एक है कमजोर संयुग्मी आधार, यानी पानी से प्रोटॉन लेने की कमजोर प्रवृत्ति a. बनाने के लिए होती है हाइड्रॉक्साइड। जबकि, अगर हम एक कमजोर एसिड के बारे में सोचते हैं, उदाहरण के लिए:
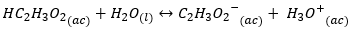
इसका संयुग्मी आधार C_2 {{H_3O_2} ^ -} _ {(ac)} \ का एक मजबूत मूल चरित्र होगा, इससे हाइड्रॉक्साइड का निर्माण होगा:
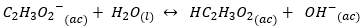
पूर्व संतुलन प्रतिक्रिया की सीधी दिशा में दाईं ओर स्थानांतरित हो जाता है और, परिणामस्वरूप, इस आयन में पीएच को प्रभावित करने की उच्च क्षमता होती है उत्पादन हाइड्रॉकसिल। जबकि Cl- के मामले में, घोल के pH पर कोई प्रभाव नहीं पड़ता है।
यदि संयुग्म आधार, आयन, है a प्रजातियां पानी से प्रोटॉन लेने में सक्षम है, तो OH- के बनने के कारण घोल का pH बढ़ जाता है।
मजबूत और कमजोर आधार
आइए अब हम मजबूत या कमजोर आधारों के मामले को देखें जो पानी में आंशिक रूप से या पूरी तरह से आयनित होते हैं और समाधान के पीएच को प्रभावित कर सकते हैं या नहीं भी कर सकते हैं।
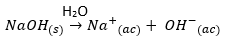
यदि हम {{Na} ^ +} {(ac)}, एक छोटा धनायन, एक कमजोर अम्ल लेते हैं, तो यह किसी विलयन के pH को प्रभावित नहीं करेगा, क्योंकि यह पानी को प्रोटॉन देने में सक्षम नहीं है। जब तक:
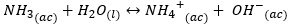
धनायन {{NH_4} ^ +} {(ac)} एक प्रबल अम्ल है, जो दुर्बल क्षार (अमोनिया) से आता है। इसलिए, इसमें पानी (हाइड्रोलाइज़) के लिए एक प्रोटॉन दान करने की क्षमता इस प्रकार है:
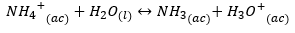
यह बताता है कि हाइड्रोनियम के गठन को देखते हुए पानी में अमोनिया का विघटन पीएच को कम क्यों करता है। इस मामले में, विस्थापन संतुलन दाईं ओर है।
लवणों का विघटन
जिस तरह हमने धनायनों और ऋणायनों के अलग-अलग प्रभाव को देखा, जब वे घुल जाते हैं तुम बाहर जाओ पानी में दोनों प्रभाव संयुक्त होते हैं और, पानी के साथ प्रतिक्रिया करने के लिए आयनों की सापेक्ष क्षमता के आधार पर, हाइड्रॉक्सिल हाइड्रॉक्सिल का निर्माण हाइड्रोनियम पर या इसके विपरीत प्रबल होगा।
इसे बेहतर ढंग से समझने के लिए, हम कुछ मामलों पर काम करेंगे:
- अगर हम टेबल सॉल्ट को पानी में घोलें, तो उपाय हमारे पास Na + धनायन और Cl- आयन होंगे। जैसा कि हमने पहले देखा, दोनों प्रजातियों में पानी के साथ प्रतिक्रिया करने की क्षमता बहुत कम है, इसलिए, दोनों में से कोई भी आधार जल के पीएच को संशोधित करने में सक्षम नहीं होगा। तब यह उम्मीद की जाती है कि पीएच 7 है। इस मामले में, एक मजबूत आधार संयुग्मित कटियन भंग हो जाता है, यह एक कमजोर एसिड होगा जो पीएच को प्रभावित नहीं करता है। और मजबूत एसिड का संयुग्मित आयन, एक कमजोर आधार, पीएच को भी नहीं बदलता है।
- दूसरी ओर, यदि एक नमक जिसका कमजोर आधार का संयुग्मित धनायन भंग हो जाता है, तो वह एक मजबूत अम्ल होता है। जबकि, यदि ऋणायन एक मजबूत अम्ल के साथ संयुग्मित होता है, तो यह एक कमजोर आधार होगा जो पानी के साथ प्रतिक्रिया करने में असमर्थ होगा। प्रबल संयुग्मित अम्ल की प्रबल संयुग्मित अम्ल की पानी के साथ प्रोटॉन दान करने वाली और पीएच कम करने की प्रतिक्रिया क्या होगी।
- विपरीत तब होता है जब धनायन एक मजबूत आधार संयुग्म (कमजोर एसिड) होता है और आयन एक कमजोर एसिड संयुग्म (मजबूत आधार) होता है। पानी के साथ मजबूत आधार की प्रतिक्रिया क्या प्रबल होगी, ओएच- के उत्पादन में वृद्धि और परिणामस्वरूप पीएच में वृद्धि होगी।
- अंत में, यह ऐसा मामला हो सकता है जहां आयन और धनायन मजबूत आधार और एसिड होते हैं जो पीएच को प्रभावित कर सकते हैं। इस मामले में, यह देखा जाना चाहिए कि कौन सी प्रतिक्रिया दूसरे पर प्रबल होती है, यदि ओएच- या एच 3 ओ + का गठन होता है। ऐसा करने के लिए, हमें अम्लता और क्षारीयता स्थिरांक का सहारा लेना चाहिए: यदि अम्लता स्थिरांक मूलता स्थिरांक से अधिक है, तो pH 7 से कम होगा। इसके विपरीत, यदि क्षारीयता स्थिरांक अम्लता स्थिरांक पर प्रबल होती है, तो pH 7 से अधिक होगा। संक्षेप में, जब दोनों स्थिरांक समान होते हैं, तो pH = 7 और अध्ययन किए गए पहले मामले के समान होता है।
हाइड्रोलिसिस में विषय