आणविक ज्यामिति की परिभाषा
अनेक वस्तुओं का संग्रह / / January 11, 2022
वैचारिक परिभाषा
यह एक अणु की संरचना है जो अंतरिक्ष में इसे बनाने वाले परमाणुओं की त्रि-आयामी व्यवस्था को निर्धारित करती है।

रासायनिक इंजीनियर
आणविक ज्यामिति को वर्तमान में के आधार पर परिभाषित किया गया है सिद्धांत वालेंसिया परत (TRPECV) के इलेक्ट्रॉनिक जोड़े के प्रतिकर्षण का। यह सिद्धांत व्यवहार की भविष्यवाणी करने की अनुमति देता है रासायनिक पदार्थों का (विशेष रूप से सहसंयोजक) और समझने में मदद करता है वितरण इलेक्ट्रॉनिक्स, के लिए अग्रणी ज्यामिति का अणु. यह, बदले में, हमें उन कई गुणों को समझने की अनुमति देता है जो पदार्थ प्राप्त करते हैं।
यह सिद्धांत मूलभूत स्तंभों की एक श्रृंखला पर आधारित है जिनकी हम समीक्षा करेंगे और फिर उन्हें समझने की कोशिश करेंगे आवेदन अभ्यास। सबसे पहले, बंधुआ और असंबद्ध (वैलेंस) इलेक्ट्रॉनों को इलेक्ट्रॉनों के समुद्र के रूप में माना जाता है, जिसके द्वारा उनके पास एक ही प्रकार का आवेश होता है, वे एक दूसरे को प्रतिकर्षित करते हैं, इसलिए वे हमेशा के केंद्रीय परमाणु से दूर स्थित होंगे अणु
दूसरा, इलेक्ट्रॉनों का यह "समुद्र" या "इलेक्ट्रॉनिक बादल" उच्च इलेक्ट्रॉन घनत्व के क्षेत्र बनाता है, जो बंधों में गठित होते हैं, जहां इलेक्ट्रॉनों को साझा किया जाता है या इलेक्ट्रॉनों के जोड़े में साझा नहीं किया जाता है। बदले में, बनने वाले बांड सिंगल, डबल या ट्रिपल हो सकते हैं।
अंत में, के लिए निर्णय करना आणविक ज्यामिति, लुईस संरचना का होना बहुत मददगार है, जहां केंद्रीय परमाणु के चारों ओर इलेक्ट्रॉन घनत्व की मात्रा की गणना की जाएगी और यह देगा संकेत इसकी ज्यामिति के नाम से और उस आकार से जो अणु त्रि-आयामी रूप से लेता है।
यह ध्यान दिया जाना चाहिए कि सबसे स्थिर संरचना को अपनाने के लिए और जहां कम प्रतिकर्षण है, इन घनत्वों को यथासंभव दूर स्थित किया जाएगा। इस प्रकार, पहले इलेक्ट्रॉनिक ज्यामिति की पहचान की जाती है और फिर आणविक ज्यामिति की।
घनत्व के छह स्तर
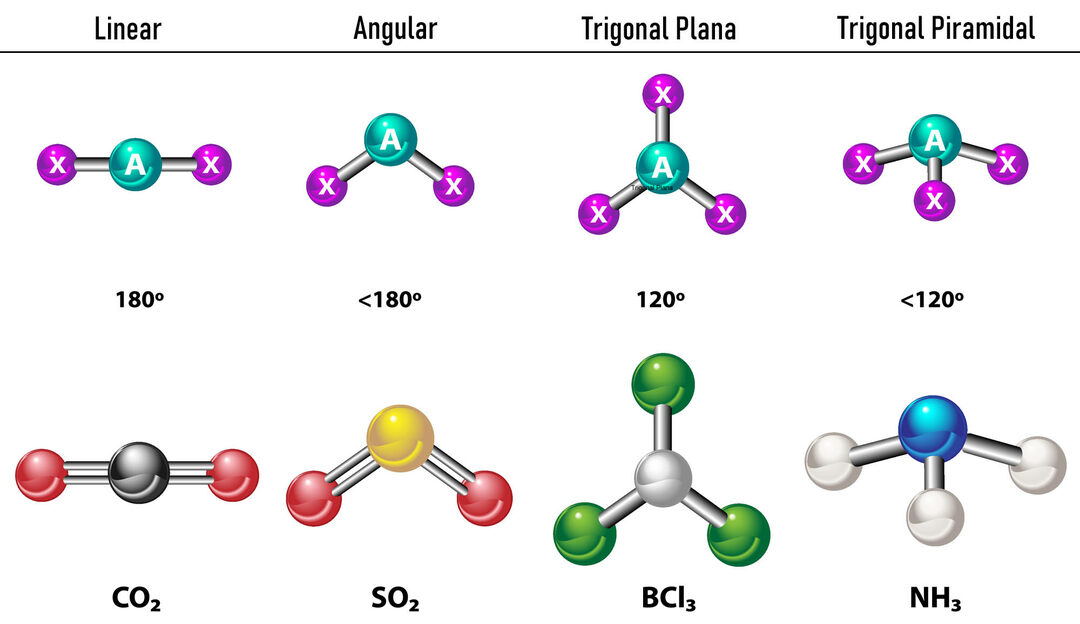
इस मामले में कि केंद्रीय परमाणु के चारों ओर दो इलेक्ट्रॉन घनत्व हैं, बांड दूर स्थित होंगे उनके बीच, यानी 180º एक दूसरे से और इसलिए, उनकी इलेक्ट्रॉनिक ज्यामिति रैखिक है और आणविक रूप से यह रैखिक भी है।
इस मामले में कि केंद्रीय परमाणु के चारों ओर तीन इलेक्ट्रॉन घनत्व हैं, दो विकल्प हैं: तीन बंधन या दो बंधन और एक अनबाउंड जोड़ी। यदि तीन बंध हैं, तो इलेक्ट्रॉनिक ज्यामिति है त्रिकोणीय फ्लैट, बंधों और आणविक ज्यामिति के बीच 120º कोणों के साथ एक ही नाम लेता है। अब, यदि कोई अबंध युग्म है, तो वे एक दूसरे को अधिक से प्रतिकर्षित करते हैं तीव्रता इसलिए बंधुआ आवेश बंध कोणों को संकुचित करते हैं। मुक्त जोड़ी और प्रत्येक बंधन के बीच का कोण 120º है और इलेक्ट्रॉनिक ज्यामिति त्रिकोणीय विमान है जबकि आणविक ज्यामिति कोणीय है।
इस मामले में कि केंद्रीय परमाणु के चारों ओर चार इलेक्ट्रॉन घनत्व हैं, इलेक्ट्रॉनिक ज्यामिति चतुष्फलकीय है। यदि इलेक्ट्रॉनों के सभी चार जोड़े बंधे हैं, तो उनकी आणविक ज्यामिति उनके इलेक्ट्रॉनिक ज्यामिति के नाम से मेल खाती है और बंधन कोण 109.5º है। अब, यदि जोड़ों में से एक मुक्त है, तो बंधन कोण छोटा हो जाता है (107º) और आणविक ज्यामिति टाइप. है त्रिकोणीय पिरामिड. अंत में, यदि दो मुक्त जोड़े हैं और दो बंधे हैं, तो बंधन कोण 104.5º है जबकि आणविक ज्यामिति कहा जाता है कोणीय.
जब केंद्रीय परमाणु के चारों ओर इलेक्ट्रॉन घनत्व पांच हो जाता है, तो इसे a. कहा जाता है त्रिकोणीय द्विपिरामिड इसकी इलेक्ट्रॉनिक ज्यामिति। यदि सभी भार जुड़े हुए हैं, तो भूमध्यरेखीय रूप से स्थित लिंक के बीच 120ºC और भूमध्यरेखीय वाले अक्षीय के बीच 90º के कोण हैं। अब, आणविक ज्यामिति को त्रिकोणीय द्विपिरामिड भी कहा जाता है, जबकि चार जुड़े जोड़े और एक मुक्त जोड़ी होने पर, आणविक ज्यामिति विकृत हो जाती है जिससे प्रसिद्ध "घुमाव”, वहाँ इसका नाम प्राप्त होता है विकृत टेट्राहेड्रोन. जबकि, यदि इलेक्ट्रॉनों के पांच जोड़े में से दो मुक्त हैं और उनमें से तीन बंधित हैं, तो इसकी एक "T"-आकार की ज्यामिति है और इसका नाम ठीक इसकी संरचना के कारण है। अंत में, यदि यह विपरीत है, तो तीन मुक्त जोड़े और दो बंधुआ चार्ज, आणविक ज्यामिति रैखिक है।
अंत में, केंद्रीय परमाणु के चारों ओर छह इलेक्ट्रॉन घनत्व होते हैं और एक अष्टफलक बनता है, इसलिए इसका नाम इलेक्ट्रॉनिक ज्यामिति में है। इसी तरह, आणविक ज्यामिति का नाम दिया जाता है यदि इसके सभी जोड़े जुड़े हुए हैं। यदि आपके पास पांच जुड़े जोड़े और एक मुक्त जोड़ी है, तो आणविक ज्यामिति स्क्वायर बेस पिरामिड है। यदि आपके पास चार बंधित जोड़े और दो मुक्त जोड़े हैं, तो आणविक ज्यामिति है स्क्वायर फ्लैट.
चित्र: मीठी प्रकृति
आण्विक ज्यामिति में विषय


