लैंथेनाइड लक्षण
रसायन विज्ञान / / July 04, 2021
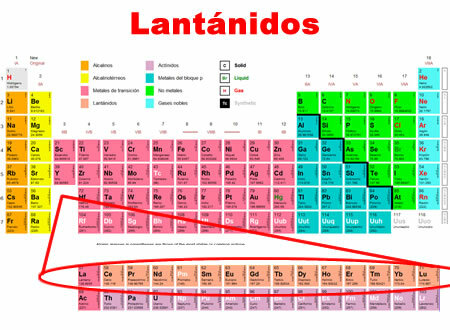
लैंथेनाइड्स रासायनिक तत्व हैं जो लैंथेनम से लेकर ल्यूटेटियम तक होते हैं। वे सामान्य विशेषताओं को साझा करते हैं, जिसके लिए उन्हें आवर्त सारणी के निचले भाग में एक विशेष श्रेणी में वर्गीकृत किया गया है।
लैंथेनाइड्स की मुख्य विशेषताएं:
- वे आवर्त सारणी की अवधि 6 में स्थित हैं।
- वे 57 से 71 तक 15 तत्वों को कवर करते हैं।
- वे लैंथेनम की संरचना को साझा करते हैं, जिसमें एक ऊर्जा स्तर f जोड़ा जाता है, जो रासायनिक रूप से कम प्रतिक्रियाशील होता है।
- उन्हें दुर्लभ पृथ्वी कहा जाता था क्योंकि प्राकृतिक अवस्था में वे हमेशा ऑक्साइड बनाने के लिए संयुक्त होते हैं।
- कुछ अपेक्षाकृत प्रचुर मात्रा में हैं।
- हालांकि उनके पास परिवर्तनीय वैलेंस हैं, अधिकांश में वैलेंस +3 है।
- जैसे-जैसे इसकी परमाणु संख्या बढ़ती है, इसकी त्रिज्या घटती जाती है।
- वे सभी एक चमकदार धातु की तरह दिखते हैं।
लैंथेनाइड्स की व्यक्तिगत विशेषताएं:
लैंथेनम (ला)।
- परमाणु क्रमांक 57
- परमाणु भार: 139
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: 920 डिग्री सेल्सियस
- क्वथनांक: 3457 डिग्री सेल्सियस
इसकी खोज 1839 में हुई थी। उद्योग में इसका उपयोग अन्य लैंथेनाइड्स के साथ मिश्र धातुओं में हल्का पत्थर बनाने के लिए किया जाता है; प्रकाशिकी में इसका उपयोग ऑप्टिकल चश्मे के लिए किया जाता है। इसका उपयोग हाइड्रोजन स्पंज के लिए भी किया जाता है, जिसमें गैसें होती हैं। दवा में इसका उपयोग गुर्दे की विफलता के उपचार के लिए लैंथेनम कार्बोनेट के रूप में किया जाता है, क्योंकि इसमें फॉस्फेट के साथ मिश्रण करने के लिए एक आत्मीयता होती है, जिससे हाइपरफॉस्फेमिया कम होता है।
सेरियम (सीई)
- परमाणु संख्या 58
- परमाणु भार: 140
- राज्य: नरम ठोस
- सूरत: धात्विक, सिल्वर ग्रे, आयरन जैसा
- वालेंसियास: +3, +4
- गलनांक: 798 डिग्री सेल्सियस
- क्वथनांक: 3426 डिग्री सेल्सियस
इसकी खोज 1803 में हुई थी। यह सबसे प्रचुर मात्रा में लैंथेनाइड है। इसका उपयोग उत्प्रेरक बनाने के लिए किया जाता है, मुख्य रूप से ऑटोमोबाइल (उत्प्रेरक कन्वर्टर्स) और तेल क्रैकिंग के लिए। ऑक्साइड के रूप में इसका उपयोग चश्मे और लेंस को चमकाने के लिए किया जाता है। यद्यपि इसका कोई ज्ञात जैविक कार्य नहीं है, चिकित्सा में इसका उपयोग जले हुए मलहम में किया जाता है।
प्रेजोडायमियम (पीआर)
- परमाणु क्रमांक 59
- परमाणु भार: 144
- राज्य: नरम ठोस
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: 931 डिग्री सेल्सियस
- क्वथनांक: 3520 डिग्री सेल्सियस
इसे 1841 में खोजा गया था और 1885 में इसे अलग कर दिया गया था। उद्योग में इसका उपयोग मैग्नीशियम के साथ मिश्र धातुओं में हवाई जहाज के इंजन बनाने के लिए किया जाता है; इसका उपयोग कांच और तामचीनी को पीला रंग देने के लिए किया जाता है। निकल मिश्र धातुओं में चुंबकीय गुण होते हैं। फ्लोराइड, क्लोराइड, ब्रोमाइड और आयोडाइड का उत्पादन करने के लिए हैलोजन के साथ प्रतिक्रिया करता है।
नियोडिमियम (एनडी)
- परमाणु क्रमांक 60
- परमाणु भार: 139
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: 1024 डिग्री सेल्सियस
- क्वथनांक: 3100 डिग्री सेल्सियस
यह १८८५ में खोजा गया था, जब प्रेजोडायमियम को अलग किया गया था; 1925 तक नियोडिमियम को अलग कर दिया गया था। यह सबसे अधिक प्रतिक्रियाशील लैंथेनाइड्स में से एक है। उद्योग में इसका उपयोग कांच और तामचीनी को रंगने के लिए किया जाता है। प्रकाश को अवशोषित करने की इसकी क्षमता के कारण, इसका उपयोग खगोल विज्ञान में क्रिस्टल बनाने के लिए किया जाता है जिसके साथ अवरक्त स्पेक्ट्रोमीटर और फिल्टर को कैलिब्रेट किया जाता है। इसका एक मुख्य उपयोग उच्च चुंबकीय तीव्रता के चुम्बक बनाना है। इन चुम्बकों का उपयोग सटीक उपकरणों के लिए किया जाता है, जैसे कि कंप्यूटर हार्ड ड्राइव में उपयोग किए जाने वाले, साथ ही कुछ पतले प्रारूप वाले स्पीकर।
प्रोमेथियम (पीएम)
- परमाणु संख्या 61
- परमाणु भार: 145
- ठोस अवस्था
- सूरत: ?
- वालेंसियास: +3
- गलनांक: 1100 डिग्री सेल्सियस
- क्वथनांक: 3000 डिग्री सेल्सियस
इसके अस्तित्व की भविष्यवाणी १९०२ में की गई थी, लेकिन १९४४ तक इसे सिद्ध नहीं किया जा सका। यह लैंथेनाइड प्रकृति में नहीं पाया जाता है, इसके प्राप्त करने और अध्ययन का स्रोत यूरेनियम का विखंडन है। जब परमाणु रिएक्टर में यूरेनियम का विखंडन होता है, तो इस परमाणु पृथक्करण से उत्पन्न होने वाले परमाणुओं में से एक प्रोमेथियम होता है। इसमें रेडियोधर्मी विशेषताएं हैं, जो इसे फॉस्फोरेसेंस देती हैं, और इसका उपयोग अंशशोधकों और अंतरिक्ष यान में उपयोग की जाने वाली परमाणु बैटरी के लिए किया जाता है।
समैरियम (एस.एम.)
- परमाणु संख्या 62
- परमाणु भार: 150
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: १०७२ डिग्री सेल्सियस
- क्वथनांक: १८०३ डिग्री सेल्सियस
यह 1853 में खोजा गया था और 1879 में अलग किया गया था। इसके कई समस्थानिक हैं, और उनमें से कम से कम दो रेडियोधर्मी हैं। उद्योग में इसका उपयोग प्रकाशिकी में क्रिस्टल बनाने के लिए किया जाता है जो अवरक्त प्रकाश को अवशोषित करते हैं। इसका उपयोग अल्कोहल प्राप्त करने के लिए उत्प्रेरक के रूप में और कुछ फ्लोरोसेंट लैंप और टीवी में एक तत्व के रूप में भी किया जाता है। जहां तक स्वास्थ्य की बात है, यदि श्वास में लिया जाए (जैसे कि क्रिस्टल को चमकाने के लिए इस्तेमाल किया जाने वाला ऑक्साइड), तो यह फुफ्फुसीय अन्त: शल्यता का कारण बन सकता है या यकृत को प्रभावित कर सकता है। रेडियोधर्मी समस्थानिकों का उपयोग गंभीर रूप से बीमार रोगियों की रेडियोथेरेपी में किया जाता है।
यूरोपियम (यूरोपीय संघ)
- परमाणु क्रमांक 63
- परमाणु भार: 152
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +2, +3
- गलनांक: 826 डिग्री सेल्सियस
- क्वथनांक: १५२७ डिग्री सेल्सियस
इसकी खोज 1890 में हुई थी। यह लैंथेनाइड्स में सबसे अधिक प्रतिक्रियाशील है। इसका उपयोग फ्लोरोसेंट लैंप और टीवी में किया गया है, हालांकि फुफ्फुसीय अन्त: शल्यता पैदा करने के लिए यदि यह है यदि मानव शरीर में जमा हो जाए या जिगर को नुकसान पहुंचाए, तो इसका लगभग कोई औद्योगिक उपयोग नहीं है। परमाणु अनुसंधान में इसका उपयोग किया जाता है क्योंकि यह न्यूट्रॉन को अवशोषित करता है।
गैडोलिनियम (जीडी)
- परमाणु संख्या 64
- परमाणु भार: 157
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: १३१२ डिग्री सेल्सियस
- क्वथनांक: 3250 डिग्री सेल्सियस
गैडोलीनियम के कुछ उपयोग हैं, जिनमें से एक मुख्य चुंबकीय औद्योगिक प्रशीतन है, क्योंकि यह कम तापमान पर अपने चुंबकीय गुणों को बढ़ाता है; लेकिन चूंकि इस प्रकार के कूलर में आर्सेनिक के उपयोग की आवश्यकता होती है, इसलिए घरेलू प्रशीतन में उनका उपयोग नहीं किया जाता है। चिकित्सा में इसका उपयोग चुंबकीय-परमाणु अनुनाद के लिए एक विपरीत माध्यम के रूप में किया जाता है।
टर्बियम (टीबी)
- परमाणु संख्या 65
- परमाणु भार: १५९
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +4
- गलनांक: 1356 डिग्री सेल्सियस
- क्वथनांक: 3230 डिग्री सेल्सियस
इसे 1843 में खोजा गया था और 1905 में इसे अलग कर दिया गया था। यह इलेक्ट्रॉनिक्स उद्योग में बहुत महत्वपूर्ण है, क्योंकि यह अर्धचालक बनाने के लिए उपयोग किए जाने वाले तत्वों में से एक है। अन्य उपयोग फ्लोरोसेंट ट्यूब और पिक्चर ट्यूब बनाने के लिए हैं। इसका उपयोग ईंधन कोशिकाओं में उत्प्रेरक के रूप में भी किया जाता है। यद्यपि इसके जैविक कार्य नहीं होते हैं, लेकिन इसके साँस लेना या मानव शरीर में प्रवेश का विषाक्त प्रभाव होता है, जो मुख्य रूप से यकृत को प्रभावित करता है।
डिस्प्रोसियम (उप)
- परमाणु क्रमांक 66
- परमाणु भार: 162.5
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +2, +3
- गलनांक: 1407 डिग्री सेल्सियस
- क्वथनांक: 2567 डिग्री सेल्सियस
इसे 1843 में खोजा गया था और 1905 में इसे अलग कर दिया गया था। यह इलेक्ट्रॉनिक्स उद्योग में बहुत महत्वपूर्ण है, क्योंकि यह अर्धचालक बनाने के लिए उपयोग किए जाने वाले तत्वों में से एक है। अन्य उपयोग फ्लोरोसेंट ट्यूब और पिक्चर ट्यूब बनाने के लिए हैं। इसका उपयोग ईंधन कोशिकाओं में उत्प्रेरक के रूप में भी किया जाता है। यद्यपि इसके जैविक कार्य नहीं होते हैं, लेकिन इसके साँस लेना या मानव शरीर में प्रवेश का विषाक्त प्रभाव होता है, जो मुख्य रूप से यकृत को प्रभावित करता है।
होल्मियम (हो)
- परमाणु क्रमांक 67
- परमाणु भार: 166
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: 1474 डिग्री सेल्सियस
- क्वथनांक: 2700 डिग्री सेल्सियस
यह 1878 में खोजा गया था और इसका नाम लैटिन, होल्मिया में इसकी खोज के शहर, स्टॉकहोम से निकला है। इसका लगभग कोई व्यावहारिक उपयोग नहीं है; हालाँकि, इसका उपयोग कुछ उद्योगों में रासायनिक प्रतिक्रियाओं के लिए उत्प्रेरक के रूप में और साथ ही कुछ इलेक्ट्रॉनिक घटकों के लिए किया जाता है। इसका उपयोग लेजर बीम की आवृत्ति और तीव्रता को बदलने के लिए भी किया जाता है।
एर्बियम (एर)
- परमाणु संख्या 68
- परमाणु भार: 167
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: १७९५ डिग्री सेल्सियस
- क्वथनांक: 2863 डिग्री सेल्सियस
इसकी खोज 1843 में हुई थी। इसका उपयोग परमाणु उद्योग में न्यूट्रॉन बफर के रूप में किया जाता है। ऑक्साइड के रूप में यह क्रिस्टल के लिए एक रंगारंग है, जो उन्हें एक गुलाबी रंग देता है; इन क्रिस्टल का उपयोग प्रकाशिकी और गहनों में किया जाता है। इसका उपयोग फाइबर ऑप्टिक्स बनाने के लिए भी किया जाता है।
थुलियम (टीएम)
- परमाणु क्रमांक 69
- परमाणु भार: 167
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: १५४५ डिग्री सेल्सियस
- क्वथनांक: 1947 ° C
इसकी खोज 1879 में हुई थी। इसकी कम उपलब्धता के बावजूद, इसकी रेडियोधर्मी विशेषताओं के कारण, इसका मुख्य उपयोग पोर्टेबल उपकरणों में और सॉलिड-स्टेट लेजर के लिए एक्स-रे स्रोत के रूप में होता है।
येटरबियम (Yb)
- परमाणु संख्या 70
- परमाणु भार: 173
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: 824 डिग्री सेल्सियस
- क्वथनांक: 1194 डिग्री सेल्सियस
इसे 1878 में खोजा गया था और 1907 में इसे अलग कर दिया गया था। रेडियोधर्मी आइसोटोप का उपयोग पोर्टेबल एक्स-रे उपकरण के लिए किया जाता है जो बिजली के बिना काम करता है। इसका उपयोग स्टील मिश्र धातुओं में सुधार और उनके प्रतिरोध को बढ़ाने के लिए भी किया जाता है, एक विशेषता जिसका उपयोग दंत चिकित्सा में किया जाता है, स्टील के यांत्रिक गुणों में सुधार के कारण। इसे सावधानी से संभालना चाहिए क्योंकि इससे जलन और जलन हो सकती है। इसके अलावा, हवा के साथ प्रतिक्रिया करते समय, यह विस्फोट या आग का कारण बन सकता है।
ल्यूटेटियम (लू)
- परमाणु क्रमांक 71
- परमाणु भार: 175
- ठोस अवस्था
- सूरत: धातुई, चांदी सफेद
- वालेंसियास: +3
- गलनांक: 1652 डिग्री सेल्सियस
- क्वथनांक: 3402 डिग्री सेल्सियस
इसकी खोज 1907 में हुई थी। यह पृथ्वी की पपड़ी में कम से कम प्रचुर मात्रा में रासायनिक तत्व है। इसकी कम उपलब्धता के बावजूद, इसका उपयोग तेल शोधन के लिए और कार्बनिक रसायन प्रतिक्रियाओं के उत्प्रेरक के रूप में किया जाता है। विकिरण चिकित्सा उपचार के लिए कुछ रेडियोधर्मी समस्थानिकों का भी परीक्षण किया गया है।
